
【题目】用无机矿物资源生产部分材料,其产品流程示意图如下:

下列有关说法不正确的是( )
A.制取粗硅时生成的气体产物为CO
B.生产铝、铜、高纯硅及玻璃的过程中都涉及氧化还原反应
C.黄铜矿冶炼铜时,SO2可用于生产硫酸,FeO可用作冶炼铁的原料
D.粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法
科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是
A. 氧化物:CO2、NO、SO2、H2O
B. 碱:NaOH、KOH、Ba(OH)2、Na2CO3
C. 铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3·H2O
D. 碱性氧化物:Na2O、CaO、Mn2O7、Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、N2、Fe2O3、Fe 和 X。
(1)根据题意,可判断出X是_____________(写化学式)
(2)写出并配平该反应的化学方程式,并用双线桥标出电子转移的方向和数目:________________。
(3)在反应 3BrF3+5H2O=HBrO3+Br2+9HF+O2 中,被氧化的元素是____________,当有5 mol水反应时,由H2O还原的BrF3为______________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图—致的是( )
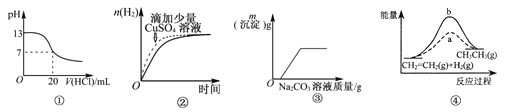
A.图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液, 溶液的pH随加入酸体积的变化
B.图②中表示常温下,两份少量等浓度的盐酸与过量锌粉反应时,其中一份滴加了少量硫酸铜溶液
C.图③表示10 mL 0.01 mol/LKMnO4酸性溶液与过量的0.1 mol/L H2C2O4溶液混合时(Mn2+是该反应的催化剂),n (Mn2+)随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) +H2(g) →CH3CH3 (g)△H < 0,使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青毒素是最早被发现及大量被采用的抗生素,下列说法错误是( )
A.使用青毒素前一定进行皮试 B.注射青毒素可能过敏休克
C.青毒素可以水解生成氨基酸 D.青毒素不能水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是______________________;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 ![]() 7N2+12H2O
7N2+12H2O
① 上述反应中被还原的元素是_________(填元素符号),反应中每转移3mol电子,生成标准状况下N2的体积为____________;
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3![]() O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
上述反应中NOx所起的作用是_____________;
(3)下表列出了2种燃煤烟气脱硫方法的原理。
方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的___________性质(选填字母编号)。
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物
②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有______(填字母).
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是_________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于N2(g)+3H2(g)![]() 2NH3(g) △H1KJ/mol,满足如下图像:
2NH3(g) △H1KJ/mol,满足如下图像:

(1)根据图判断△H1 0,T3 T4。(填“>”“<”“=”)
(2)若温度为T1且容器为2L的密闭容器下中,发生合成氨的反应,起始时通入2mol的N2和6mol的H2,10分钟达到平衡状态,此时NH3的体积分数为60%。则0到10min内用H2表示化学反应速率为_________mol/(L·min),N2的转化率为___________,反应开始和平衡状态体系的压强之比等于___________。
(3)若第(2)小问中反应体系达到平衡后,再通入1molN2和3mol的H2,则H2的转化率为___________(填“增大”“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应N2(g)+O2(g)2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是 ( )
A.恒容充入N2
B.缩小体积使压强增大
C.恒容充入氦气
D.恒压充入氦气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定质量的均匀固体混合物Cu、CuO和Cu2O,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少3.20 g,另一份中加入500 mL稀硝酸(其还原产物为NO),固体恰好完全溶解,且同时收集到标准状况下NO气体4.48 L,则所用硝酸的物质的量浓度为( )
A.2.4 mol/L B.1.4 mol/L C.1.2 mol/L D.0.7 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com