
【题目】下列关于组成细胞的化合物的叙述,正确的是( )
A. DNA是生物体各项生命活动的主要承担者
B. RNA由四种核苷酸组成,可以作为遗传物质
C. 组成淀粉、糖原、纤维素的单体都是葡萄糖
D. 肽链的盘曲和折叠被解开时,其特定功能并未发生改变
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A的相对分子质量为136,分子式为C8H8O2。A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱和核磁共振氢谱如下图。下列关于A的说法中不正确的是


A. A分子属于酯类化合物,在一定条件下能发生水解反应
B. A在一定条件下可与3 mol H2发生加成反应
C. 与A属于同类化合物的同分异构体只有4种
D. 符合题干特征的A分子结构只有1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①有机物X的相对分子质量小于180,其中氧的质量分数约为49.4%,②1molX在稀硫酸中发生水解反应生成2mol甲醇和1molA,③X中没有支链。④有机物X、A物质能发生如下图转化关系,E为高分子的化合物,B为环状结构。
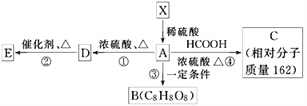
根据以上信息填写下列空白:
(1)1个X分子中,含有________个氧原子,X不可能发生的反应有________(填序号)。
①加成反应 ②酯化反应 ③氧化反应 ④消去反应
(2)写出①的反应类型_______,A分子中的官能团是(写名称)________________。
(3)写出④的化学方程式________________________________________。
(4)有机物“C8H8O8”因分子组成中含有三个国人心目中的吉利数字“8”而被称为“吉利分子”。由A转化而生成的“吉利分子”有多种不同的环状结构,写出符合条件的有机物B有__________种结构,其中的含一个六元环的有机物B结构简式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了①~⑨九种元素在周期表中的位置。
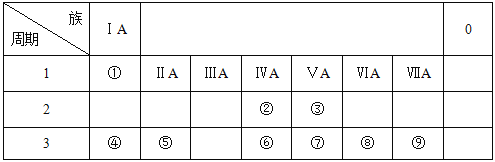
请按要求回答下列问题:
(1)⑧的原子结构示意图是__________;
(2)③、⑤、⑦三种元素的原子半径由大到小的顺序是 __________(填元素符号);
(3)元素②的气态氢化物比元素⑥的气态氢化物的稳定性较 __________(填 “强”或“弱”);
(4)④和⑨两种元素组成的化合物与AgNO3溶液反应的离子方程式是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将空气缓慢通过如图所示装置后,在试管中收集到少量稀有气体。空气在通过a~d装置时,依次除去的气体是 ( )
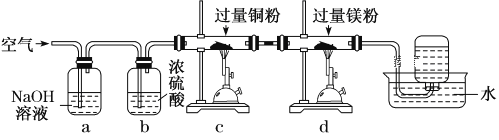
A. O2、N2、H2O、CO2 B. CO2、H2O、O2、N2
C. CO2、H2O、N2、O2 D. N2、O2、CO2、H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
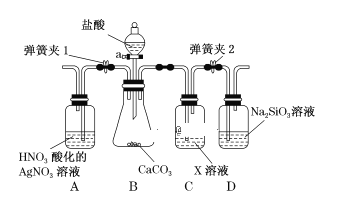
实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,…,关闭活塞a。请回答:
(1)B中反应的离子方程式是_________________________________________。
(2)通过步骤 Ⅰ、 Ⅱ 得知盐酸具有的性质是________(填字母)。
A.挥发性 B.还原性 C.氧化性 D.酸性
(3)C装置的作用是______________,X是____________________(写化学式)。
(4)为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是_______________,D中反应的化学方程式是__________________________________。
(5)碳、硅的非金属性逐渐减弱的原因是_____________________(从原子结构角度加以解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卫生部严令禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。过氧化钙(CaO2)常用作杀菌剂、防腐剂,是一种白色固体,带有结晶水,通常还含有CaO。
I、制备过氧化钙。
某实验小组选用如下装置制备过氧化钙。已知化学反应Ca2++H2O2+2NH3+xH2O===CaO2·xH2O↓+2NH4+。在碱性环境中制取CaO2·xH2O的装置如下图:
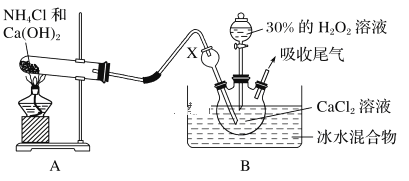
(1)装置B中仪器X的作用是_____________;反应在冰水浴中进行的原因是_________________。
(2)反应结束后,经________、________、低温烘干获得CaO2·xH2O。
II、含量测定。
(1)称取13.52 g过氧化钙样品,灼热时发生如下反应:2[CaO2·xH2O]→2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL,该样品中CaO2的物质的量为____________。
(2)另取同一样品13.52 g,溶于适量稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 7.0 g。样品中杂质CaO的质量为_____________;样品CaO2·xH2O中的x值为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到固体TiO2。用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为______________________
(2)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是:____________;使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的________(填字母代号)。
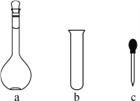
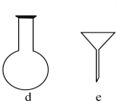
(3)滴定终点的现象是________________________________________。
(4)检验TiO2·xH2O中Cl-是否被除净的方法是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com