
【题目】化合物F是感冒药的常用成分,一种合成F的路线如下:
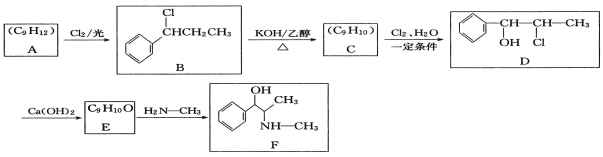
回答下列问题:
(1)A的结构简式为______。
(2)B的化学名称为_________。
(3)由C生成D的化学方程式为____________。
(4)由E生成F的反应类型为___________。
(5)F的分子式为____________。
(6)R是D的同分异构体,则同时符合下列条件的R共有___种。①只含1个甲基②苯环上有2个取代基③能与FeCl3溶液发生显色反应,其中核磁共振氢谱为6组峰,且峰面积之比为1:2:2:3:1:2的结构简式为________、_________。(任写2种)
【答案】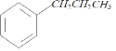 1-苯基-1-氯丙烷
1-苯基-1-氯丙烷 ![]() +Cl2+H2O
+Cl2+H2O![]() HCl+
HCl+![]() 加成反应 C10H15NO 3
加成反应 C10H15NO 3 ![]()
![]() (
(![]() )
)
【解析】
分析合成路线,A(C9H12)与Cl2在光照下反应生成B,发生的是取代反应,则A为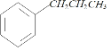 ,B在KOH、乙醇加热条件下发生消去反应生成C(C9H10),则C为
,B在KOH、乙醇加热条件下发生消去反应生成C(C9H10),则C为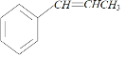 ,C与Cl2和H2O能在一定条件下反应生成D,D与Ca(OH)2发生反应生成E(C9H10O),E发生加成反应生成F,结合F的结构简式可知E为
,C与Cl2和H2O能在一定条件下反应生成D,D与Ca(OH)2发生反应生成E(C9H10O),E发生加成反应生成F,结合F的结构简式可知E为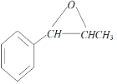 ,E与NH2-CH3反应生成F。
,E与NH2-CH3反应生成F。
(1)A(C9H12)与Cl2在光照下反应生成B,发生的是取代反应,则A为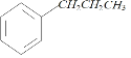 ;
;
(2)B为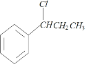 ,化学名称为1-苯基-1-氯丙烷。
,化学名称为1-苯基-1-氯丙烷。
(3)C为![]() ,D为
,D为![]() ,由C与Cl2在H2O条件下反应生成D,则反应方程式为
,由C与Cl2在H2O条件下反应生成D,则反应方程式为![]() +Cl2+H2O
+Cl2+H2O![]() HCl+
HCl+![]() 。
。
(4)E为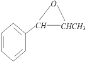 ,E与NH2-CH3反应生成F(
,E与NH2-CH3反应生成F(![]() ),由E生成F的反应类型为加成反应;
),由E生成F的反应类型为加成反应;
(5)F(![]() )的分子式为C10H15NO。
)的分子式为C10H15NO。
(6)D为![]() ,R是D的同分异构体,R的结构符合条件:①只含1个甲基,②苯环上有2个取代基,③能与FeCl3溶液发生显色反应,说明含有酚羟基,④其核磁共振氢谱为6组峰,且峰面积之比为1:2:2:3:1:2,说明含有6种H,综合考虑,则R可以为:
,R是D的同分异构体,R的结构符合条件:①只含1个甲基,②苯环上有2个取代基,③能与FeCl3溶液发生显色反应,说明含有酚羟基,④其核磁共振氢谱为6组峰,且峰面积之比为1:2:2:3:1:2,说明含有6种H,综合考虑,则R可以为: ,
, ,
, 。
。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
【题目】三氯化六氨合钴[Co(NH3)6]Cl3是橙黄色、微溶于水的配合物,是合成其它一些含钴配合物的原料。如图是某科研小组以含钴废料(含少量Fe、Al等杂质)制取[Co(NH3)6]Cl3的工艺流程:
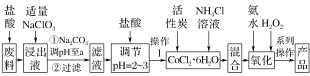
写出加“适量NaClO3”发生反应的离子方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
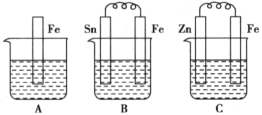
①B中Sn极的电极反应式为___________,Sn极附近溶液的pH________(填“增大”“减小”或“不变”)。
②C中总反应方程式为_________。比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是__________。
(2)如图是甲烷燃料电池工作原理示意图,回答下列问题:
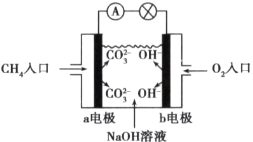
①电池的负极是__(填“a”或“b”)极,该极的电极反应式是___。
②电池工作一段时间后,电解质溶液的pH是____(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+3B(g)![]() 2C(g),ΔH=-192 kJ·mol-1。向M、N中,分别通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
2C(g),ΔH=-192 kJ·mol-1。向M、N中,分别通入x mol A和y mol B的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
![]()
A.若平衡时A气体在两容器中的体积分数相等,则x一定等于y
B.若x∶y=1∶2,则平衡时,M中的转化率:A>B
C.若x∶y=1∶3,当M中放出热量172.8 kJ时,A的转化率为90%
D.若x=1.4,y=1,N中达到平衡时体积为2L,C为0.4mol,则反应起始时N的体积为2.6L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理某废水时,反应过程中部分离子浓度与反应进程关系如下图,反应过程中主要存在N2、HCO3、ClO、CNO(C+4价,N-3价)、Cl等微粒。下列说法不正确的是

A.该废水呈强酸性
B.废水处理后转化为无害物质
C.反应的离子方程式:3ClO+2CNO+H2O == N2+2HCO3+3Cl
D.每处理1 mol CNO转移3 mol e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr![]() C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?_____________。
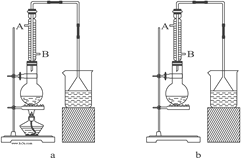
(2)反应装置中的烧瓶应选择下列哪种规格最合适(_____)
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是(_____)
A. A进B出 B. B进A出 C. 从A进或B进均可
(4)可能发生的副反应为:_____________、__________、______________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是
A.H+、Fe2+、![]() 、
、![]() B.Na+、OH-、
B.Na+、OH-、![]() 、
、![]()
C.Na+、Al3+、Cl-、![]() D.Fe3+、K+、SCN-、Cl-
D.Fe3+、K+、SCN-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯: 6 H2(g) +2CO2(g)![]() CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
CH2=CH2(g) +4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是
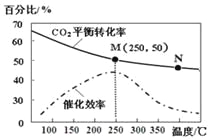
A. 生成乙烯的速率:v(M)一定小于v(N)
B. 化学平衡常数:KN>K M
C. 当温度高于250℃时,升高温度,平衡向逆反应方向移动,从而使催化剂的催化效率降低
D. 若投料比n(H2):n(CO2)=3:1,则图中M点时,乙烯的体积分数为7.7%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一些晶体中的某些结构,请回答下列问题:
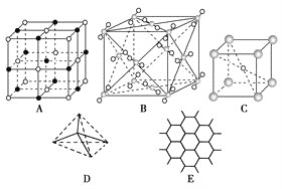
(1)代表金刚石的是(填编号字母,下同)___,其中每个碳原子与____个碳原子最近且距离相等。金刚石属于____晶体。
(2)代表石墨的是____,每个正六边形占有的碳原子数平均为____个。
(3)代表NaCl的是___,每个Na+周围与它最近且距离相等的Na+有___个。
(4)代表CsCl的是___,它属于____晶体,每个Cs+与____个Cl-紧邻。
(5)代表干冰的是___,它属于___晶体,每个CO2分子与___个CO2分子紧邻。
(6)已知石墨中碳碳键的键长比金刚石中碳碳键的键长短,则上述五种物质熔点由高到低的排列顺序为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com