
【题目】实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr![]() C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?_____________。
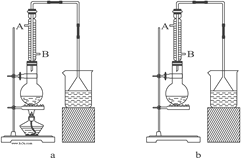
(2)反应装置中的烧瓶应选择下列哪种规格最合适(_____)
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是(_____)
A. A进B出 B. B进A出 C. 从A进或B进均可
(4)可能发生的副反应为:_____________、__________、______________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是_____________________________。
【答案】a C B C2H5OH![]() C2H4↑+H2O 2C2H5OH
C2H4↑+H2O 2C2H5OH![]() C2H5OC2H5+H2O 2HBr+H2SO4(浓)
C2H5OC2H5+H2O 2HBr+H2SO4(浓)![]() Br2+SO2↑+2H2O
Br2+SO2↑+2H2O
C2H5OH+2H2SO4(浓)![]() 2C+2SO2↑+5H2O
2C+2SO2↑+5H2O
C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O(任意选取 3 个反应即可) 将粗溴乙烷和稀NaOH(aq)的混合物放在分液漏斗中用力振荡,并不断放气,至油层无色,分液可得纯溴乙烷
CO2↑+2SO2↑+2H2O(任意选取 3 个反应即可) 将粗溴乙烷和稀NaOH(aq)的混合物放在分液漏斗中用力振荡,并不断放气,至油层无色,分液可得纯溴乙烷
【解析】
(1)由题给信息,知该反应为:C2H5-OH+HBr![]() C2H5Br+H2O,反应需要加热,所以应采用装置a;
C2H5Br+H2O,反应需要加热,所以应采用装置a;
(2)烧瓶的规格与所盛液体的体积有关,加热时烧瓶内液体的体积应小于烧瓶的容积的,V(C2H5OH)=![]() =14cm-3=14mL,忽略混合时体积变化,混合后液体的总体积约为36mL+25mL+14mL=75mL,所以150mL的烧瓶最合适,故答案为C;
=14cm-3=14mL,忽略混合时体积变化,混合后液体的总体积约为36mL+25mL+14mL=75mL,所以150mL的烧瓶最合适,故答案为C;
(3)冷凝时,水需充满冷凝器,为了防止冷凝器冷凝时,受热不均匀破裂,冷凝水应下进上出,故答案为B;
(4)可能发生的副反应有:C2H5OH脱水生成乙烯和乙醚;浓H2SO4氧化HBr;C2H5OH脱水炭化等反应.故答案为:C2H5OH![]() C2H4↑+H2O、2C2H5OH
C2H4↑+H2O、2C2H5OH![]() C2H5OC2H5+H2O、2HBr+H2SO4(浓)
C2H5OC2H5+H2O、2HBr+H2SO4(浓)![]() Br2+SO2↑+2H2O、C2H5OH+2H2SO4(浓)
Br2+SO2↑+2H2O、C2H5OH+2H2SO4(浓)![]() 2C+2SO2↑+5H2O、C+2H2SO4(浓)
2C+2SO2↑+5H2O、C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O(任意选取2个反应即可);
CO2↑+2SO2↑+2H2O(任意选取2个反应即可);
(5)棕黄色的粗溴乙烷,是由于溴乙烷溶解了Br2的缘故,可用质量分数小于5%的稀NaOH溶液洗涤除去,采用稀NaOH溶液,是为了防止C2H5Br的水解。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列实验中,现象及得出的结论正确的是()
实验 | 现象 | 结论 | |
A |
| 试管(1)中紫色褪去, 试管(2)中紫色未褪 | 甲基使苯环的活性增强 |
B |
| 试管内壁有 银镜生成 | 有机物X中一定含有醛基 |
C | 向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜悬浊液并加热 | 未见砖红色沉淀 | 淀粉未水解 |
D |
| 最后一只试管中有浅黄色沉淀 | 有机物中含有溴原子 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法不正确的是( )
A.制口罩的原料是聚丙烯,其分子式为(C3H6)n,它能使溴水褪色
B.分子式为C4H10O并能与金属钠反应放出氢气的有机物(不含立体异构)有4种
C.在一定条件下,苯与液溴、硝酸作用生成溴苯、硝基苯的反应都属于取代反应
D.聚合物(![]() )可由单体 CH2=CH2和CH3CH=CH2加聚制得
)可由单体 CH2=CH2和CH3CH=CH2加聚制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度T1和T2时,分别将0.50 mol CH4和1.20 mol NO2充入体积为1L的密闭容器中,发生如下反应:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g),测得n(CH4)随时间变化数据如下表:
时间/min | 0 | 10 | 20 | 40 | 50 | |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | … | 0.15 |
下列说法正确的是( )
A. T2时,NO2的平衡转化率为70.0%
B. 该反应的△H>0、T1<T2
C. 保持其他条件不变,T1时向平衡体系中再充入0.30molCH4和0.80molH2O(g),平衡向正反应方向移动
D. 保持其他条件不变,T1时向平衡体系中再充入0.50molCH4和1.20molNO2,与原平衡相比,达新平衡时N2的浓度增大、体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是感冒药的常用成分,一种合成F的路线如下:
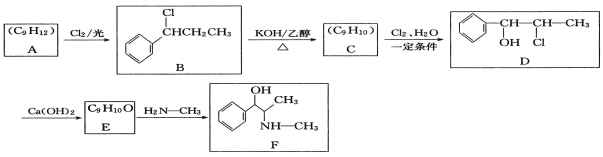
回答下列问题:
(1)A的结构简式为______。
(2)B的化学名称为_________。
(3)由C生成D的化学方程式为____________。
(4)由E生成F的反应类型为___________。
(5)F的分子式为____________。
(6)R是D的同分异构体,则同时符合下列条件的R共有___种。①只含1个甲基②苯环上有2个取代基③能与FeCl3溶液发生显色反应,其中核磁共振氢谱为6组峰,且峰面积之比为1:2:2:3:1:2的结构简式为________、_________。(任写2种)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不能达到实验目的的是( )
序号 | 实验操作 | 实验目的 |
A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
B | MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝的金属性强弱 |
C | 测定等物质的量浓度的H2CO3、H2SO4溶液的pH | 比较碳、硫的非金属性强弱 |
D | Fe、Cu分别放入相同浓度的盐酸中 | 比较铁、铜的金属性强弱 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组用如图装置模拟电镀铜和精炼铜。下列说法不正确的是

A.电镀铜和精炼铜时,Y上的电极反应都是:Cu2++2e-=Cu
B.电镀铜时,Y 电极为待镀的金属制品
C.精炼铜时,X 电极是粗铜,比铜活泼的金属最终变成阳极泥
D.电镀铜时,X 电极是铜,溶液中的Cu2+浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为原电池装置示意图:
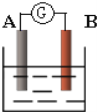
(1)若A为Zn,B为石墨棒,电解质溶液为稀硫酸,则A为________极(填正或负),写出电极反应式:正极_______________________,负极________________________.总反应为:____________________。
(2)若A为铜片,B为铁片,电解质为FeCl3溶液,则A为________极(填正或负),写出电极反应式:正极_____________________________,负极________________________.总反应为:_______________________________。
(3)若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入H2和O2,该电池即为燃料电池,通入氧气的一极为该电池的________极(填正或负),该电池的总反应为:____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:
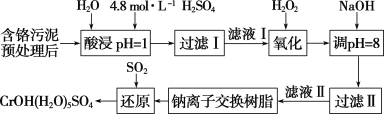
已知:酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+等。
(1)配制500mL4.8mol/L的稀硫酸溶液,需要的玻璃仪器除烧杯、玻璃棒外,还需要______。
(2)酸浸时,为了提高浸取率可采取的措施有________、________。(答出两点)
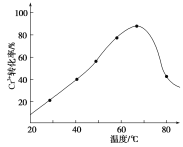
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O![]() ,则此反应中氧化剂和还原剂的物质的量之比为________。控制其他条件不变,反应温度对Cr3+转化率的影响如图所示。请分析温度超过70 ℃时,Cr3+转化率下降的原因是__________。
,则此反应中氧化剂和还原剂的物质的量之比为________。控制其他条件不变,反应温度对Cr3+转化率的影响如图所示。请分析温度超过70 ℃时,Cr3+转化率下降的原因是__________。
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | — | — |
沉淀完全时的pH | 3.7 | 5.4(>8溶解) | 9(>9溶解) |
①用NaOH调节溶液的pH不能超过8,其理由是_________。
②当pH=8时,Mg2+是否开始沉淀(溶液中镁离子浓度约为1 mol·L-1)________(填 “是”或“否”)。已知Ksp[Mg(OH)2]=1.8×10-11。
(5)上述流程中,加入NaOH溶液后,溶液呈碱性,Cr2O72-转化为CrO42-,写出上述流程中用SO2进行还原反应生成CrOH(H2O)5SO4沉淀的离子方程式 _________。
(6)Cr(OH)3和Al(OH)3类似,也是两性氢氧化物,写出向CrCl3溶液中逐滴加NaOH溶液至过量的离子方程式_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com