
【题目】写出[Ag(NH3)2]OH的中心离子的核外电子排布式________、配位体的电子式________、配位体的杂化方式是________写出[Ag(NH3)2]OH电离的离子方程式________。
科目:高中化学 来源: 题型:
【题目】为除去 括号内的杂质,所选用的试剂或方法不正确的是
A.Na2CO3溶液(NaHCO3),选用适量NaOH溶液
B.NaHCO3溶液(Na2CO3),通入过量的CO2气体
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.CO2气体(CO),通入O2点燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A和a是生活中常见的两种有机物,可用于制备安眠药苯巴比妥Q,合成过程如下:
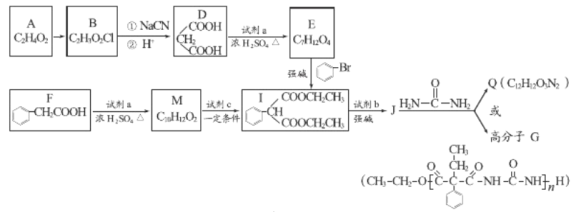
已知: 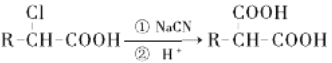
(1)A的官能团名称为_________。
(2)A→B的反应类型为_________。
(3)D→E的反应方程式为_________________________。
(4)写出F符合下列条件的同分异构体的结构简式_________。
①遇Fe3+溶液显紫色 ②发生银镜反应 ③苯环上的一溴代物有两种
(5)J与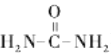 在催化剂作用下既可以生成Q,又可以生成G,写出生成G的化学方程式 _________________________________。
在催化剂作用下既可以生成Q,又可以生成G,写出生成G的化学方程式 _________________________________。
(6)下列说法正确的是 _________。
a.E与M互为同系物
b.B水解酸化后的产物可以发生加聚反应
c.用试剂b制备乙烯的条件是NaOH的醇溶液、加热
d.Q的结构简式是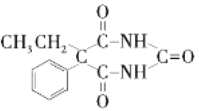
(7)试剂c为酯类,核磁共振氢谱有两组吸收峰,与M反应生成I和a,此反应为取代,则试剂c的结构简式为 _________。
(8)写出以CH2=CH-CH=CH2和E为主要原料制备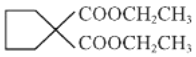 的流程_____________________________________________________________。
的流程_____________________________________________________________。
(无机试剂自选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全沉淀相同体积的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗相同浓度的AgNO3溶液的体积之比为3:2:1,则NaCl、MgCl2、AlCl3溶液的物质的量浓度之比为( )
A. 1:2:3 B. 3:2:1 C. 6:3:2 D. 9:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是
A. K值不变,平衡可能移动 B. K值变化,平衡一定移动
C. 平衡移动,K值可能不变 D. 平衡移动,K值一定变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质鉴别所用试剂不正确的是( )
A.乙醇与乙酸用CaCO3固体B.乙醇和乙醛用酸性高锰酸钾溶液
C.苯和乙酸用水D.乙烯与乙烷用酸性高锰酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【山西省实验中学2017届下学期模拟热身】[化学―选修3:物质结构与性质]
研究物质的微观结构,有助于人们理解物质变化的本质。请根据已学习的物质结构知识,回答下列问题:
(1)基态Mn原子的价电子排布式为___,气态Mn2+再失去l个电子比Fe2+再失去1个电子更难,其原因是________。
(2)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有_____。写出难溶物溶于氨水时的离子方程式__________。实验过程中加入C2H5OH 后可观察到析出深蓝色Cu(NH3)4SO4·5H2O晶体。实验中所加C2H5OH 的作用是______。
(3)HClO2、HClO3为氯元素的含氧酸,试推测ClO2-的空间结构:________;HClO3分子中,Cl原子的杂化方式为______;两种酸酸性较强的是_______.
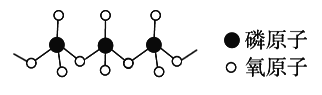
(4)多磷酸盐的酸根阴离子是由两个或两个以上磷氧四面体通过共用角顶氧原子而连接起来的,部分结构如图所示,多磷酸根离子的通式为______。(磷原子数目用n表示)
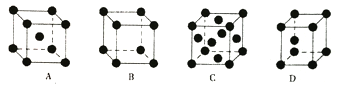
(5)金属Pt采用“…ABCABC…”型堆积方式,抽出一个晶胞,其正确的是________。
已知金属Pt的密度为21.4 g/cm3,则Pt原子半径的计算式为______pm (只列式,不必计算结果,Pt的相对原子质量为M,阿伏加德罗常数为6.02×1023mol-1)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com