
| A. | 利用金属钠或者金属钾 | B. | 利用质谱法 | ||
| C. | 利用红外光谱法 | D. | 利用核磁共振氢谱 |
分析 二甲醚和乙醇中分别含有醚键和-OH,二者性质不同,-OH可与Na反应,二者含有的H原子的种类和性质不同,以此解答该题.
解答 解:A.乙醇中含有-OH,可与金属钠或金属钾反应生成氢气,可鉴别,故A正确;
B.利用质谱法,因二者的相对分子质量相等,则不能鉴别,故B错误;
C.二甲醚和乙醇中分别含有醚键和-OH,官能团不同,可用红外光谱法鉴别,故C正确;
D.二者含有的H原子的种类和性质不同,可用核磁共振氢谱鉴别,故D正确.
故选B.
点评 本题考查有机物的鉴别,为高频考点,把握物质的性质、性质差异、结构等为解答的关键,侧重分析与应用能力的考查,注意有机物结构的确定方法及应用,题目难度不大.


科目:高中化学 来源: 题型:填空题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
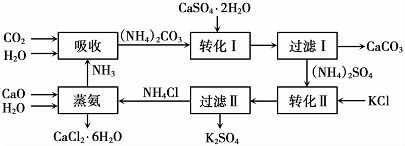
| 温度(℃) | 0 | 20 | 60 |
| K2SO4溶解得量(g) | 7.4 | 11.1 | 18.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 装置 | 操作 | 现象 |
 | 添加试剂,检查装置气密性,点燃酒精灯 | i.C中气体颜色变浅 ii.稍后,C中出现白烟并逐渐增多 |

 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
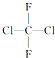 下列有关叙述正确的是( )
下列有关叙述正确的是( )| A. | 它有两种同分异构体 | B. | 它是平面分子 | ||
| C. | 它只有一种结构 | D. | 它有4种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯和浓溴水用铁做催化剂制溴苯 | |
| B. | 将苯与浓硝酸和浓硫酸的混合酸共热至50℃~60℃制硝基苯 | |
| C. | 甲烷与氯气光照制得纯净的一氯甲烷 | |
| D. | 乙烯通入溴的四氯化碳溶液得到1,2-二溴乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
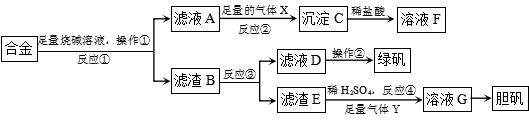
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com