
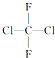 下列有关叙述正确的是( )
下列有关叙述正确的是( )| A. | 它有两种同分异构体 | B. | 它是平面分子 | ||
| C. | 它只有一种结构 | D. | 它有4种同分异构体 |
分析 运用知识迁移的方法,与CH4的分子构型对比回答,该化合物是甲烷的取代产物,甲烷是正四面体型结构,氟利昂-12为四面体结构,F、Cl原子在空间都彼此相邻,它只有一种结构.
解答 解:A.由甲烷的结构可知,四个氢原子的空间位置只有一种,则氟利昂-12只有一种结构,故A错误;
B.甲烷是正四面体型结构,则氟利昂-12为四面体结构,故B错误;
C.从结构式可知,该化合物是甲烷的取代产物,由于甲烷是正四面体型结构,所以该化合物也是四面体,因此结构只有一种,没有同分异构体,故C正确;
D.由甲烷的结构可知,四个氢原子的空间位置只有一种,则氟利昂-12只有一种结构,故D错误;
故选C.
点评 本题以甲烷的正四面体型结构为载体,考查学生对知识的迁移和空间想象能力.烃的空间结构必须掌握甲烷正四面体型,乙烯、苯为平面型分子,乙炔为直线型分子,题目难度不大.


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:解答题
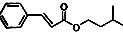 )是一种香料,一种合成路线如下:
)是一种香料,一种合成路线如下: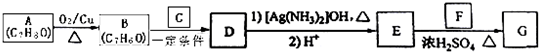
 ;
;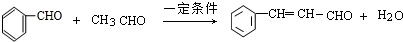 .
.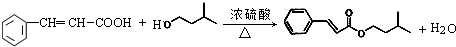 ,反应类型为酯化反应或取代反应.
,反应类型为酯化反应或取代反应.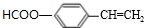 、
、 (写结构简式)
(写结构简式)查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 二氯化二硫(S2Cl2)是基本有机化工的直接原料,实验室可采用干燥的氯气在110℃-140℃与硫反应,即可得S2Cl2粗品.
二氯化二硫(S2Cl2)是基本有机化工的直接原料,实验室可采用干燥的氯气在110℃-140℃与硫反应,即可得S2Cl2粗品.| 物质 | S | SCl2 | S2Cl2 |
| 熔点/℃ | 112.8 | -78 | -77 |
| 沸点/℃ | 444.6 | 59.6 | 137 |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
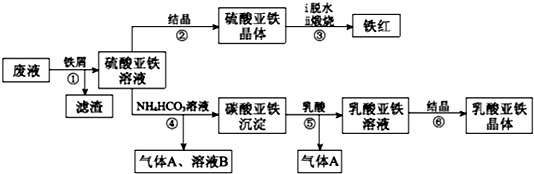
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用金属钠或者金属钾 | B. | 利用质谱法 | ||
| C. | 利用红外光谱法 | D. | 利用核磁共振氢谱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体熔点由高到低:CI4>CBr4>CCl4>CF4 | |
| B. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| C. | 熔点由高到低:Na>Mg>Al | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标况下,22.4LSO3含有σ键数目为3NA | |
| B. | 已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,则某容器内加入0.5 NA个N2(g)与足量的H2(g),充分反应后放出的热量为46 kJ | |
| C. | 标准状况下,22.4L氦气含有的原子数为2NA | |
| D. | 0.1mol HCN分子中含有的π键数目为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com