
【题目】将200mLH2SO4和Fe2(SO4)3的混合溶液分成两等份,向其中一份中加入足量铁粉,充 分反应后测得固体质量减少3.36g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干燥、称量,得到23.3g白色沉淀。请计算:
(1)原溶液中c(SO42﹣)=_____。
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量之比为_____。
【答案】1.00mol/L 2:1
【解析】
23.3g沉淀为硫酸钡,发生反应为SO42-+Ba2+=BaSO4↓,根据n=![]() 、c=
、c=![]() 可计算出原溶液中硫酸根离子浓度;
可计算出原溶液中硫酸根离子浓度;
(2)设出H2SO4和Fe2(SO4)3的物质的量,固体减少的3.36g为Fe,发生反应为2Fe3++Fe=3Fe2+、Fe+2H+=Fe2++H2↑,结合(1)中硫酸根离子的物质的量列式计算即可。
(1)每份溶液的体积100mL,生成23.3g沉淀为BaSO4,其物质的量为:n(BaSO4)=![]() =0.1mool,原溶液中n(SO42﹣)=n(BaSO4)=0.1mol,则c(SO42﹣)=
=0.1mool,原溶液中n(SO42﹣)=n(BaSO4)=0.1mol,则c(SO42﹣)=![]() =1.00mol/L;
=1.00mol/L;
(2)固体质量减少的3.36g为Fe,其物质的量为:![]() =0.06mol,设H2SO4和Fe2(SO4)3 的物质的量分别为x、y,根据反应2Fe3++Fe=3Fe2+、Fe+2H+=Fe2++H2↑可知:①x+y=0.06mol,根据硫酸根离子守恒可知:②x+3y=0.1mol,联立①②解得:x=0.04mol、y=0.02mol,溶液具有均一性,则原溶液中H2SO4和Fe2(SO4)3的物质的量之比=0.04mol:0.02mol=2:1。
=0.06mol,设H2SO4和Fe2(SO4)3 的物质的量分别为x、y,根据反应2Fe3++Fe=3Fe2+、Fe+2H+=Fe2++H2↑可知:①x+y=0.06mol,根据硫酸根离子守恒可知:②x+3y=0.1mol,联立①②解得:x=0.04mol、y=0.02mol,溶液具有均一性,则原溶液中H2SO4和Fe2(SO4)3的物质的量之比=0.04mol:0.02mol=2:1。


科目:高中化学 来源: 题型:
【题目】若用AG表示溶液的酸度,AG的定义为AG=lg![]() 。室温下实验室中用0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定过程如图所示,下列叙述正确的是
。室温下实验室中用0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定过程如图所示,下列叙述正确的是
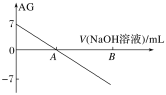
A.室温下,醋酸的电离常数约为10-5
B.A点时加入氢氧化钠溶液的体积为20.00 mL
C.若B点为40 mL,所得溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)
D.从A到B,水的电离程度逐渐变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的三个容积相同的容器①②③中进行如下反应:3A(g)+B(g) ![]() 2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )
2C(g) ΔH<0,若起始温度相同,分别向三个容器中通入3 mol A和1 mol B,则达到平衡时各容器中C物质的体积分数由大到小的顺序为( )
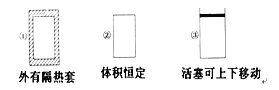
A. ③②①B. ③①②C. ①②③D. ②①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。
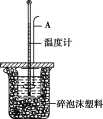
(1)理论上强酸强碱的稀溶液反应生成1 mol水时放出57.3 kJ的热量,写出表示稀硫酸和氢氧化钠稀溶液反应的中和热的热化学方程式: ____________________。
(2)仪器A的名称是 _____________;在实验过程中,如果不把温度计上的酸用水冲洗干净就直接测量NaOH溶液的温度,则测得的ΔH_____________ (填“偏大”“偏小”或“无影响”)。
(3)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白: ___________
实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3中和后生成溶液的比热容c=4.18 J/(g·℃)则中和热ΔH= _____________(取小数点后一位)
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是_____________ (填序号)。
a.实验装置保温隔热效果差
b.用量筒量取NaOH溶液的体积时仰视读数
c.分多次把NaO溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用系统命名法给下列有机物命名:
①![]() __;
__;
②(CH3)3COH__;
(2)相对分子质量为114,其一氯代物只有一种的链烃的结构简式__,该物质的名称为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴酸银(AgBrO3)溶解度随温度变化曲线如图所示。下列说法正确的是
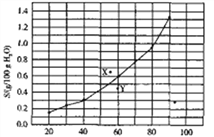
A. 溴酸银的溶解是一个熵增、焓减过程
B. 对应温度下,X点的分散系中,V(溶解)>v(沉淀)
C. Y点的分散系中,c(Ag+)·c(BrO3-)>6.25×10-4
D. 60 ℃时溴酸银饱和溶液中c(BrO3-)=0.025mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 A、B、C、D 的原子序数依次增大,B 和 D 同主族,A 和 C 同主族;X、Y、N 分别是由以上四种元素中两种组成的化合物,Z 是由以上三种元素组成的化合物;若 X 与 Y 的摩尔质量相同, Y 为淡黄色固体,N 常温下是液体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
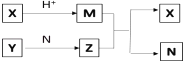
A.相对分子质量M>N,沸点 M>NB.原子半径:D>B>C>A
C.Z 为 NaOHD.M 中含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】久置的FeSO4溶液变黄,一般认为是二价铁被氧化为三价铁的缘故。某硏究小组为硏究溶液中Fe2+被O2氧化的过程,查阅资料发现:溶液中Fe2+的氧化过程分为先后两步,首先是Fe2+水解,接着水解产物被O2氧化。于是小组同学决定研究常温下不同pH对Fe2+被O2氧化的影响,并测定了Fe2+氧化率随时间变化的关系,结果如图。
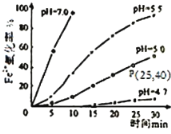
回答下列问题:
(1)写出Fe2+水解的离子方程式___;要抑制FeSO4水解,可以采取的措施是___。
(2)若配制的FeSO4溶液浓度为0.01mol/L,反应过程中溶液体积不变,计算图中P点Fe2+的氧化速率___。
(3)在酸性条件下,Fe2+被O2氧化的反应方程式为:4Fe2++O2+4H+![]() 4Fe3++2H2O,已知常温下该反应的平衡常数很大。则下列说法正确的是___。
4Fe3++2H2O,已知常温下该反应的平衡常数很大。则下列说法正确的是___。
a.Fe2+转化为Fe3+的趋势很大
b.Fe2+转化为Fe3+的速率很大
c.该反应进行得很完全
d.酸性条件下Fe2+不会被氧化
(4)结合图分析不同pH对Fe2+被O2氧化的反应产生了怎样的影响___。
(5)用K2Cr2O7标准溶液測定溶液中Fe2+浓度,从而计算Fe2+的氧化率。反应如下:6Fe2++Cr2O72-+14H+→2Cr3++6Fe3++7H2O,若取20mL待测溶液,用0.0200mol·L1K2Cr2O7标准溶液滴定,消耗标准溶液16.50mL,则溶液中c(Fe2+)=___mol·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.4g某有机物M置于密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气。将燃烧产物依次通过浓硫酸、碱石灰和灼热的氧化铜(试剂均足量,且充分反应),测得浓硫酸增重1.44g,碱石灰增重1.76g,氧化铜减轻0.64g。下列说法中不正确的是
A. M的实验式为CH2O
B. 若要得到M的分子式,还需要测得M的相对分子质量或物质的量
C. 若M的相对分子质量为60,则M一定为乙酸
D. 通过红外光谱仪可分析M中的官能团
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com