
| A、NaHSO4═Na++H++SO42- |
| B、NaHCO3═Na++H++CO32- |
| C、MgCl2═Mg2++Cl- |
| D、Ba(OH)2═Ba2++2OH- |


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| 试管 | 盐酸浓度 | 温度 | 铁的状态 |
| A | 0.5mol/L | 20℃ | 块状 |
| B | 0.5mol/L | 20℃ | 粉末状 |
| C | 1mol/L | 35℃ | 块状 |
| D | 2mol/L | 35℃ | 粉末状 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
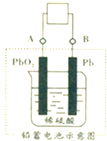 电瓶车所用的电池一般是铅蓄电池,如图是一种典型的可充电电池,电池总反应式为:
电瓶车所用的电池一般是铅蓄电池,如图是一种典型的可充电电池,电池总反应式为:| 放电 |
| 充电 |
| A、放电时电极 PbO2 发生氧化反应 |
| B、放电时电子流向由A到B |
| C、工作时蓄电池里电解质溶液的pH不变 |
| D、放电时正极反应是PbO2+2e-+4H++SO42-═PbSO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol甲烷含有的电子数为NA |
| B、1 L 0.1 mol/L Na2CO3溶液中含有的CO3数目为0.1 NA |
| C、1 L pH=1的硫酸溶液中含有的H+数为0.2 NA |
| D、标准状况下,2.24 L CO和CO2混合气体中含有的氧原子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、燃烧热指的是可燃物完全燃烧生成稳定的氧化物所放出的热量 |
| B、勒夏特列原理指的是,如果改变影响平衡的条件之一(如温度、压强,以及参加反应的化学物质的浓度),平衡将向着能够减弱这种改变的方向移动 |
| C、盐溶液不一定显中性,不显中性的盐都会促进水的电离 |
| D、电镀是利用原电池原理在某些金属表面镀上一薄层其他金属或合金的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热才能发生的反应一定是吸热反应 |
| B、强电解质溶液的导电能力一定比弱电解质溶液的强 |
| C、SO3溶于水,其水溶液能导电,故SO3是电解质 |
| D、升高温度,可提高活化分子百分数,使有效碰撞几率提高,化学反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁和稀硝酸反应制得浅绿色溶液:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| B、向Ca(ClO)2溶液中通入过量CO2制取次氯酸:2ClO-+H2O+CO2=2HClO+CO32- |
| C、向酸性KMnO4溶液中通入SO2:2MnO4-+5SO2+4OH-=2Mn2++5SO42-+2H2O |
| D、0.01 mol?L-1NH4Al(SO4)2溶液与0.02 mol?L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com