
����Ŀ��A��B��C��D��E��Ԫ�����ڱ���ǰ�����������ֳ���Ԫ�أ��������Ϣ�����
Ԫ�� | �����Ϣ |
A | ԭ�Ӻ���L���������K���2�� |
B | ��һ�ֵ��ʱ���Ϊ��������ġ�����ɡ�� |
C | Ԫ�صĵ�һ�������ǵ�3��������Ԫ������С�� |
D | ��̬ԭ�����������Ų�Ϊ��n+1��sn��n+1��p��n+2�� |
E | ���γɶ������������һ��Ϊ���д��Եĺ�ɫ���� |
��ش��������⣺
��1��C��Ԫ�����ڱ���λ�ڵ����ڡ����壻D�Ļ�̬ԭ�Ӻ�������Ų�ʽ�� ��
��2��B��C��D�ļ����Ӱ뾶�ɴ�С��˳��Ϊ���û�ѧ���ű�ʾ����ͬ�� �� B��D�ļ��⻯�����ȶ��Խϴ���� ��
��3��B�ij������ʺ�C�ĵ��ʰ����ʵ�����1��2��Ӧ���ɵĻ������л�ѧ��������Ϊ���û������������壮
��4��E�γɵĺ�ɫ���Ծ��巢�����ȷ�Ӧ�Ļ�ѧ����ʽ�� ��
��5����֪��2AB��g��+B2��g���T2AB2��g����H=��566.0kJmol��1
D��s��+B2��g���TDB2��g����H=��296.0kJmol��1
������AB��DB2�̵�����Ⱦ��һ�ַ����ǽ����ڴ���������ת��Ϊ��̬����D����д���˷�Ӧ���Ȼ�ѧ����ʽ�� ��
���𰸡�
��1������IA��1s22s22p63s23p4
��2��S2����O2����Na+��H2O
��3�����Ӽ������ۼ�������
��4��3Fe3O4+8Al ![]() 9Fe+4Al2O3
9Fe+4Al2O3
��5��2CO��g��+SO2��g��=S��s��+2CO2��g����H=��270kJ?mol��1
���������⣺AԪ��ԭ�Ӻ���L���������K���2������L����4�����ӣ���AΪ̼Ԫ�أ�BԪ�ص�һ�ֵ��ʱ���Ϊ��������ġ�����ɡ������BΪ��Ԫ�أ�CԪ�صĵ�һ�������ǵ�3��������Ԫ������С�ģ���CΪNaԪ�أ�DԪ�ػ�̬ԭ�����������Ų�Ϊ��n+1��sn��n+1��p��n+2�� �� ����n=2����DΪSԪ�أ�EԪ�ؿ��γɶ������������һ��Ϊ���д��Եĺ�ɫ���壬��EΪFeԪ�أ�
��1.��CΪNaԪ�أ��������ڱ��е�������IA�壬DΪ��Ԫ�أ���̬ԭ�Ӻ�������Ų�ʽ��1s22s22p63s23p4 �� ���Դ��ǣ�����IA��1s22s22p63s23p4��
��2.��B��C��D�ļ����ӷֱ�ΪO2����Na+��S2�� �� ���Ӳ��Ų���ͬ���˵����Խ�����Ӱ뾶ԽС��������������ͬ�����Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶�ɴ�С��˳��Ϊ��S2����O2����Na+ �� ���ڷǽ�����O��S������̬�⻯�����ȶ���H2O��H2S�����Դ��ǣ�S2����O2����Na+��H2O��
��3.��B��C�ĵ��ʰ����ʵ�����1��2�γɵĻ�����ΪNa2O2 �� �������Ӽ������ۼ����������Ӿ��壬���Դ��ǣ����Ӽ������ۼ������ӣ�
��4.��E�ĺ�ɫ���Ծ���ΪFe3O4 �� �������ȷ�Ӧ�Ļ�ѧ����ʽ�ǣ�3Fe3O4+8Al ![]() 9Fe+4Al2O3 �� ���Դ��ǣ�3Fe3O4+8Al
9Fe+4Al2O3 �� ���Դ��ǣ�3Fe3O4+8Al ![]() 9Fe+4Al2O3��
9Fe+4Al2O3��
��5.��������CO��SO2�̵�����Ⱦ��һ�ַ����ǽ����ڴ���������ת��Ϊ����S����֪���١�2CO��g��+O2��g��=2CO2��g����H=��566.0kJmol��1 �� �ڡ�S��s��+O2��g��=SO2��g����H=��296.0kJmol��1 �� �ɸ�˹���ɣ��٩��ڵ�2CO��g��+SO2��g��=S��s��+2CO2��g����H=����566.0kJmol��1��������296.0kJmol��1��=��270kJmol��1 �� ���Դ��ǣ�2CO��g��+SO2��g��=S��s��+2CO2��g����H=��270kJmol��1 ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��Q��W��R���ֶ�����Ԫ��ԭ��������������������׳ƿ����ƣ���X��Z��Q����Ԫ����ɡ�ҽѧ�г���QR��Һ����������ˮ������������X��R����Ԫ����ɡ���ش��������⣺
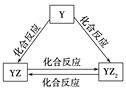
(1)Q�����ӽṹʾ��ͼΪ__��
(2)YԪ�صĵ��ʼ��仯�����ܷ�������ͼ��ʾ��ת������YԪ��Ϊ___(��Ԫ�ط���)���ڼ���Һ��ͨ������YZ2���壬д���÷�Ӧ�����ӷ���ʽ��______��
(3)W�ĵ��ʼ��������Һ��Ӧ������������Һ��Ӧ��
�ٳ����£���W�ĵ��ʺͼ���Һ��ϣ�������Ӧ�����ӷ���ʽΪ_______��
��Q��W����Ԫ�ؽ����Ե�ǿ��ΪQ____W(�<����>��)�����б�������֤����һ��ʵ����____(�����)��
a��Q���ʵ��۵��W���ʵĵ�
b��W��ԭ��������
c��Q������������ˮ����ļ��Ա�W������������ˮ����ļ���ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һһ�������Ե��ǣ�������
A.���н϶�H+����Һ
B.pH��7����Һ
C.c��OH������c��H+������Һ
D.�μӷ�̪����ɫ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A�ǻҺ�ɫ���н�������Ĺ��嵥�ʡ�������ͼ��ʾ������֮���ת����ϵ���ش������й����⡣
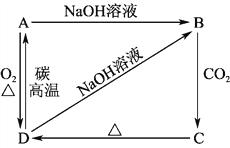
��1��д��A��B��C��D�Ļ�ѧʽ��A________��B________��C________��D________��
��2��д��D��A�Ļ�ѧ����ʽ��__________________________________________��
��3��д�����з�Ӧ�����ӷ���ʽ��
B��C��____________________________________��
D��B��____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������֤�����������������ʵ�ǣ� ��
A.���ԺͼӦB.���������Ư����
C.������ȶ��������ֽ�D.������ƿ��Ժ�̼�ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС��õ�һ�����̿���Ʒ������Ҫ�ɷ�Ϊ��������(MnO2)��ʯӢ(SiO2)��Ϊ����ȡ��������������������ʵ�飬��װ����ͼ��ʾ����ش��������⣺
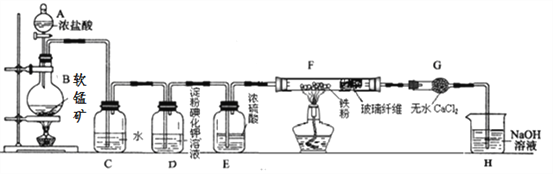
��1��ȡ�������̿�������ƿ�У���������Ũ���Ტ���ȣ���ƿ�з����Ļ�ѧ��ӦΪ��MnO2 ��4HCl(Ũ)![]() MnCl2��Cl2����2H2O����ַ�Ӧ����ƿ�в����Ĺ�����____________������4molŨ������뷴Ӧ�������������ڱ�״���µ����Ϊ____22.4L (��������������С��������������)��Ũ�����ڸ÷�Ӧ�б��ֳ���������_______________________��
MnCl2��Cl2����2H2O����ַ�Ӧ����ƿ�в����Ĺ�����____________������4molŨ������뷴Ӧ�������������ڱ�״���µ����Ϊ____22.4L (��������������С��������������)��Ũ�����ڸ÷�Ӧ�б��ֳ���������_______________________��
��2�������������ɫ��������C�У��۲쵽�������� ______ ��ԭ���� ______________ ���û�ѧ����ʽ�����ֻش���
��3��ʵ���й۲쵽D��Һ����ɫ��д��Dװ���з�����Ӧ�����ӷ���ʽ ____________ ��
��4��Ϊ̽��������Fe��Ӧ�IJ���������ͨ�����Ĺ�ϵ�����ʵ�飬����¼�������£�
ʵ�鷽�� | ʵ������ | ʵ����� |
1.ȡ��Ӧ��ʼ��(����������)F�в���ô�����ȥ������Fe��ʣ���������ˮ�У�ȡ�ϲ���Һװ����ֻ�Թ��У��ټ���KSCN��Һ���ڼ���KMnO4��Һ | ��KSCN��Һ�Ժ�ɫ ��KMnO4��Һ����ɫ | ����� |
2.ȡ��ַ�Ӧ��(����ͨ���㹻��ʱ��)F�в������ˮ�У�����KMnO4��Һ | KMnO4��Һ����ɫ |
����ʵ�����ó�ʵ����ۣ�д��������Fe�۹���ʱ������Ӧ�Ļ�ѧ����ʽ______��
��5����֪F�еIJ����׳��⣬��F��Hװ��֮�䰲װGװ�ã�Ŀ����_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH��ֽ��������Һ��pHʱ�������Ƚ�pH��ֽ������ˮ��ʪ�����������ᣨ������
A.ƫ��
B.ƫС
C.����
D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��һ����Ҫ�ķ�Ӧ��
��1����֪��Ӧ2I-��2Fe3+=I2��2Fe2+����Ӧ�л�ԭ����_________��������Fe3+______I2 (� �� ���� �� ��) ��
��2����2Na2O2+2CO2��2Na2CO3+O2��Ӧ�У���ת��3mol���ӣ����������������ڱ�״���µ����Ϊ___________L��
��3����xR2++yH++O2�TmR3++nH2O�����ӷ���ʽ�У���ϵ��m��R2+��R3+�ж���ȷ����__��
A��m=y��R3+�ǻ�ԭ�� B��m=2y��R2+������
C��m=2��R3+�������� D��m=4��R2+�ǻ�ԭ��
��4����˫���ű����Ӧ2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O�е���ת�Ƶķ������Ŀ_________��
��5��������ʯӢɰ��̼�۹��ȿɷ�����Ӧ��SiO2��2C��2Cl2![]() SiCl4��2CO����Ӧ����6g̼ʱ�����ɻ�ԭ����_________mol��
SiCl4��2CO����Ӧ����6g̼ʱ�����ɻ�ԭ����_________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ɫ������ֲ����������������ϳ���Ҫ��ǰ�����ʣ��ձ�����ڸߵ�ֲ���У�������ɫ����Ϊ��ɫ����ɫ�ᾧ������ˮ������������������ƣ���ṹ��ͼ��ʾ�����й���ɫ�����˵������ȷ���ǣ� �� 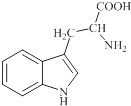
A.ɫ����ķ���ʽΪC11H12N2O2
B.ɫ�����ܷ���ȡ�����ӳɡ��������кͷ�Ӧ
C.ɫ��������ˮ��������������Һ����Ϊ�����ᡢ��ܷ�Ӧ������
D.��ɫ������ʰ��ᣨNH2CH2COOH����ϣ���һ�������������γ����ֶ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com