
【题目】短周期元素X,Y,Z,W,R的化合价与原子序数的关系如图所示.下列说法正确的是( ) 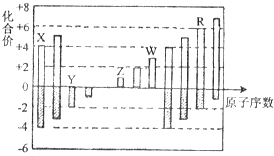
A.原子半径:Z>Y>X
B.气态氢化物的稳定性:Y<R
C.Z和Y形成的化合物是离子化合物
D.常温下单质W能溶于R的最高价氧化物对应水化物的浓溶液
【答案】C
【解析】解:由表中化合价可知,Y的化合价为﹣2价,没有正化合价,故Y为O元素,X的化合价为+4、﹣4价,处于ⅣA族,原子序数比O元素小,故X为C元素,Z的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素,W为+3价,为Al元素,R的化合价为+6、﹣2价,故R为S元素,A、同周期随原子序数增大,原子半径减小,故原子半径Li>C>O,同主族自上而下原子半径增大,故Na>Li,故Na>C>O,即Z>X>Y,故A错误;
B、非金属性O>S,即Y>R,非金属性越强氢化物越稳定,故气态氢化物的稳定性:Y>R,故B错误;
C、Z和Y形成的化合物是氧化钠、过氧化钠,属于离子化合物,故C正确;
D、Al在浓硫酸中发生钝化现象,不能溶解,故D错误;
故选C.
由表中化合价可知,Y的化合价为﹣2价,没有正化合价,故Y为O元素,X的化合价为+4、﹣4价,处于ⅣA族,原子序数比O元素小,故X为C元素,Z的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素,W为+3价,为Al元素,R的化合价为+6、﹣2价,故R为S元素.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】工业上,向500﹣600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁.现用如图所示的装置模拟上述过程进行试验.回答下列问题: 
(1)制取无水氯化铁的实验中,A中反应的化学方程式为 , 装置B中加入的试剂是 .
(2)制取无水氯化亚铁的实验中,装置A用来制取 . 尾气的成分是 . 若仍用D的装置进行尾气处理,存在的问题是、 .
(3)若操作不当,制得的FeCl2 会含有少量FeCl3 , 检验FeCl3常用的试剂是 . 欲制得纯净的FeCl2 , 在实验操作中应先点燃处的酒精灯,目的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人体必须的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程如图1和实验装置如图2: 
(1)指出上述提取碘的过程中有关实验操作的名称:步骤③ , 步骤⑤ .
(2)写出步骤④对应反应的离子方程式:
(3)提取碘的过程中,可供选择的有机试剂是(填编号)
A.醋酸
B.苯
C.四氯化碳
D.酒精
(4)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是 .
(5)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏.指出如图实验装置中存在的错误之处: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应过程中能量变化的说法正确的是( )
A.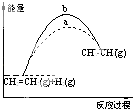 图中a、b曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化
图中a、b曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化
B.己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2 . 则△H1>△H2
C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
D.在一定条件下,某可逆反应的△H=+100kJmol﹣1 , 则该反应正反应活化能比逆反应活化能大100kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( ) 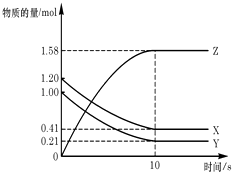
A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g)Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.电负性的大小顺序为Cl>S>P
B.由于NO3﹣和SO3互为等电子体,所以可以推断NO3﹣的空间构型为平面三角形
C.根据晶格能的大小可以判断MgCl2的熔点比CaCl2高
D.液态HF的沸点比液态HCl的沸点高是因为氢氟键的键能比氢氯键的键能大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】15 g A物质和10.5 g B物质恰好完全反应,生成7.2 g C物质,1.8 gD物质和0.3 mol E物质,则E物质的摩尔质量是
A. 16.5 g/mol B. 111 g/mol C. 55 g/mol D. 27.5 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL 0.5mol/L的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示.下列关于混合溶液的相关说法错误的是( ) 
A.醋酸的电离平衡常数:b点>a点
B.由水电离出的c(OH):b点>c点
C.从a点到b点,混合溶液中可能存在:c(CH3COO﹣)=c(Na+)
D.b点到c点,混合溶液中一直存在:c(Na+)>c(CH3COO﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究外界条件对过氧化氢分解速率的影响,某化学兴趣小组的同学做了以下实验。请回答下列问题:
编号 | 实验操作 | 实验现象 |
① | 分别在试管A、B中加入5mL5%H2O2溶液,各滴入2滴1mol/LFeCl3溶液。待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡。 | 试管A中不再产生气泡; 试管B中产生的气泡量增多。 |
② | 另取两支试管分别加入5mL5%H2O2溶液和5mL10%H2O2溶液。 | 两支试管中均未明显见到有气泡产生。 |
(1)实验①的目的是其它条件相同时,探究______条件对H2O2分解速率的影响。
(2)实验②未观察到预期的实验现象,为了帮助该组同学达到实验目的,请你用实验中所提供的几种试剂,对上述操作进行的改进是____________________________________。
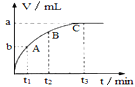
(3)某同学在50mL一定浓度的H2O2溶液中加入适量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图所示,则A、B、C三点所表示的瞬时反应速率最慢的是____(填字母代号)。
(4)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该化学兴趣小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

①定性分析:如图甲可通过观察________________________,定性比较得出结论;该实验中将FeCl3溶液改为Fe2(SO4)3溶液的原因是______________________。
②定量分析:用图乙所示装置做对照试验,实验时均以3min时间为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是________________,所需仪器为_______。
(5)通过对上述实验过程的分析,在实验设计时,要考虑_________思想方法的应用。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com