
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
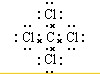 ,C和Cl之间形成的化学键是极性共价键,故答案为:
,C和Cl之间形成的化学键是极性共价键,故答案为: ;极性.
;极性.


科目:高中化学 来源: 题型:
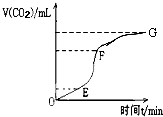 请用相关知识回答下列问题:
请用相关知识回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
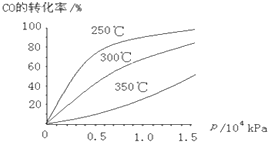 Ⅰ.一定温度下,将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:C02(g)+H2(g)?CO(g)+H2O(g)
Ⅰ.一定温度下,将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:C02(g)+H2(g)?CO(g)+H2O(g)查看答案和解析>>
科目:高中化学 来源: 题型:
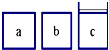 如图所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的SO2和O2使三容器压强相等,一定条件下发生2SO2+O2?2SO3的反应.问:
如图所示,相同体积的a、b、c三密闭容器,其中c容器有一活塞,a、b两容器为定容容器,起始向三容器中都加入相同量的SO2和O2使三容器压强相等,一定条件下发生2SO2+O2?2SO3的反应.问:查看答案和解析>>
科目:高中化学 来源: 题型:
| 一定条件 |
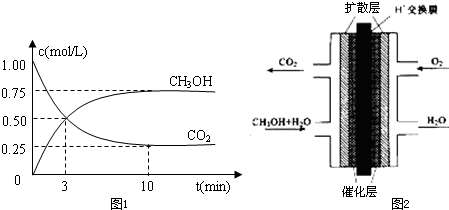
| n(CH3OH) |
| n(CO2) |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,33.6L CO2中含有氧原子数为3NA |
| B、1 mol OH-和1 mol-OH(羟基)所含质子数均为9NA |
| C、常温下,100mL 0.1mol?L-1醋酸钠溶液中含醋酸根的数目小于0.01NA |
| D、50mL 18.4mol?L-1浓硫酸与足量铜加热反应,生成SO2分子数为0.46NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、60克SiO2含有2NA个Si-O共价键 |
| B、1.0L 1.0mo1/L的NaAlO2水溶液中含有的氧原子数为2NA |
| C、8.2g Na218O2与足量的CO2和H2O(g)的混合气体充分反应后转移电子数为0.1NA |
| D、NA个Fe(OH)3胶体粒子的质量为107g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com