
| A. | 1L 0.1mol•L-1 NaAlO2溶液中AlO2-数为0.1NA | |
| B. | 4.48L N2与CO的混合物中所含分子数为0.2NA | |
| C. | 1.2g金刚石所含共价键数为0.2NA | |
| D. | 12.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
分析 A、偏铝酸根为弱酸根,在溶液中会水解;
B、气体所处的状态不明确;
C、求出金刚石的物质的量,然后根据1mol金刚石中含2mol共价键来分析;
D、铜只能和浓硫酸反应,和稀硫酸不反应.
解答 解:A、偏铝酸根为弱酸根,在溶液中会水解,故溶液中的偏铝酸根的个数小于0.1NA个,故A错误;
B、气体所处的状态不明确,故混合气体的物质的量无法计算,则含有的分子个数无法计算,故B错误;
C、1.2g金刚石的物质的量为0.1mol,而1mol金刚石中含2mol共价键,故0.1mol金刚石中含0.2NA条共价键,故C正确;
D、铜只能和浓硫酸反应,和稀硫酸不反应,故当浓硫酸变稀后反应即停止,即浓硫酸不能反应完全,则转移的电子数小于0.2NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 四种主族元素的性质或结构信息如下:
四种主族元素的性质或结构信息如下:| 元素编号 | 相关信息 |
| X | 地壳中含量最大的金属元素;元素最高价为+3价. |
| Y | 原子最外层电子数是电子层数的2倍,最外层电子数是X最外层电子数的2倍. |
| Z | 同周期主族元素中原子半径最小,常温下单质呈液态. |
| M | 能从海水中提取的金属元素,单质可在氮气或二氧化碳中燃烧. |
 ;上述元素最高价氧化物对应的水化物碱性最强的是(写分子式)Mg(OH)2(元素用元素符号表示,下同!).
;上述元素最高价氧化物对应的水化物碱性最强的是(写分子式)Mg(OH)2(元素用元素符号表示,下同!).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 25 | 200 | 300 | 400 | 500 |
| K | 5×108 | 1.0 | 0.86 | 0.507 | 0.152 |
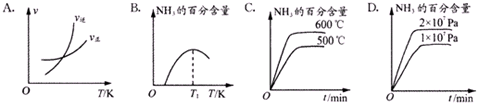
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑥ | B. | ③④⑤ | C. | ①②④⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③⑤⑨ | C. | ④⑤⑥⑦ | D. | ②③⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “钴酞菁”的分子(直径为1.3×10-9m)在水中形成的分散系能产生丁达尔效应 | |
| B. | 氢氟酸可用细口玻璃试剂瓶保存 | |
| C. | 粘附有硫单质的试管可用酒精洗涤 | |
| D. | “地沟油”分馏可制得矿物柴油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,20gH218O中含有中子数目为12NA | |
| B. | 标准状况下,11.2LC2H6中含有极性键的数目为3.5NA | |
| C. | 1LpH=3的CH3COOH溶液中,含有H+的数目大于10-3NA | |
| D. | 1L1mol•L-1稀硝酸(还原产物为NO)与铁完全反应,转移电子数目为0.75NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76.8 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com