
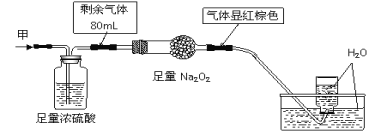
【题目】无色的混合气体甲中可能含有NO、CO2、NO2、NH3、N2中的几种,将100mL气体甲经过下图实验处理,结果得到酸性溶液,还有少量气体剩余,则气体甲的组成可能为 ( )
A. NH3、NO、CO2 B. NH3、NO2、N2 C. NH3、NO2、CO2 D. NO、CO2、N2
【答案】A
【解析】
二氧化氮是红棕色的气体,浓硫酸可以和氨气反应,二氧化碳可以和过氧化钠反应生成氢氧化钠和氧气,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,氮气不溶于水,将100mL甲气体经过如图实验的处理,结果得到酸性溶液,还有少量气体剩余,无法确定有无氮气。
二氧化氮是红棕色的气体,无色的混合气体甲中一定不存在,硫酸和碱性气体能反应,所以100mL甲气体经过足量的浓硫酸,剩余气体80mL,说明一定有NH3存在且体积为20mL,二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有NO、CO2,排水法收集气体,结果得到酸性溶液,还有少量气体剩余,无法确定有无氮气。
故选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】制取氯化铁粉末,已知氯化铁粉末很容易吸水生成结晶化合物FeCl3+6H2O===FeCl3·6H2O。
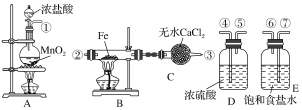
(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):
①接_______________________________________________________
(2)烧瓶A发生的反应中,氧化剂是________(填物质名称),B中反应的化学方程式是___________________。
(3)容器D的作用是_____________________________________________,容器E的作用是__________________________________________________。
(4)A、B中的酒精灯应先点燃________处(填“A”或“B”)的酒精灯,理由是___________________。
(5)这套实验装置是否完整?________(填“是”或“否”),若不完整,还须补充________装置(若第一问填“是”,则此问不需要作答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,它们应用广泛。
(1)N2O是人类最早应用于医疗的麻醉剂之一。它可由NH4NO3在加热条件下分解产生,此反应的化学方程式为______________________________。
(2)N2O4可作火箭高能燃料N2H4的氧化剂。已知:2NO2(g)![]() N2O4(g)△H=﹣akJmol﹣1;N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣bkJmol﹣1;N2(g)+2O2(g)=2NO2(g)△H=+ckJmol﹣1;(a、b、c均大于0)。写出气态肼(N2H4)在气态(N2O4)中燃烧生成氮气和气态水的热化学方程式________。
N2O4(g)△H=﹣akJmol﹣1;N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣bkJmol﹣1;N2(g)+2O2(g)=2NO2(g)△H=+ckJmol﹣1;(a、b、c均大于0)。写出气态肼(N2H4)在气态(N2O4)中燃烧生成氮气和气态水的热化学方程式________。
(3)平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压 × 物质的量分数[例如p(NO2)=p总×x(NO2)]。则反应2NO2(g)N2O4(g)△H=﹣akJmol﹣1平衡常数Kp表达式为______(用p总、和各气体物质的量分数x表示)。
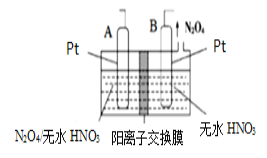
(4)新型绿色硝化剂N2O5可以通过N2O4为原料用电解法制备,实验装置如图所示。则电极B接直流电源的___极,电解池中生成N2O5的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对电负性的理解不正确的是( )
A.电负性是人为规定的一个相对数值,不是绝对标准
B.元素电负性的大小反映了元素原子对键合电子吸引力的大小
C.元素的电负性越大,则元素的非金属性越强
D.元素的电负性是元素固有的性质,与原子结构无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯碱是生活中常用的去油污洗涤剂。某同学欲用碳酸钠晶体(Na2CO310H2O)配制100mL1molL-1的纯碱溶液。请回答下列问题:
(1)计算所需要Na2CO310H2O的质量为________g;
(2)取该溶液20mL稀释到100mL后的溶液中c(Na+)为_______molL-1。
(3)完成上述实验,除下图所示的仪器外,还需要添加的玻璃仪器是__________________________。
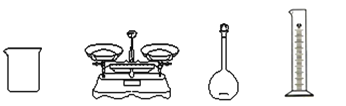
(4)配制溶液时,下列实验操作会使配制溶液浓度偏低的是__________。
A.容量瓶内有水,未经过干燥处理
B.定容操作时,俯视刻度线
C.向容量瓶中转移时有少量液体溅出
D.定容后倒转容量瓶几次,发现液面最低点低于刻度线,再补加几滴水到刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业中,常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。某同学为了从腐蚀废液中回收铜,并重新获得FeCl3溶液,设计如下流程图
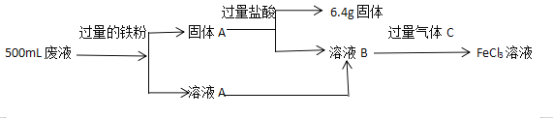
请回答下列问题:
(1)FeCl3溶液腐蚀铜箔反应的离子方程式为___________。
(2)固体A的成分是_______,气体C的化学式为____________。
(3)设计实验方案证明FeCl3溶液中的金属阳离子_____________。
(4)反应消耗铁粉11.2g,则废液中Fe3+的物质的量浓度是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3 mol·L-1 NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1 g,则下列有关叙述中正确的是( )
A. 加入合金的质量不可能为6.4 g
B. 参加反应的硝酸的物质的量为0.1 mol
C. 沉淀完全时消耗NaOH溶液的体积为150 mL
D. 溶解合金时收集到NO气体的体积在标准状况下为2.24 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com