
比较法是化学中研究物质性质的基本方法之一,请运用比较法解答下题。Na2O2几乎可与所有的常见气态非金属氧化物反应。如
2Na2O2+2CO2 == 2Na2CO3+O2, Na2O2+CO = Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式: _________________;___________________。
(2)通过比较可知,当非金属元素处于____________价时,其氧化物与Na2O2反应有O2生成。
(3)依上述规律,写出Na2O2与N2O5反应的化学方程式________________________________。
(1)Na2O2+SO2 = Na2SO4 2Na2O2+2SO3 =2Na2SO4 + O2
(2) 最高化合价
(3) 2Na2O2+2N2O5 =4NaNO3 + O2
【解析】
试题分析:(1)过氧化钠与二氧化硫反应时二氧化硫具有还原性,过氧化钠具有氧化性,二者发生氧化还原反应,过氧化钠中O元素的化合价只能降低,所以生成硫酸钠,化学方程式为Na2O2+SO2 = Na2SO4;过氧化钠与三氧化硫反应时,与二氧化碳的反应类似,生成硫酸钠和氧气,化学方程式是2Na2O2+2SO3 =2Na2SO4 + O2;
(2)根据以上事实,可知二氧化碳、三氧化硫中非金属元素的化合价是最高价,所以生成盐和氧气;
(3)根据以上规律N2O5中N元素的化合价是+5价,是最高价态,所以生成硝酸钠和氧气,化学方程式为2Na2O2+2N2O5 =4NaNO3 + O2
考点:考查比较法在化学中的应用


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届湖北省四校高三上学期期中联考化学试卷(解析版) 题型:选择题
下列关于实验操作的说法正确的是( )
A.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾淀粉试纸检验,观察试纸颜色的变化
B.盛放NaOH溶液时,使用带玻璃瓶塞的磨口瓶
C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出
D.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏高
查看答案和解析>>
科目:高中化学 来源:2015届海南省高三第四次月考化学试卷(解析版) 题型:选择题
常温下,向0.1 mol/L的H2SO4溶液中逐滴加入0.1 mol/L 的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示,下列说法中正确的是( )
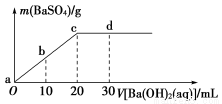
A.a~d溶液的pH:a<b<c<d
B.a~d溶液的导电能力:a<b<c<d
C.b处溶液的c(H+)与d处溶液的c(OH-)相等
D.c处溶液和d处溶液均呈碱性
查看答案和解析>>
科目:高中化学 来源:2015届浙江省协作体高三第一次适应性测试理科综合化学卷(解析版) 题型:填空题
(14分)黄铜矿CuFeS2可用于冶炼铜,冶炼原理为:2CuFeS2+2SiO2+5O2=2Cu+2FeSiO3+4SO2。
(1)黄铜矿冶炼铜产生的炉渣中主要含Fe2O3、FeSiO3、SiO2、Al2O3等,请完成以下验证炉渣中含有+2价的铁的探究过程中的有关问题:
仅限选择的试剂有:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水
①应选用试剂为 。
②有关的实验现象为 。
(2)据报道,有一种叫Thibacillus Ferroxidans的细菌在氧气存在下,酸性溶液中,将黄铜矿CuFeS2氧化成硫酸盐:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O。利用反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):

①操作a的名称是 ,操作b的操作方法是 。
②检验溶液B中Fe3+是否被除尽的试剂是 ,证明Fe3+已被除尽的现象是 。
③在实验室中,设计两个原理不同的方案,从溶液B中提炼金属铜(要求:一种方案只用一个反应来完成)。写出两种方案的化学方程式:
方案一: ; 方案二: 。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省协作体高三第一次适应性测试理科综合化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.向Na2CO3溶液通入CO2,可使水解平衡:CO32 -+H2O HCO3- +OH-向正反应方向移动,则溶液pH增大
HCO3- +OH-向正反应方向移动,则溶液pH增大
B.室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4
C.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA
D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH值
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期回头考试化学试卷(解析版) 题型:选择题
某溶液中在25℃时由水电离出的氢离子浓度为1×10-12 mol/L,下列说法正确的是( )
A.HCO3-离子在该溶液中一定不能大量共存
B.该溶液的pH一定是12
C.向该溶液中加入铝片后,一定能生成氢气
D.若该溶液的溶质只有一种,它一定是酸或碱
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三上学期回头考试化学试卷(解析版) 题型:选择题
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl = Na2Mn5O10+2AgCl 下列“水” 电池在海水中放电时的有关说法正确的是( )
A.正极反应式:Ag+Cl--e-== AgCl
B.每生成1 mol Na2Mn5O10转移2 mol电子
C.Na+不断向“水”电池的负极移动
D.AgCl是还原产物
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三第一次联考化学试卷(解析版) 题型:选择题
一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g) CH3OCH3(g)+H2O(g),则下列说法正确的是
CH3OCH3(g)+H2O(g),则下列说法正确的是
容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 |
|
|
Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
A、该反应的正方应为吸热反应
B.达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ的小
C.容器I中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高三9月月考化学试卷(解析版) 题型:填空题
(10分)如图所示的实验装置可用来测定含两种元素的某种气体X的化学式?
在注射器A中装有240 mL气体X,慢慢通过不含空气并装有红热的氧化铜的玻璃管B,使之完全反应,得到下面的实验结果:
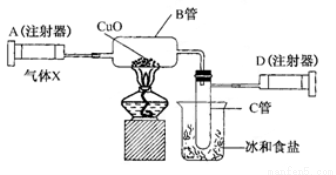
实验前B管总重20.32 g,实验后B管总重20.00 g,B管中的黑色粉末变成红色粉末?
在C管中收集到的无色液体是水;在注射器D中收集的气体是氮气?试回答下列问题:
(1)X气体是由________和________元素组成的?
(2)若240 mL X气体完全反应后,收集到的氮气质量是0.28 g?根据实验时温度和压强计算1 mol X气体的体积是24000 mL,则X的摩尔质量是________g/mol?
(3)通过计算,确定X的化学式为________?
(4)写出B中发生反应的化学方程式(X在该条件下不发生分解反应)_______________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com