
�о���Ա���������һ�֡�ˮ����أ����ֵ�������õ�ˮ�뺣ˮ֮�京���������з��磬�ں�ˮ�е���ܷ�Ӧ�ɱ�ʾΪ��5MnO2��2Ag��2NaCl = Na2Mn5O10��2AgCl ���С�ˮ�� ����ں�ˮ�зŵ�ʱ���й�˵����ȷ����(�� ��)
A��������Ӧʽ��Ag��Cl����e��== AgCl
B��ÿ����1 mol Na2Mn5O10ת��2 mol����
C��Na��������ˮ����صĸ����ƶ�
D��AgCl�ǻ�ԭ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�����и�����У������ѧ�Ծ��������棩 ���ͣ�ѡ����
��C6H10O2������ͬ���칹���У�����Na2CO3��Һ��Ӧ����CO2���������ʹ������Ȼ�̼��Һ��ɫ����(������˳���������칹)
A��8�� B��13�� C��17�� D��21��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�캣��ʡ�������Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Ԫ�����ڱ������е�����Ԫ��.������������˵��X�ķǽ����Ա�Yǿ����
A.Xԭ�ӵĵ��Ӳ�����Yԭ�ӵĵ��Ӳ�����
B.X���⻯��ķе��Y���⻯��ķе��
C.X����̬�⻯���Y����̬�⻯���ȶ�
D.Y�ĵ����ܽ�X��NaX����Һ���û�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ѧ�ڻ�ͷ���Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
�ȽϷ��ǻ�ѧ���о��������ʵĻ�������֮һ�������ñȽϷ�������⡣Na2O2�����������еij�����̬�ǽ��������ﷴӦ����
2Na2O2+2CO2 == 2Na2CO3+O2�� Na2O2+CO = Na2CO3��
��1���Էֱ�д��Na2O2��SO2��SO3��Ӧ�Ļ�ѧ����ʽ�� _________________��___________________��
��2��ͨ���ȽϿ�֪�����ǽ���Ԫ�ش���____________��ʱ������������Na2O2��Ӧ��O2���ɡ�
��3�����������ɣ�д��Na2O2��N2O5��Ӧ�Ļ�ѧ����ʽ________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ѧ�ڻ�ͷ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ӡ��⡱ʳ�ν϶��ʹ���˵����(KIO3)��������ڹ�ҵ�Ͽ��õ�ⷨ��ȡ����ʯī�Ͳ����Ϊ�缫����KI��ҺΪ���Һ����һ�������µ�⣬��Ӧ�Ļ�ѧ����ʽΪ��KI��3H2O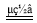 KIO3��3H2���������й�˵������ȷ���� �� ��
KIO3��3H2���������й�˵������ȷ���� �� ��
A�����ת��3 mol e��ʱ�������Ͽ��Ƶ�KIO3 107 g
B�����ʱ�� ʯī�������������������
C�����ʱ�������缫��Ӧʽ��I��?6e����3H2O = IO3����6H��
D���������е������Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ѧ�ڻ�ͷ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и����У����ɡ����ۼ������ϵ����ȷ���� ( )
A�����ڼ���EN��N> ECl-Cl���ʵ��ʵķе㣺N2>Cl2
B�����ڷ����пɵ����H+����H2SO4> CH3COOH�������ߵ����ԣ�H2SO4>CH3COOH
C������Ԫ�صķǽ�����N>P�����⻯����ȶ��ԣ�NH3>PH3
D�����ڽ�����Fe>Cu�� �ʻ�ԭ��Fe2+>Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ʮУ�����������һ��������ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣�.���������[(NH4)2Fe(SO4)2��6H2O]�������������ױ������������Ƿ�����ѧ����Ҫ���Լ��������ڴ������������������������ 500��ʱ��������������ȫ�ֽ⡣�ش��������⣺
��1����������笠�������������ȫ�ֽ⣬������������ԭ��Ӧ��������������FeO��Fe2O3��������������NH3��SO3��H2O��N2�͡��������� ���� ��
��2��Ϊ����ֽ����ijɷݣ��������ʵ��װ�ý���ʵ�飬����A�е�������������ֽ���ȫ��
�� A�й����ּ��Ƚϳ�ʱ���ͨ�뵪����Ŀ���ǡ��������� ������������ ��
��Ϊ��֤A�в������Ƿ���FeO����Ҫѡ�õ��Լ��С�������������
��A��KSCN��Һ���� ��B��ϡ���ᡡ��������
C��Ũ���� ��D��KMnO4��Һ
��װ��B��BaCl2��Һ��������Ϊ�˼���ֽ�������Ƿ��С��������� �������ɣ������и����壬�۲쵽������Ϊ������������������ �������������������� ��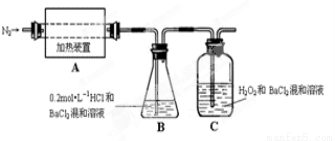
����A�зֽ������N2�����������ֻ��Fe2O3��Fe2O3�����ʵ���Ϊbmol��C�г������ʵ���Ϊamol����b���� ��a������ڡ�����С�ڡ����ڡ���
��ʵ���У��۲쵽C���а�ɫ�������ɣ���C�з����ķ�ӦΪ����������������������������������������
�������ӷ���ʽ��ʾ����
��3����֪�������ӱ����������ķ�Ӧ�ǣ�4Fe2+ + O2 + (4+2x) H2O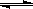 2Fe2O3?xH2O + 8H+�������������Һ������������Һ���ױ�������������ԭ���ǡ��� ������ �� ��������������
2Fe2O3?xH2O + 8H+�������������Һ������������Һ���ױ�������������ԭ���ǡ��� ������ �� ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ʮУ�����������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ������У�ʼ���������������
A��Cl2ͨ��FeSO4��Һ�� B��CO2ͨ��Ca(OH)2��Һ��
C����AlCl3��Һ���� NaOH ��Һ�� D��SO2ͨ��BaCl2��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ����9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ͭм���뵽100 mLŨ�Ⱦ�Ϊ2 mol��L��1��HNO3��H2SO4�Ļ����Һ�У���ַ�Ӧ��ת�Ƶ��ӵ����ʵ���Ϊ (����)
A��0.6 mol��������B��0.8 mol C��0.45 mol������D��0.4 mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com