
【题目】下列各组物质相互混合反应后,最终无白色沉淀生成的是
A. 过量Ba(OH)2溶液加入明矾溶液中 B. 过氧化钠投入FeCl2溶液中
C. 向NaAlO2溶液中通入过量CO2 D. 向饱和Na2CO3溶液中通入过量CO2
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】CO2既是温室气体,也是重要的化工原料,二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)用活性炭还原法可以处理汽车尾气中的氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+ 2NO(g) ![]() N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g) △H,在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
浓度/(mol/L)/\时间/min | 0 | 10 | 20 | 30 | 40 |
NO | 2.0 | 1.16 | 0.40 | 0.40 | 0.6 |
N2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 1.2 |
①若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:3:3,则达到新平衡时NO的转化率____(填“升高”或“降低”),△H____0(填“>”或“<”)。
②根据图表数据分析T1℃时,该反应在0~10min内的平均反应速率v(N2)=__mol·L-1·min-1;计算该反应的平衡常数K=___。
③若30min后只改变某一条件,据上表中的数据判断改变的条件可能是____________(填字母编号)。
A.加入合适的催化剂 B.适当缩小容器的体积
C.通入一定量的NO D.加入一定量的活性炭
(2)工业上用CO2和H2反应合成二甲醚(CH3OCH3)。二甲醚燃料电池具有能量转化率高、电量大的特点而被广泛应用,一种二甲醚氧气电池(电解质为KOH溶液)的负极反应式为:______________。
(3)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。若某次捕捉后得到pH=10 的溶液,则溶液c(CO32-)∶c(HCO3-)=____________。[常温下K1(H2CO3)=4.4×10-7、 K2(H2CO3)=5×10-11]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。

请回答下列问题:
(1)物质A的化学式为____________________。
(2)写出单质B与强碱溶液反应的离子方程式_______________,氧化物D与NaOH溶液反应的化学方程式________________________________。
(3)溶液E中加入氨水时,先生成白色沉淀L,L最终变为红褐色沉淀G,写出L变为G的化学反应方程式__________________________________。
(4)溶液E敞口放置容易变质,写出检验溶液E是否变质的实验操作、现象及结论__________,为了防止溶液E的变质,可往溶液中加入___________________。
(5)溶液I中所含金属离子是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数。下列叙述中正确的是( )
A. 标准状况下,22.4 L SO3中含SO3分子数为NA
B. 46 g NO2中含有分子数为NA
C. 标况下22.4L Cl2与足量的NaOH溶液反应,转移的电子数为2NA
D. 标况下,足量的Fe与22.4L Cl2发生燃烧反应(Cl2完全反应),转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的量热计中,将100mL0.50mol/L CH3COOH溶液与100mL0.55mol/LNaOH溶液混合,温度从25.0℃升高到27.7℃。已知该量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J·℃-1,生成溶液的比热容为4.184J·g-1·℃-1,两溶液的密度均近似为lg/mL.下列说法错误的是
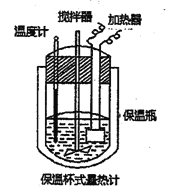
A. 若量热计的保温瓶绝热效果不好,则所测△H偏大
B. 该实验测得反应放出的热量为2665.7J
C. 该实验测得的中和热ΔH为-45.2kJ/mol
D. 所加NaOH溶液过量,目的是保证CH3COOH溶液完全被中和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是( )
 (选项中按 W X Y Z 的顺序)
(选项中按 W X Y Z 的顺序)
A. S SO2 SO3 H2SO4 B. Na Na2O2 NaOH NaCl
C. Fe FeCl3 Fe(OH)2 FeCl2 D. Al AlCl3 NaAlO2 Al2(SO4)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,硫化铜矿的湿法冶炼技术已经取得了很大的发展。现有一种催化氧化酸浸硫化铜矿的冶炼法,其工艺流程如图所示:

反应温度、固液比、反应时间、氯离子浓度都对铜的浸出率有较大的影响,下面是实验得出的这几种因素对铜的浸出率影响的变化曲线图(如图~如图所示)。

回答下列问题:
(1)火法炼铜的主要反应:①2CuFeS2+4O2![]() Cu2S+3SO2+2FeO(炉渣);
Cu2S+3SO2+2FeO(炉渣);
②2Cu2S+3O2![]() 2Cu2O+2SO2;③2Cu2O+Cu2S
2Cu2O+2SO2;③2Cu2O+Cu2S![]() 6Cu+SO2↑;则在反应①、②、③中被氧化的元素为_______(填元素符号);若生成的SO2在标准状况下体积为4.48L,则发生转移的电子数目为________NA;由amolCuFeS2生成amolCu,共消耗________molO2。
6Cu+SO2↑;则在反应①、②、③中被氧化的元素为_______(填元素符号);若生成的SO2在标准状况下体积为4.48L,则发生转移的电子数目为________NA;由amolCuFeS2生成amolCu,共消耗________molO2。
(2)写出反应1的化学方程式:________________。经查,硫黄、FeSO4·7H2O均可入药,用途广泛,湿法炼铜与火法炼铜相比,优点是_____________________。
(3)从溶液中得到FeSO4·7H2O晶体的操作是_______________________________。
(4)根据实验以及工业生产的实验要求,从下表中得出的最佳工艺条件为________(填字母代号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结晶玫瑰是具有玫瑰香气的香料,可由下列方法合成(部分反应物及反应条件未标出)。

已知:![]() (-R表示烃基)
(-R表示烃基)
(1)A是苯的一种同系物,相同条件下,其蒸气对氢气的相对密度是46,则A的名称是________。
(2)反应②所需药品及反应条件是________________。
(3)C的核磁共振氢谱峰面积之比是________。
(4)⑤的化学方程式是_____________________________________________________。
(5)C有多种同分异构体,其中属于芳香族化合物的有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH <0,写出该反应的化学平衡常数表达式K=___________。降低温度,二氧化硫的转化率___________(填“增大”“ 减小”“ 不变”)。
2SO3(g) ΔH <0,写出该反应的化学平衡常数表达式K=___________。降低温度,二氧化硫的转化率___________(填“增大”“ 减小”“ 不变”)。
(2)Na2CO3溶液显___________(填“酸性”、“碱性”或“中性”),室温下,pH=10的溶液中,由水电离出的c(OH-)=___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com