
����Ŀ��ʵ��������480mL��0.1mol/L��CuCl2��Һ��ʵ�ʲ��������У�
������ƽ�ϳ���һ������CuCl2�������ձ�����ˮ�ܽ⣻
�ڰ��Ƶõ���ҺС�ĵ�ע������ƿ�У�
�ۼ���������ƿ�м�ˮ����̶�1��2���״������ý�ͷ�ιܼ�ˮ���̶ȣ�
��������ˮϴ���ձ��Ͳ�����2��3�Σ�ÿ�ν�ϴ��Һת������ƿ����ҡ�ȣ�
�ݽ�����ƿ�����������ҡ�ȡ���д���пհף�
(1)����CuCl2����������______��
(2)�����������ȷ˳����(�����)________��
(3)��ʵ��ʹ�õ��IJ����������ձ�������������ͷ�ιܡ�______����������
(4)��û�н��Тܲ�������ʹ���(��ƫ�ߡ�ƫ�ͻ���Ӱ�죬��ͬ)_____��
(5)������ƽ�ƹ���ʱ��������մ�����ۣ��������Ƶ���ҺŨ�Ƚ�_______��
���𰸡�6.8g �٢ڢܢۢ� 500mL����ƿ ƫ�� ƫ��
��������
��������һ�����ʵ���Ũ����Һ��ʵ�鲽�衢��������������𣻸���ʵ�������c=![]() ������������
������������
(1)Ҫ����480mL0.1mol/L��CuCl2��Һ��ʵ��������500mL����ʵ�������������ã�m(CuCl2)=McV=135g/mol��0.5L��0.1mol/L=6.75g�����������������Ϊ6.8g���ʴ�Ϊ��6.8��
(2)����һ�����ʵ���Ũ�ȵ���Һ��ȷ��������Ϊ���㡢�������ܽ⡢��ȴ��ת�ơ�ϴ�ӡ����ݡ�ҡ�ȵȣ�������ȷ������˳��Ϊ���٢ڢܢۢݹʴ�Ϊ���٢ڢܢۢݣ�
(3)���ƹ�������Ҫʹ�õIJ��������У�500mL����ƿ���ձ�������������ͷ�ιܣ��ʴ�Ϊ��500mL����ƿ��
(4)��û�н���ϴ�Ӳ�����ת��������ƿ�е��������ʵ���ƫС����ʹ���ƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�
(5)����ʱ�������������ۣ��������������ӣ����³���������ƫ�࣬�������Ƶ���ҺŨ�Ƚ�ƫ�ߣ��ʴ�Ϊ��ƫ�ߡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪H-H���ļ���Ϊ436kJ�� mol-1��H-N���ļ���Ϊ391 kJ�� mol-1�������Ȼ�ѧ����ʽ��N2(g)+3H2(g) ![]() 2NH3(g) ��H=-92.4 kJ�� mol-1����֪N��N���ļ�����
2NH3(g) ��H=-92.4 kJ�� mol-1����֪N��N���ļ�����
A.431 kJ�� mol-1B.649 kJ�� mol-1C.945.6 kJ�� mol-1D.896 kJ�� mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼװ����,��U�ιܵײ�ʢ��CCl4,�ֱ���U�ι�����С�ĵ��뱥��ʳ��ˮ��ϡ������Һ,��ʹa��b����Һ����ƽ,Ȼ��ֱ����ϲ�������˿������,�ܷ��,����һ��ʱ���,�����й������д������

A. ��˿�������ĸ�ʴ����:a < b
B. a��b������ͬ�ĵ缫��ӦʽΪFe-2e-==Fe2+
C. һ��ʱ���,a��Һ�����b��Һ��
D. ����˿�е�̼��a��b�����ֱ���ԭ��صĸ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʳ��ά���е�ͻ���������ܣ��������ܵ����ǵ��ձ��ע��������������֯��Ϊ����ġ�����Ӫ���ء���ľ������һ�ַ�������ʳ��ά���䵥��֮һ�ǽ��Ӵ����ṹ��ͼ��ʾ�������йؽ��Ӵ���˵����ȷ����( )
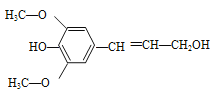
A�����Ӵ��ķ���ʽ��C11H12O4
B�����Ӵ�����������ԭ�ӿ�����ͬһƽ��
C��1mol���Ӵ�����������ˮ��Ӧ����3molBr2
D��1mol���Ӵ���������������Ӧ��������4mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ʯī�缫���100mL��0.1molL-1NH4Cl��Һ������������Һ����仯���Բ��ƣ���Һ��pH�����������������(��״����)�仯��������ͼ������˵����ȷ���ǣ� ��
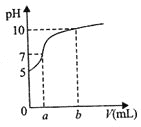
A.��ҺpH=5ʱ��c(NH3H2O)=1.0��10-5molL-1
B.������ʹNH4+��ˮ��̶ȼ�С��pH����
C.��b=56mL��c(NH4+)��5.01��10-2molL-1
D.��������������bmL��������ͨ����Һ��c(NH4+)����ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25 ��ʱ��HCN�ĵ��볣��Ka��6.2��10��10 mol��L��1��CH3COOH�ĵ��볣��Ka��1.7��10��5 mol��L��1������������ĸ�ͼ��ش����⡣
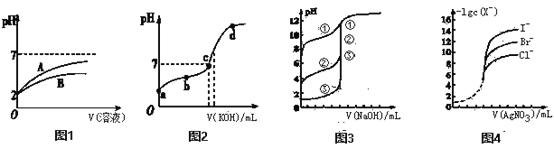
(1)25 ��ʱ�������Ϊ100 mL��pH��2��CH3COOH��Һ��HCN��Һ����ˮϡ��������Һ��pH�仯����Һ����Ĺ�ϵ��ͼ1��ʾ�����ʾCH3COOH��Һ��pH�仯���Ƶ������ǣ�______(����A������B��)����ͬ�����£�NaCN��Һ��pH________(�� ��>������������<��)CH3COONa��Һ��pH����0.2 mol��L��1HCN��Һ��0.1mol��L��1NaOH��Һ�������ϣ�����Һ������Ũ���ɴ�С˳��Ϊ______________������ʾ���ɸ���ƽ�ⳣ����С��ϵ�жϷ�Ӧ�̶ȴ�С��
(2)��ͼ2��ʾ��25 ��ʱ��20 mL 0.01 mol��L��1CH3COOH��Һ����μ���0.01 mol��L��1 KOH��Һ����pH�仯������ͼ��ʾ(�����¶ȱ仯)������˵����ȷ����_______
A��a����Һ��c(H��)Ϊ1��10��4 mol��L��1
B��a��b��c��d�ĵ���ˮ�ĵ���̶�������c��
C���ζ���������ѡ�÷�̪��ָʾ��
D��b����Һ������Ũ�ȴ�С˳��һ��Ϊc(CH3COO��)> c(H��)>c(K��)>c(OH��)
(3)��ͼ3��ʾ����ͬ��NaOH��Һ�ֱ�ζ�Ũ����ͬ������һԪ�ᣬ��ͼ��֪������ǿ����_____�������١����ڡ��������ۡ� ����
(4)��ͼ4��ʾ��ͬŨ�ȵ�AgNO3����Һ�ֱ�ζ�Ũ����ͬ�ĺ�Cl-��Br- ��I-�Ļ����Һ����ͼ��ȷ�����ȳ�����������________����֪25 ��ʱKsp(AgCl)��2��10��10����1L 0.1mol/L��NaCl��Һ�м���1L 0.2mol/L��AgNO3��Һ����ַ�Ӧ����Һ��c(Cl��)=_________����������Һ�����Ϊ2L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ӣ����һ�ֿ�������ˮ����ӣ���к���һ���ǻ��ᣬ��ṹ��ͼ�������йظ��ǻ����˵���в���ȷ����
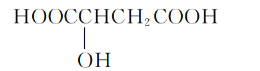
A.���ǻ���ķ���ʽΪC4H6O5
B.���ǻ���ɷ���������Ӧ
C.���ǻ���ɷ���ȡ����Ӧ
D.0.1mol���ǻ�����ȫȼ��ʱ����6.72L O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ����0.10 mol��L��1��NaOH��Һ�ζ�ijŨ�ȵ����ᡣ��¼�������£�
ʵ����� | ����Һ���(mL) | ������NaOH��Һ�����(mL) | |
�ζ�ǰ | �ζ��� | ||
1 | 20.00 | 0.50 | 20.54 |
2 | 20.00 | 6.00 | 26.00 |
3 | 20.00 | 1.40 | 21.36 |
(1)��������ʵ���Ũ��Ϊ_____��
(2)��ʽ�ζ��ܼ��첿�������ݣ��ζ�����ʧ���Բⶨ�����Ӱ����_____(�ƫ�ߡ���ƫ�͡�����Ӱ�족)��
(3)�����й�ʵ���˵����ȷ����______��
A.�ڲⶨ�кͷ�Ӧ�ķ�Ӧ��ʵ���У�����Ҫ�������¶�
B.����pH��ֽ�ⶨ������ˮ�е�pH
C.�к͵ζ�ʵ���У�ϴ�������ƿ����Ҫ����
D.��CH3COONa��Һ�е���ʯ����Һ����Һ����
E.���ɫZnS�����ϵμ�CuSO4��Һ��������Ϊ��ɫ��˵��Ksp(ZnS)<Ksp(CuS)
(4)�����£�pH=5�������pH=9������������Һ�������9��11��ϣ�����Һ��pH=_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ�ֹ㷺���ڵ��Ӻ�ͨ���������Ҫ�������仯ѧ�����������ơ�
(1)��ҵ���ᴿ�صķ����кܶ࣬�����Ե�⾫����Ϊ��������ԭ������:�Դ��ᴿ�Ĵ���(����Zn��Fe��Cu����)Ϊ�������Ըߴ���Ϊ��������NaOHˮ��ҺΪ�������Һ���ڵ���������ʹ�����������ܽ����������Һ��ͨ��ij������Ǩ�Ƽ��������������������ŵ������ߴ��ء�
����֪���ӵ�������˳��ΪZn2+<Ga3+<Fe2+<Cu2+��⾫����ʱ������ijɷ�Ϊ________��
��GaO2�� �������ŵ�ĵ缫��ӦʽΪ______��
(2)��ҵ�����ù�̬Ga��NH3�ڸ��������ºϳɹ�̬�뵼����ϵ�����(GaN)��ͬʱ���������ɡ���Ӧ������ÿ����3 mol H2���ų�30.8 kJ��������
���÷�Ӧ���Ȼ�ѧ����ʽΪ______��
��һ�������£�һ������Ga��NH3����������Ӧ����������������ʵ�ҿ���Ϊ�жϷ�Ӧ�Ѵﵽƽ��״̬�ı�־����______(����ĸ)��
A. ���º�ѹ�£����������ܶȲ���
B. ����3 mol H��H����ͬʱ����2 mol N��H��
C. ���º�ѹ�£���Ӧ�ﵽƽ��ʱ,��Ӧ��ϵ�м��� 2 mol H2��NH3���������ʵ���ԭƽ��ʱNH3����������
D. ���º����£� NH3 ��H2�����ʵ���Ũ��֮��Ϊ2�U3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com