
���л��ﻯѧ������
ƻ����㷺������ƻ����ˮ���Ĺ����У���һ�ֳ��õ�ʳƷ���Ӽ������ⶨ��ƻ�������Է�������Ϊ134��������Ԫ�ص���������Ϊ��w(c)=35.82% W(H)=4.86%,����Ϊ�������д���5�ֲ�ͬ��ѧ������Hԭ�ӡ�1molƻ��������2molNaHCO3��ȫ��Ӧ������������Na��Ӧ����1.5molH2�ġ�����ϩΪԭ���˹��ϳ�ƻ�������·���£�
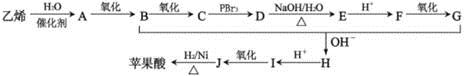
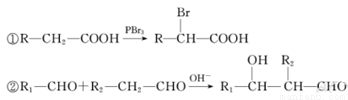
��֪��
��ش��������⣺
��1��ƻ����ķ���ʽΪ_______��A���ʵ�����Ϊ_______��
��2��F�к��еĹ�����������_______��G+B��H�ķ�Ӧ������_______��
��3���ںϳ���·�У�C��D��һ���跴Ӧ��Ŀ����_____��
��4��D��E��Ӧ�Ļ�ѧ����ʽΪ_________��
��5��ƻ�����NaHCO3��ȫ��Ӧ�Ļ�ѧ����ʽΪ________��
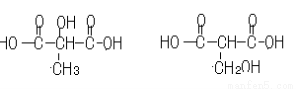
��6����ƻ���Ậ����ͬ����������Ĺ����ŵ�ͬ���칹��Ľṹ��ʽΪ____��
��1��C4H6O5 �Ҵ�
��2�� �ǻ����Ȼ� �ӳɷ�Ӧ��
��3����C����������Brԭ�ӣ�
��4��Br��CH2��COOH+2NaOH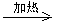 HO��CH2��COONa+NaBr+H2O
HO��CH2��COONa+NaBr+H2O
��5��
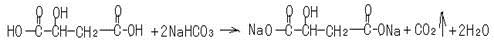
��6��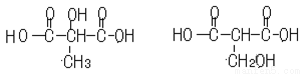
����������1������̼���⡢��ԭ�ӵ�������������Է��������������ƻ����ķ���ʽ��C4H6O5����ϩ��ˮ�ڴ�������ʱ�����ӳɷ�Ӧ����A���Ҵ���������������̼ԭ�Ӳ����֪��B����ȩ��C����������Ϣ�ٽ�һ���ƶϣ�D��BrCH2COOH��E��HOCH2COONa��F��HOCH2COOH��G��OHC-CH2COOH��������Ϣ�ڣ����ɵ�HΪNaOOC-CH��OH��-CH2CHO���ữ���I��HOOCH��OH��-CH2CHO��I������ΪJ��J��HOOC-CO-CH2-COOH��������������õ�ƻ���HOOC-CH��OH��-CH2COOH��
��3���������ͼ֪��C��D��һ����Ӧ��Ŀ����Ϊ����C������Brԭ�ӡ�
��4��D��E�Ļ�ѧ����ʽ��Br��CH2��COOH+2NaOH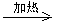 HO��CH2��COONa+NaBr+H2O
HO��CH2��COONa+NaBr+H2O
��5��ƻ�����NaHCO3��ȫ��Ӧ�Ļ�ѧ����ʽ��
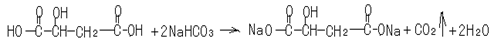
��6����ƻ���Ậ����ͬ�������Ŀ�Ĺ����ŵĽṹΪ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��16 ���ͣ�ѡ����
�������������ʶ�У�����ȷ����
A���������ø�������������л�����ӣ�ʹ֮����ɴ���ġ���Ƭ���������������������л���ṹ�ķ���
B�������ЧӦ������������Һ�뽺�壬�ơ�����ϡ������ܲ��������ЧӦ
C���Ȱ���(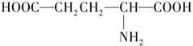 )���۵�ߴ�205�棬�����ڱ����л��ܼ�����Ҫ����Ϊ�γ�����
)���۵�ߴ�205�棬�����ڱ����л��ܼ�����Ҫ����Ϊ�γ�����
D�����ع��͡������ӹ������Ƶ÷�����������ͣ�����ʵ�ֳ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��15 ���ͣ�ѡ����
��֪(HF)2(g)  2HF(g)����H>0����ƽ����ϵ��������(m��)�������ʵ���(n��)֮���ڲ�ͬ�¶�����ѹǿ�ı仯������ͼ��ʾ������˵����ȷ����
2HF(g)����H>0����ƽ����ϵ��������(m��)�������ʵ���(n��)֮���ڲ�ͬ�¶�����ѹǿ�ı仯������ͼ��ʾ������˵����ȷ����
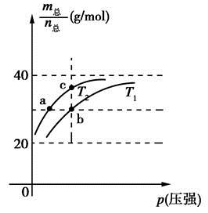
A���¶ȣ�T1<T2
B��ƽ�ⳣ����K(a)��K(b)<K(c)
C����Ӧ���ʣ�vb>va
D���� 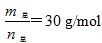 ʱ��n(HF):n[(HF)2]��2:1
ʱ��n(HF):n[(HF)2]��2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��14 ���ͣ�ѡ����
��ͼ�Dz��ֶ�����Ԫ��ԭ�Ӱ뾶��ԭ�������Ĺ�ϵͼ��������˵����ȷ����
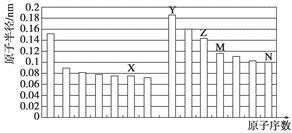
A��Z��N����Ԫ�ص����Ӱ뾶��ȣ�ǰ�߽ϴ�
B��X��N����Ԫ�ص���̬�⻯��ķе���ȣ�ǰ�߽ϵ�
C����X��M����Ԫ����ɵĻ����ﲻ�����κ��ᷴӦ��������ǿ�Ӧ
D��Z���������ֱܷ��ܽ���Y�����������N���⻯���ˮ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ�ʵ����
п�̸ɵ�������Ĺ���������ڷ�������뻷���н��������Σ�����ԷϾɵ�ؽ�����Դ�������Ե÷dz���Ҫ��ij��ѧ��ȤС����������´����������շϵ���еĸ�����Դ��
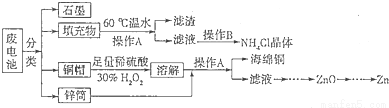
��1������п�̸ɵ�صĵ����ΪKOH���ܷ�ӦΪZn+2MnO2+2H2O=2MnOOH+Zn(OH)2���为���ĵ缫��ӦʽΪ ��
��2���������60����ˮ�ܽ⣬Ŀ���Ǽӿ��ܽ����ʣ�����������¶Ȳ���̫�ߣ���ԭ���� ��
��3������A������Ϊ ��
��4����������Ҫ�ɷ�Ϊ���̻������̻�����м���һ������ϡ���ᡢϡ���ᣬ�����Ͻ�����������Ϊֹ������Ҫ��ӦΪ2MnO(OH)+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2+6H2O��
�ٵ�1 mol MnO2�μӷ�Ӧʱ������ mol���ӷ���ת�ơ�
��MnO(OH)��Ũ�����ڼ���������Ҳ�ɷ�����Ӧ����д���䷴Ӧ�Ļ�ѧ����ʽ ��
��5��ͭñ�ܽ�ʱ����H2O2��Ŀ���� ���û�ѧ����ʽ��ʾ����ͭñ�ܽ���ȫ�ɲ���_______������ȥ��Һ�й�����H2O2��
��6��п�̸ɵ�������Ĺ�����KMnO4��Һ���ա��ڲ�ͬpH�£�KMnO4��Һ��Hg�������ʼ���Ҫ��������ͼ��ʾ��

������ͼ��֪��
��pH��Hg�����ʵ�Ӱ������� ��
����ǿ���Ի�����Hg�������ʸߵ�ԭ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ�ѡ����
���и������ʣ����ܰ�����ͼ����������ʾ��Ӧһ����ɣ���ϵת������
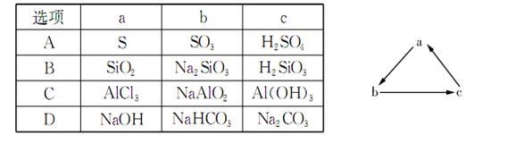
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��13 ���ͣ�ѡ����
ij�����X��Al2O3��Fe2O3��Cu��SiO2�е�һ�ֻ���������ɡ���������ʵ�飺

A��������м��ٵ�3 g����һ���ǻ����
B����������������ٵ�����һ����Cu
C�����ݲ��������жϻ����X�ijɷ�ΪAl2O3��Fe2O3��Cu��SiO2
D�����������������Եó�m(Fe2O3)��m(Cu)��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��12 ���ͣ�ѡ����
����˵������ȷ����
A����֪H2(g)��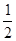 O2(g)===H2O(g)����H1��a kJ��mol��1��
O2(g)===H2O(g)����H1��a kJ��mol��1��
2H2(g)��O2(g)===2H2O(g)����H2��b kJ��mol��1����a��b
B��CO��ȼ����Ϊ283.0 kJ��mol��1����
2CO2(g)===2CO(g)��O2(g)����H����566.0 kJ��mol��1
C����N2(g)��3H2(g)  2NH3(g)����H����d kJ��mol��1������ij������Ͷ��1 mol N2��3 mol H2��ַ�Ӧ�ų�������С��d kJ
2NH3(g)����H����d kJ��mol��1������ij������Ͷ��1 mol N2��3 mol H2��ַ�Ӧ�ų�������С��d kJ
D��HCl��NaOH��Ӧ���к��Ȧ�H����57.3 kJ��mol��1����H2SO4��KOH��Ӧ���к��Ȧ�H����114.6 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��10 ���ͣ�ѡ����
����˵����ȷ����
A���������ڽ���Ԫ�ص������ﶼ���ڼ���������
B�����Ӳ�ṹ��ͬ�IJ�ͬ���ӣ���뾶��˵�����������С
C��IA��Ԫ�صĽ�����һ����IIA��Ԫ�صĽ�����ǿ
D����ԭ���γɵ�����,һ����ϡ������ԭ�ӵĺ�������Ų���ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com