
【题目】某铅酸蓄电池的工作原理如图所示,其总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列判断不正确的是( )
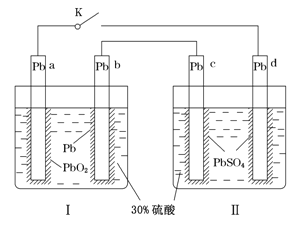
A. 闭合K时,d电极的反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42—
B. 当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol
C. 闭合K时,Ⅱ中SO42—向c电极迁移
D. 闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极
【答案】C
【解析】试题分析:断开K,I两个电极之间有电势差,II两个电极之间没有电势差,所以I是电源,II是电解池,K闭合后相当于I为II充电.K闭合,I中a为正极,b为负极,II中c为阴极,d为阳极,A、K闭合后相当于I为II充电.K闭合,I中a为正极,b为负极,II中c为阴极,d为阳极,K闭合时, d电极反应式:PbSO4+2H2O-2e-![]() PbO2+4H++S
PbO2+4H++S![]() ,A项正确;B、当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol ,B项正确;C、K闭合时, I中a为正极,b为负极,II中c为阴极,d为阳极,Ⅱ中S
,A项正确;B、当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol ,B项正确;C、K闭合时, I中a为正极,b为负极,II中c为阴极,d为阳极,Ⅱ中S![]() 向d电极迁移,C项错误;D、K闭合一段时间后断开,Ⅱ可单独作为原电池,d电极为正极,D项正确;答案选C。
向d电极迁移,C项错误;D、K闭合一段时间后断开,Ⅱ可单独作为原电池,d电极为正极,D项正确;答案选C。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 植物油氢化过程中发生了加成反应
B. 淀粉和纤维素互为同分异构体
C. 己烷与苯可用酸性KMnO4溶液鉴别
D. 水可以用来分离溴苯和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S废气资源化利用途径之一是回收能量并得到单质硫。反应原理为:2H2S(g) + O2(g) = S2(s) + 2H2O(l) ![]() H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法不正确的是
H=-632kJ·mol-1。右图为质子膜H2S燃料电池的示意图。下列说法不正确的是

A. 电路中每流过2mol电子,电池内部释放316kJ热能
B. 每34gH2S参与反应,有2mol H+经质子膜进入正极区
C. 电极a为电池的负极
D. 电极b上发生的电极反应为:O2+4e![]() +4 H+=2H2O
+4 H+=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.1mol的H2的体积为22.4LB.0.012kgC-12含有的原子数就是阿伏伽德罗常数
C.17gNH3中含有的电子数为10D.N2和CO的摩尔质量相等,都是28
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 标准状况下,5.6LCl2与足量NaOH反应转移的电子数为0.25NA
B. 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C. 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
D. 5NH4NO32HNO3+4N2↑+9H2O反应中,生成56gN2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各图与表述一致的是( )

A. 图①表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B饱和溶液分别升温至t2℃时,溶质的质量分数B>A
B. 用图②所示装置蒸发FeCl3溶液制备无水FeCl3
C. 图③可以表示向一定量的明矾溶液中逐滴摘加一定浓度氢氧化钡溶液时产生Al(OH)3沉淀的物质的量变化
D. 图④电解饱和食盐水的装置中,溶液A、B中由水电离出的c(H+):A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,下列溶液混合后,pH大于7的是
A. 0.1 mol·L-1的盐酸和pH=13的氢氧化钡溶液等体积混合
B. 0.1 mol·L-1的NaHCO3溶液和pH=1的盐酸等体积混合
C. pH=3的硫酸和pH=11的氨水等体积混合
D. pH=1的醋酸和0.1mol/L的氢氧化钠溶液等体积混合
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com