
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 标准状况下,5.6LCl2与足量NaOH反应转移的电子数为0.25NA
B. 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C. 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
D. 5NH4NO32HNO3+4N2↑+9H2O反应中,生成56gN2时,转移的电子数目为3.75NA
【答案】A
【解析】Cl2与足量NaOH反应生成氯化钠和次氯酸钠,1mol氯气转移1mol电子,所以标准状况下,5.6LCl2与足量NaOH反应转移的电子数为0.25NA,故A正确;室温下, pH=13的NaOH溶液中,由水电离的OH-离子的浓度是![]() ,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为
,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为![]() NA,故B错误;氢氧燃料电池正极是氧气得电子,1mol氧气得4mol电子,所以消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA,故C错误;根据方程式5NH4NO3
NA,故B错误;氢氧燃料电池正极是氧气得电子,1mol氧气得4mol电子,所以消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA,故C错误;根据方程式5NH4NO3![]() 2HNO3+4N2↑+9H2O,生成4molN2转移15mol电子,所以生成56gN2时,转移的电子数目为7.5NA,故D错误。
2HNO3+4N2↑+9H2O,生成4molN2转移15mol电子,所以生成56gN2时,转移的电子数目为7.5NA,故D错误。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】酚醛树脂是应用广泛的高分子材料,可用酚类与醛类在酸或碱的催化下相互缩合而成,类似的合成过程如:
反应①
反应②
(1)化合物Ⅰ的分子式______。
(2)苯酚与浓溴水反应的化学方程式为__________________。
(3)化合物Ⅱ 也能与CH3CHO发生类似反应①的反应,生成有机物Ⅲ,该反应化学方程式为___________________________________;写出有机物Ⅱ与足量NaHCO3反应的化学方程式________________________________。
也能与CH3CHO发生类似反应①的反应,生成有机物Ⅲ,该反应化学方程式为___________________________________;写出有机物Ⅱ与足量NaHCO3反应的化学方程式________________________________。
(4)有关化合物Ⅱ和Ⅲ的说法正确的有____(填字母)。
A.都属于芳香烃 B.含有官能团种类相同,性质也完全相同
C.二者互为同系物 D.1mol的Ⅱ或Ⅲ都能与2mol的NaOH完全反应
(5)符合下列有条件的化合物Ⅱ的同分异构体有_________种,写出其中苯环上一元取代只有两种的异构体的结构简式_________________________________。
①遇FeCl3溶液发生显色反应 ②可以发生银镜反应 ③可以发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请完成下列问题:
(1)画出氯原子结构示意图________;
(2)写出小苏打的化学式________;
(3)写出实验室制氯气的离子方程式________;
(4)写出红热的木炭与浓硫酸反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2O黄棕色具有强烈刺激性气味的气体,是一种强氧化剂,易溶于水且会与水反应生成次氯酸,与有机物、还原剂接触或加热时会发生燃烧并爆炸。种制取Cl2O 的装置如图所示。
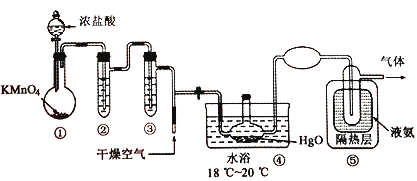
已知:C12O的熔点为-116℃,沸点为3.8℃,Cl2 的沸点为-34.6℃;HgO+2Cl2=HgCl2 +Cl2O
下列说法不正确的是
A. 装置②、③中盛装的试剂依次是饱和食盐水和浓硫酸
B. 通入干燥空气的目的是将生成的Cl2O稀释减少爆炸危险
C. 从装置⑤中逸出气体的主要成分是Cl2O
D. 装置④与⑤之间不用橡皮管连接,是为了防止橡皮管燃烧和爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定草酸晶体(H2C2O4xH2O)中的x值,进行如下实验
(1)称取Wg草酸晶体,配成100.00mL溶液
(2)取25.00mL所配溶液于锥形瓶内,加入适量稀H2SO4后,用浓度为amolL-1的KMnO4溶液滴定至KMnO4不再褪色为止,所发生的反应为:2KMnO4+5H2(C2O)4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
①实验中,不需要的仪器有(填序号)_______________
A、托盘天平(带砝码、镊子) B、滴定管 C、100mL的量筒
D、100mL的容量瓶 E、烧杯 F、漏斗 G、锥形瓶 H、玻璃棒
I、药匙 J、烧瓶
②实验中,标准液KMnO4溶液应装在_______式滴定管中,因为________________
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得的x的值会_________(填偏大、偏小、无影响).
④在滴定过程中若用去amolL-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为_____________molL-1,由此,x=_____________ .
⑤若滴定终点读数时俯视刻度,则计算的x值会_______(填偏大、偏小、无影响).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铅酸蓄电池的工作原理如图所示,其总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列判断不正确的是( )
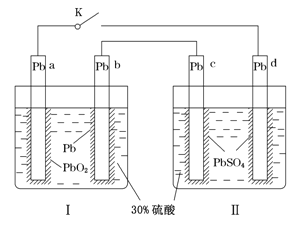
A. 闭合K时,d电极的反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42—
B. 当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol
C. 闭合K时,Ⅱ中SO42—向c电极迁移
D. 闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质子交换膜燃料电池(简称:PEMFC),又称固体高分子电解质燃料电池,是一种以含氢燃料与空气作用产生电力与热力的燃料电池,膜极组和集电板串联组合成一个燃料电池堆。目前,尤以氢燃料电池倍受电源研究开发人员的注目。它的结构紧凑,工作温度低(只有80℃),启动迅速,功率密度高,工作寿命长。工作原理如图,下列说法正确的是

A. 可用一氧化碳代替图中氢气形成质子交换膜燃料电池
B. B极的电极反应式为O2+4H++4e-=2H2O
C. 用该电池作为精炼铜的电源时,A极与粗铜电极相连
D. 当外电路中转移0.1mole-时,通过质子交换膜的H+数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取Fe和Fe2O3 的混合物 15 g,加入150 mL 2 mol/L 的稀硫酸,固体混合物完全溶解,放出气体 1.68 L(标准状况下),向所得溶液中滴入硫氰化钾溶液,未见颜色变化。若要使该溶液中的铁元素完全转化为沉淀,需加入3 mol/L 的NaOH溶液的体积为( )
A. 150 mL B. 200 mL C. 225 mL D. 250 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对实验仪器特点的描述正确的或实验能达到预期目的的是( )
A.用10mL量筒去量取5.35mL浓硫酸
B.用托盘天平称量6.25g硝酸钾固体
C.量筒的“0”刻度在下面
D.容量瓶上的标识有温度、容量和刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com