
【题目】在某温度下,向三个初始体积为1L的密闭容器中按表所示投料,发生反应N2(g)+3H2(g)2NH3(g)△H<0,达到平衡时,下列说法错误的是
容器编号 | 容器类型 | 起始物质的量 | 反应物的转化率 | 平时时 | ||
|
|
| ||||
Ⅰ | 恒温恒容 | 1 | 3 | 0 |
|
|
Ⅱ | 绝热恒容 | 0 | 0 | 2 |
| a |
Ⅱ | 恒温恒压 | 1 | 3 | 0 |
| b |
A.平衡时NH3的物质的量:a>1.2,b>1.2
B.容器I、II中平衡常数关系:K(I)>K(II)
C.a1+a2<1
D.若起始时向容器A中充入lmolN2(g)、0.4molH2(g)、0.4molNH3(g),此时平衡向正反应方向移动
【答案】D
【解析】
![]() 绝热恒容时,为NH3反应物,发生反应2NH3(g)N2(g)+3H2(g)△H>0,正反应为吸热反应,温度降低,平衡向生成
绝热恒容时,为NH3反应物,发生反应2NH3(g)N2(g)+3H2(g)△H>0,正反应为吸热反应,温度降低,平衡向生成![]() 的方向移动,a>1.2,反应N2(g)+3H2(g)2NH3(g)为气体体积减小的反应,恒温恒压时,与原平衡相比相当于压强增大,平衡向生成NH3的方向移动,
的方向移动,a>1.2,反应N2(g)+3H2(g)2NH3(g)为气体体积减小的反应,恒温恒压时,与原平衡相比相当于压强增大,平衡向生成NH3的方向移动,
b>1.2,故A正确;
B.平衡常数与温度有关,容器Ⅱ绝热,且反应2NH3(g)N2(g)+3H2(g)△H>0,随反应进行,温度会越来越低,且Ⅱ反应为Ⅰ的逆反应,则容器I、II中平衡常数关系:K(I)>K(II),故B正确;
C.根据A分析,NH3的转化率减小,即容器I中N2的转化率与容器Ⅱ中NH3的转化率之和小于1,故C正确;
D.容器I中反应达到平衡状态时,![]() ,
,![]() ,
,![]() ,化学平衡常数
,化学平衡常数![]() ,若起始时向容器A中充入lmolN2(g)、0.4molH2(g)、0.4molNH3(g),浓度商
,若起始时向容器A中充入lmolN2(g)、0.4molH2(g)、0.4molNH3(g),浓度商![]() ,则该反应向逆反应方向移动,故D错误。
,则该反应向逆反应方向移动,故D错误。
答案选D。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数的值,下列说法中正确的
表示阿伏加德罗常数的值,下列说法中正确的
![]() 一定条件下定容容器中充入
一定条件下定容容器中充入![]() 和
和![]() 发生反应:3
发生反应:3![]() ;
;![]() ,当该反应放出
,当该反应放出![]() 的热量时,容器中的氢分子数共有
的热量时,容器中的氢分子数共有![]()
![]() 常温下,
常温下,![]() 和
和![]() 的混合物中含有的碳原子数为
的混合物中含有的碳原子数为![]()
![]() 硫酸钠固体中含有
硫酸钠固体中含有![]() 个硫酸钠分子;
个硫酸钠分子;
![]() 中含有的质子数、中子数、电子数均为
中含有的质子数、中子数、电子数均为![]()
![]() 标准状况下,
标准状况下,![]() 氯仿中含有
氯仿中含有![]() 键的数目为
键的数目为![]()
![]() 将
将![]() 的
的![]() 溶液滴入沸水中可制得
溶液滴入沸水中可制得![]() 胶粒
胶粒![]() .
.
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用系统命名法给下列有机物命名:
①![]() __;
__;
②(CH3)3COH__;
(2)相对分子质量为114,其一氯代物只有一种的链烃的结构简式__,该物质的名称为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素 A、B、C、D 的原子序数依次增大,B 和 D 同主族,A 和 C 同主族;X、Y、N 分别是由以上四种元素中两种组成的化合物,Z 是由以上三种元素组成的化合物;若 X 与 Y 的摩尔质量相同, Y 为淡黄色固体,N 常温下是液体,上述物质之间的转化关系如图所示(部分生成物省略),则下列说法中一定正确的是( )
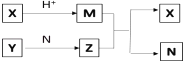
A.相对分子质量M>N,沸点 M>NB.原子半径:D>B>C>A
C.Z 为 NaOHD.M 中含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃下,三种硫酸盐MSO4(M:Pb2+、Ba2+、Sr2+)的沉淀溶解平衡曲线如图所示。已知p(M)=-lgc(M),p(SO42-)=-lgc(SO42-)。下列说法正确的是( )
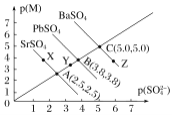
A.溶度积:BaSO4>PbSO4>SrSO4
B.Y点对应的SrSO4是不饱和溶液,能继续溶解SrSO4
C.Z点对应的溶液中c(Ba2+)>c(SO42-),c(Ba2+)·c(SO42-)等于1×10-25
D.BaSO4不可能转化成PbSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
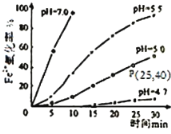
【题目】久置的FeSO4溶液变黄,一般认为是二价铁被氧化为三价铁的缘故。某硏究小组为硏究溶液中Fe2+被O2氧化的过程,查阅资料发现:溶液中Fe2+的氧化过程分为先后两步,首先是Fe2+水解,接着水解产物被O2氧化。于是小组同学决定研究常温下不同pH对Fe2+被O2氧化的影响,并测定了Fe2+氧化率随时间变化的关系,结果如图。
回答下列问题:
(1)写出Fe2+水解的离子方程式___;要抑制FeSO4水解,可以采取的措施是___。
(2)若配制的FeSO4溶液浓度为0.01mol/L,反应过程中溶液体积不变,计算图中P点Fe2+的氧化速率___。
(3)在酸性条件下,Fe2+被O2氧化的反应方程式为:4Fe2++O2+4H+![]() 4Fe3++2H2O,已知常温下该反应的平衡常数很大。则下列说法正确的是___。
4Fe3++2H2O,已知常温下该反应的平衡常数很大。则下列说法正确的是___。
a.Fe2+转化为Fe3+的趋势很大
b.Fe2+转化为Fe3+的速率很大
c.该反应进行得很完全
d.酸性条件下Fe2+不会被氧化
(4)结合图分析不同pH对Fe2+被O2氧化的反应产生了怎样的影响___。
(5)用K2Cr2O7标准溶液測定溶液中Fe2+浓度,从而计算Fe2+的氧化率。反应如下:6Fe2++Cr2O72-+14H+→2Cr3++6Fe3++7H2O,若取20mL待测溶液,用0.0200mol·L1K2Cr2O7标准溶液滴定,消耗标准溶液16.50mL,则溶液中c(Fe2+)=___mol·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行下列实验,相关说法正确的是

A. 图甲:蒸干NH4Cl饱和溶液制备NH4Cl晶体
B. 图乙:形成美丽的红色喷泉,证明HC1极易溶于水
C. 图丙:配制一定物质的量浓度的NaOH溶液,定容时如图则所配NaOH溶液浓度偏低
D. 图丁:所示装置用于除去碳酸氢钠固体中的少量碳酸钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种新型燃料,工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)![]() CH3OH(g) △H1=-116kJ/mol
CH3OH(g) △H1=-116kJ/mol
(1)已知:CO(g)+![]() O2(g)=CO2 (g) △H2=-283kJ/mol
O2(g)=CO2 (g) △H2=-283kJ/mol
H2(g) +![]() O2(g)=H2O (g) △H1=-242kJ/mol
O2(g)=H2O (g) △H1=-242kJ/mol
则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式:________________
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律。如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。

请回答:
①在上述三种温度中,曲线Z对应的温度是_________
②利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)=CH3OH(g)的平衡常数 K=_________。
③下列既能提高上述反应中 CO 的平衡转化率,又能增大反应速率的是____(填标号)。
a.增大压强 b.降低温度 c.增大H2浓度 d.加高效催化剂
④若上述反应在某恒温恒容容器中发生,能说明该反应达到平衡的是____(填标号)。
a.气体平均相对分子质量保持不变 b.△H1保持不变
c.![]() 保持不变 d.气体密度保持不变
保持不变 d.气体密度保持不变
(3)在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol/L)变化如下表所示:
0min | 5min | 10min | |
CO | 0.1 | 0.05 | |
H2 | 0.2 | 0.2 | |
CH3OH | 0 | 0.04 | 0.05 |
若5min~10min只改变了某一条件,所改变的条件是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国西部地区有丰富的盐湖资源,对盐湖矿产资源的综合开发利用是西部大开发的重要课题之一
.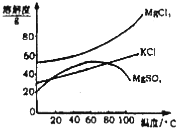
I.某研究性学习小组拟取盐湖苦卤的浓缩液![]() 富含
富含![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等
等![]() ,来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程:
,来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程:
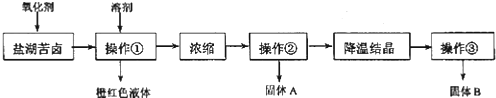
![]() 某同学提出了另一种新方案,对上述操作①后无色溶液进行除杂提纯,无色溶液中先加试剂A,再加试剂B,最后加试剂
某同学提出了另一种新方案,对上述操作①后无色溶液进行除杂提纯,无色溶液中先加试剂A,再加试剂B,最后加试剂![]() 常见的盐
常见的盐![]() ,其方案如下:
,其方案如下:
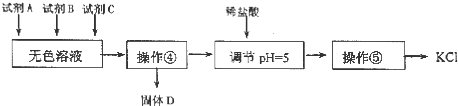
下列说法不正确的是
A.要从橙红色液体中分离出单质溴,可采取的操作是蒸馏
B.操作![]() 为过滤,主要目的是为了除去
为过滤,主要目的是为了除去![]()
C.试剂C为![]() ,固体D主要为
,固体D主要为![]() ,还有少量的
,还有少量的![]()
D.若在操作![]() 结束后发现溶液略有浑浊,应采取的措施是更换滤纸,重新过滤
结束后发现溶液略有浑浊,应采取的措施是更换滤纸,重新过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com