
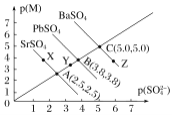
【题目】T℃下,三种硫酸盐MSO4(M:Pb2+、Ba2+、Sr2+)的沉淀溶解平衡曲线如图所示。已知p(M)=-lgc(M),p(SO42-)=-lgc(SO42-)。下列说法正确的是( )
A.溶度积:BaSO4>PbSO4>SrSO4
B.Y点对应的SrSO4是不饱和溶液,能继续溶解SrSO4
C.Z点对应的溶液中c(Ba2+)>c(SO42-),c(Ba2+)·c(SO42-)等于1×10-25
D.BaSO4不可能转化成PbSO4
【答案】B
【解析】
p(M)越大,则c(M)越小。
A. p(M)越大,则c(M)越小,即Pb2+、Ba2+、Sr2+的物质的量浓度越小;同理p(SO42-)越大,c(SO42-)越小。由图可知,p(SO42-)相同时,BaSO4、PbSO4、SrSO4对应的p(M)依次减小,所以三者的溶度积依次增大,即BaSO4<PbSO4<SrSO4,A项错误;
B. 由图可知,Y点对应的SrSO4溶液中c(SO42-)·c(Sr2+)<Ksp(SrSO4),故Y点对应的SrSO4是不饱和溶液,能继续溶解SrSO4,B项正确;
C. 由图可知,Z点对应的溶液中c(Ba2+)>c(SO42-),c(Ba2+)·c(SO42-)=1×10-10,C项错误;
D. 沉淀的转化是可逆的,若向BaSO4悬浊液中加入浓度较大的含Pb2+的溶液, BaSO4能转化成PbSO4,D项错误。
综上所述,说法正确的是B,故选B。


 核心素养学练评系列答案
核心素养学练评系列答案科目:高中化学 来源: 题型:
【题目】氯元素有 2 种稳定的同位素原子,分别可以用 ![]() 和
和![]() 表示,因此氯气分子有 3 种:
表示,因此氯气分子有 3 种:![]() 、
、![]() 、
、![]() 。若氢元素、氧元素分别各有 3 种同位素原子,则形成水分子的种类为( )
。若氢元素、氧元素分别各有 3 种同位素原子,则形成水分子的种类为( )
A.6 种B.9 种C.18 种D.27 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院化学所研制的晶体材料——纳米四氧化三铁,在核磁共振造影及医药上有广泛用途,其生产过程的部分流程如下:
![]()
下列有关叙述不合理的是
A. 纳米四氧化三铁可分散在水中,它与FeCl3溶液的分散质直径相当
B. 纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病
C. 在反应①中环丙胺的作用可能是促进氯化铁水解
D. 反应②的化学方程式是6FeOOH +CO=2Fe3O4+3H2O+CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A在标准状况下的密度为1.25gL﹣1,以A和水煤气(CO、H2)为原料在一定条件 下可获得有机物B、C、D、E,其相互转化关系如图。已知B是CO与H2以物质的量之比为 1:1 反应的产物,E为有浓郁香味、不易溶于水的油状液体。
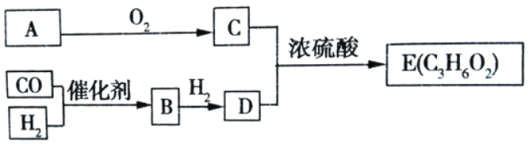
请回答:
(1)有机物C种含有的官能团名称是_____。
(2)C+D→E的反应类型是_____。
(3)有机物B在一定条件下转化为D的化学方程式是_____。
(4)下列说法不正确的是_____。
A.有机物D与金属钠反应比水与金属钠反应要剧烈
B.有机物C、D、E可用饱和碳酸钠溶液鉴别
C.实验室制备E时,浓硫酸主要起氧化作用
D.有机物 B、C均能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g)![]() CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g)![]() 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
A. ①④B. ①②③C. ②③④D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,向三个初始体积为1L的密闭容器中按表所示投料,发生反应N2(g)+3H2(g)2NH3(g)△H<0,达到平衡时,下列说法错误的是
容器编号 | 容器类型 | 起始物质的量 | 反应物的转化率 | 平时时 | ||
|
|
| ||||
Ⅰ | 恒温恒容 | 1 | 3 | 0 |
|
|
Ⅱ | 绝热恒容 | 0 | 0 | 2 |
| a |
Ⅱ | 恒温恒压 | 1 | 3 | 0 |
| b |
A.平衡时NH3的物质的量:a>1.2,b>1.2
B.容器I、II中平衡常数关系:K(I)>K(II)
C.a1+a2<1
D.若起始时向容器A中充入lmolN2(g)、0.4molH2(g)、0.4molNH3(g),此时平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各![]() 充入10L恒容密闭容器中,发生反应
充入10L恒容密闭容器中,发生反应![]() ,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法正确的是
,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法正确的是![]()
| 2 | 4 | 7 | 9 |
|
|
|
|
|
A.8min时,其他条件不变,若增大X的浓度,则反应速率加快,活化分子百分数增加
B.该温度下此反应的平衡常数![]()
C.其他条件不变,降低温度,反应达到新平衡前![]() 逆
逆![]() 正
正![]()
D.其他条件不变,再充入![]() ,平衡时X的体积分数增大
,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物的性质,设计如下实验。请回答下列问题:

(1)装置b的名称______________;按如图所示装置进行实验(夹持装置及尾气处理装置未画出)。实验过程中,装置B中观察到的现象是________________;装置C中有白色沉淀生成,该沉淀是____(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:_______________________________。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置(最简单)连接A装置中c处管口,从左到右的顺序为_____________________(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是_____________________________。



碱石灰① 品红溶液② 高锰酸钾溶液③ 澄清石灰水④
(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是____________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容条件下,不是可逆反应2A(g)+3B(s)![]() 2C(g)达到平衡标志的是( )
2C(g)达到平衡标志的是( )
①C的生成速率与C的分解速率相等;②单位时间生成amol A,同时消耗1.5amol B;③各组分的浓度不再变化;④混合气体的密度不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦混合气体的平均摩尔质量不再变化;⑧A、B、C的分子数目比为2:3:2。
A.②⑤⑧ B.⑤⑥⑧ C.①③④ D.②④⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com