硫及其化合物在化学工业中应用非常广泛.
(1)汽车尾气中主要含有CO、NO
2、SO
2、CO
2气体,其中
NO2
NO2
能导致光化学烟雾的形成;
目前采用的是在汽车排气装置中安装一个净化器,可以有效的将尾气中的有害气体转化.
如:CO(g)+NO
2(g)?NO(g)+CO
2(g)△H=-akJ?mol
-1(a>0)
2CO(g)+2NO(g)?N
2(g)+2CO
2(g)△H=-bkJ?mol
-1(b>0)
则用标准状况下的3.36L CO还原NO
2至N
2(CO完全反应)的整个过程中放出的热量为
kJ(用含有a和b的代数式表示).
(2)工业上生产硫酸时,将SO
2氧化为SO
3是关键一步.
①某温度下,已知2SO
2(g)+O
2(g)?2SO
3(g),△H=-196kJ?mol
-1.开始时在10L的密闭容器中加入4.0mol SO
2(g)和5.0mol O
2(g),5分钟后反应达到平衡,共放出热量196kJ,该温度下此反应的平衡常数K=
2.5mol-1?L
2.5mol-1?L
,用O
2表示的反应速率为
0.02mol?L-1?min-1
0.02mol?L-1?min-1
.
②一定条件下,向一带活塞的密闭容器中充入2mol SO
2和1molO
2,发生下列反应:2SO
2(g)+O
2(g)?2SO
3(g),达到平衡后改变下述条件,SO
2、O
2、SO
3气体平衡浓度都比原来增大的是
AE
AE
(填字母).
A.保持温度和容器体积不变,充入2mol SO
3B.保持温度和容器体积不变,充入2mol N
2C.保持温度和容器内压强不变,充入1mol SO
3D.升高温度
E.移动活塞压缩气体
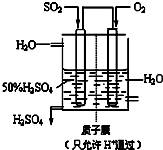
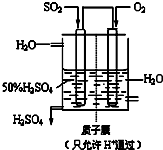
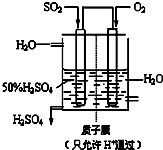
(3)某人设想以右图所示装置用电化学原理生产硫酸,写出通入SO
2的电极的电极反应式
SO2+2H2O=SO42-+4H++2e-
SO2+2H2O=SO42-+4H++2e-
.




 硫及其化合物在自然界中广泛存在,运用相关原理回答下列问题:
硫及其化合物在自然界中广泛存在,运用相关原理回答下列问题: