
����Ŀ���±���Ԫ�����ڱ����һ���֣����������Ԫ���Լ���Ӧ�������ش��й����⣺
���� ���� | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
1 | �� | ||||||
2 | �� | �� | �� | �� | |||
3 | �� | �� | �� | �� | |||
4 | �� |
��1��д���ɢٺ͢�����Ԫ����ɵIJ�������������ʵĻ�ѧʽ��________��_______��
��2����~���Ԫ��������������Ӧ��ˮ����������ǿ����Ļ�ѧʽΪ��_______��
��3���������������Ӧ��ˮ������������������ڼ��ȵ������������κ�ˮ�Ļ�ѧ����ʽΪ��___________________________________________________________��
��4�����ݵĵ���ͨ��ܵij����⻯���У���Ӧ���ң���Ӧ�Ļ�ѧ����ʽΪ��________��
��5����ͬ�����¢ݢޢߢ�����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳���ǣ�________________��
���𰸡�NH3 N2H4 HClO4 Ca��OH��2+ SiO2![]() CaSiO3 + H2O 2F2+2H2O=4HF+O2 r(Na)>r(Al)>r(Si)>r(F)
CaSiO3 + H2O 2F2+2H2O=4HF+O2 r(Na)>r(Al)>r(Si)>r(F)
��������
��Ԫ�������ڱ���λ�ÿ�֪����ΪHԪ�ء���ΪCԪ�ء���ΪNԪ�ء���ΪOԪ�ء���ΪFԪ�ء���ΪNaԪ�ء���ΪAlԪ�ء���ΪSiԪ�ء���ΪClԪ�ء���ΪCaԪ�ء�
��1����ΪHԪ�ء���ΪNԪ�أ�HԪ�غ�NԪ�ؿ�����ɵķ���ΪNH3��N2H4��
��2��10��Ԫ����ClԪ������������Ӧ��ˮ����HClO4��������ǿ���ʴ�Ϊ��HClO4��
��3���������������Ӧ��ˮ����ΪCa��OH��2��������������ΪSiO2��Ca��OH��2��SiO2�ڼ��ȵ����������ɹ���ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪCa��OH��2+ SiO2![]() CaSiO3 + H2O���ʴ�Ϊ��Ca��OH��2+ SiO2
CaSiO3 + H2O���ʴ�Ϊ��Ca��OH��2+ SiO2![]() CaSiO3 + H2O��
CaSiO3 + H2O��
��4����ΪOԪ�ء���ΪFԪ�أ�F2��H2O�����û���Ӧ����HF��O2����Ӧ�Ļ�ѧ����ʽΪ2F2+2H2O=4HF+O2���ʴ�Ϊ��2F2+2H2O=4HF+O2��
��5����ΪFԪ�ء���ΪNaԪ�ء���ΪAlԪ�ء���ΪSiԪ�أ�ͬ����Ԫ�ش����ң�ԭ�Ӱ뾶��С��ͬ����Ԫ�����϶��£�ԭ�Ӱ뾶������ԭ�Ӱ뾶�Ĵ�С˳��Ϊr(Na)>r(Al)>r(Si)>r(F)���ʴ�Ϊ��r(Na)>r(Al)>r(Si)>r(F)��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(Na2FeO4)��һ������Ч��ܾ�ˮ�������ŨNaOH��Һ�Ʊ��������Ƶ�װ����ͼ����ʾ������˵������ȷ����(����)

A. XΪ��Դ���������缫�����ĵ缫��Ӧʽ�ǣ�Fe - 6e- + 8OH- = FeO42- + 4H2O
B. ���ӽ���ĤΪ�����ӽ���Ĥ
C. ������1.66 gNa2FeO4ʱ���ռ����������ڱ�״���µ������672 mL
D. NaOH��Һ�ij�ʼŨ����������ɵ�Na2FeO4Ũ�ȵı仯��ϵ��ͼ����ʾ��c(Na2FeO4)���͵�ԭ������Ƿ����˸���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������ʳ������Ӫ���DZ�֤���彡����������������Ҫ;����
����������Ԫ�����벻���Ӱ�����������������������������ܴﵽĿ�ĵ���______��
a����������ʳ�üӵ��� b����������ʹ����ǿ������ c��������������������
����������8�ְ��������ͨ��ʳ�����룬ijƷ�Ʊ��ɺ��е�������������ת��Ϊ���������______��
a����ά�� b�������� c����֬
��������ʷ������Ҫ�Ŀ�������______��
a����ù�� b��ά���� c�����ܲ���
��2������������Ȼ�ĺ�г��Ӫ�찲ȫ����̬�����ѳ�Ϊȫ����Ĺ�ʶ��
����ͼ������ֻ250mL����ƿ�зֱ����CO2�Ϳ������ð׳��������һ��ʱ�������aƿ���¶ȼƶ����Եͣ���ʢ��CO2����ƿΪ______���a����b������
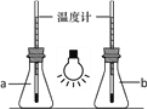
��Ϊ��ֹ��ɫ��Ⱦ���Ͼɵ�������Ͷ�뵽������ͼ��־������Ͱ�ڣ��ñ�־��ʾ����______��

�۷�ˮ����(Tl)���и߶��ԣ�����ʱ������NaClO��Һ����Tl+ת��ΪTl3+��NaClO��_____�������������ԭ��������ͬʱ����������ˮ����Tl3+ת��Ϊ������Tl(OH)3��д������Tl(OH)3�����ӷ���ʽ______��
��3��������������ᷢչ�����ʻ��������Ͽ�ѧ�ķ�չ�벻����ѧ��
��������մɵ�����ԭ�ϣ����н������˵ĸ������Ǻ������ʽ��ٵĸ�Ʒ�����������Ҫ��ɿɱ�ʾΪAl2Si2Ox(OH)4����x=______��
��2016����˻��ڰ������У����ݵĽ���������Ľ������ϡ���������ˮ�ࡢ������ͬ��ԭ����______�������ƣ��������ڵ�����ͨ���ø��ܶȾ���ϩ��HDPE��Ϊԭ���Ƶã�����ϩ����______���ϣ���ȹ��ԡ��������ԡ�������ϩ���ϳ�����ʳƷ��װ������ϩ�Ľṹ��ʽΪ_________����
�ۻ�ͨ��·�������ڻ����ƽ���������η�ֹ����ĸ�ʴ�ǹ��̼�����Ա���˵�����֮һ�����ڷ����绯ѧ��ʴʱ�ĸ�����Ӧ����ʽΪ______��
�ܹ�ҵ�ϳ���SiCl4��O2�ڸ���������ͨ���û���Ӧ�Ƶ�SiO2������2000�������ɹ���ϸ˿���÷�Ӧ�Ļ�ѧ����ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��� 0��01 mol��L��1NaOH��Һ�ζ� 20��00 mL 0��01 mol��L��1CH3COOH��Һ�����õζ�������ͼ������˵����ȷ����
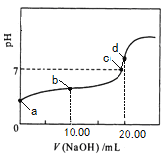
A. a���Ӧ��Һ��pH=2
B. b���Ӧ����Һ�У�c(OH��)+ c(CH3COO��) = c(Na+)+ c(H+)
C. c���ʾNaOH��Һ��CH3COOH��Һǡ����ȫ��Ӧ
D. d���Ӧ����Һ�У�ˮ�ĵ���̶�С��ͬ���´�ˮ�ĵ���̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�Ϊ��ʽ���ڱ���һ���֣����еı�Ŵ�����Ӧ��Ԫ�ء�

��ش��������⣺
��1��Ԫ�����Ļ�̬ԭ�ӵļ۵����Ų�ʽΪ_________________��
��2����10��Ԫ�أ����е縺��������________(��Ԫ�ط���)��
��3��Ԫ�آڵ�һ���⻯��(�����к���6��ԭ��)����Ҫ�Ļ���ԭ�ϣ����Ѹ��⻯��IJ�����Ϊ����ʯ�ͻ�����չˮƽ�ı�־���йظ��⻯����ӵ�˵����ȷ����________��
A.6��ԭ�Ӳ���ͬһƽ���� B.���ں��м��Լ��ķǼ��Է���
C.ֻ����4��sp2-s�Ħļ���1��P-P�Ħм� D.���⻯�������Cԭ�Ӳ���sp2�ӻ�
��4����ͼ��ʾΪѪ�쵰�ͼ��쵰�Ļ��Բ���(Ѫ����)�Ľṹʽ���˽ṹƬ���к��еĻ�ѧ����________(�����)��

A.���Ӽ� B.������ C.���Լ� D.�Ǽ��Լ� E.��λ�� G. �ļ� H.أ��
��5���±�Ϊԭ��������������Ķ�����Ԫ��A~F�ĵ�һ��������������ݡ�

��ش𣺱��е�D��E��F������������Ԫ��__________(��Ԫ�ط���)����A��B��CΪԭ���������������ͬ��������Ԫ�أ�������ʾB��A��C�ĵ�һ�����ܶ��Դ���ԭ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����Ϊ̽������Ũ����(����)�ķ�Ӧ,����֤SO2������,�����ͼ��ʾװ�ý���ʵ��,����˵������ȷ����(����)

A. װ��C�в�������ɫ�ij���,������SO2��������
B. װ��E������������δ��Ӧ��SO2����ֹ��Ⱦ����
C. װ��D��Ʒ����Һ��ɫ������ֱ��ɫ������֤SO2����ˮ������
D. ʵ��ʱ������a����Ũ������,�ɷ�ֹװ��B�е���Һ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��A��B��C��D���Ƕ�����Ԫ�أ�AԪ��ԭ�ӵ�2p����Ͻ�������δ�ɶԵ��ӣ�B��3p������пչ����A��Bͬ���壬B��Cͬ���ڣ�C��ͬ�����е縺�����ģ�D����̬�⻯���ˮ��Һ��ʹ��ɫ��̪��Һ��졣�Իش�
��1��A�ļ۵��ӹ���Ų�ͼΪ ______________________________ ��B�ĵ����Ų�ʽΪ _________ ��C�ļ۵����Ų�ʽΪ ____________ ��D��ԭ�ӽṹʾ��ͼΪ __________ ��
��2����֪D��Hԭ�����γ�һ�ָ������ķ���D2H2������Dԭ������8���ӽṹ��������÷��ӵĵ���ʽΪ _____________������ _____�������� _____ ��������
��3��B��ԭ�Ӻ�������˶�״̬________�ж����֣�ԭ�ӹ����Ϊ______���ܼ���__________������ռ�ݵ�����ܲ����Ϊ_________��
��4������Ԫ�����������ˮ����������ǿ�������ǣ��ö�Ӧ��ѧʽ�ش�____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ����ȷ���ǣ�������
A. 4g��������ȫȼ������SO2���ų�37 kJ������S(s)+O2(g)=SO2(g) ��H= -296kJ/mol
B. 1molN2��3molH2��ij�ܱ������з�Ӧ�ų�73kJ��������Ӧ���Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)![]() 2NH3(g) ��H= -73kJ/mol
2NH3(g) ��H= -73kJ/mol
C. ����ı�ȼ����Ϊ-890.3kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)+2O2(g) ==CO2(g)+ 2H2O(g) ��H=-890.3kJ��mol-1
D. ǿ��ǿ����к���Ϊ- 57.3 kJ/mol��Ba(OH) 2(aq)+H2SO4(aq)=BaSO4(S)+2H2O(l) ��H=-114.6kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��ֽ���ұ�������У������Ƶ���Ӧ��������
A. ����������B. �����������۸��¹���
C. ��������Ȼ���D. ��������̼���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com