
【题目】下列有关糖类的说法,错误的是( )
A.糖类由碳、氢、氧三种元素组成
B.糖类是人类食物的重要成分之一
C.在人类食物所提供的总能量中大约有75%来自糖类
D.淀粉在人体内经酶的催化作用,与水发生一系列反应,最终变为蔗糖
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是( )
编号 | 金属(粉末状) | 酸的浓度 | 酸的体积 | 反应温度 |
A | 0.1molMg | 6mol/L硝酸 | 10mL | 60℃ |
B | 0.1molMg | 3mol/L盐酸 | 10mL | 60℃ |
C | 0.1molFe | 3mol/L盐酸 | 10mL | 60℃ |
D | 0.1molMg | 3mol/L盐酸 | 10mL | 30℃ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.反应中,被氧化的物质是氧化剂
B.氧化还原反应的本质是电子的转移
C.某物质的元素在反应中失去电子,则此物质是氧化剂
D.氧化还原反应中,一种元素被氧化一定有另一种元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的碱性溶液中能大量共存的离子组是
A.Fe3+、Na+、Cl-、HCO3-B.K+、Na+、NO3-、CO32-
C.Mg 2+、H+、NO3-、SO42-D.K+、MnO4-、Na+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿制高锰酸钾的流程如下:
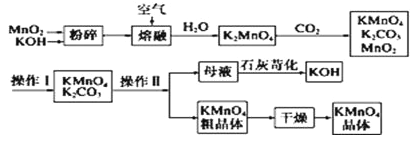
请回答下列问题:
(1)MnO2和KOH在熔融前粉碎的目的是_____________________________________________。
(2)写出二氧化锰和氢氧化钾熔融物中通入空气时发生的主要反应的化学方程式___________。
(3)通入CO2后,生成的KMnO4与MnO2的物质的量之比为___________。
(4)上述流程中可以循环使用的物质有___________、___________(填化学式)。
(5)已知:常温下,Ksp[Mn(OH)2]=2.4×10-13工业上,调节pH可以沉淀废水中Mn2+,当pH=10时,溶液中c(Mn2+)=___________mol/L。
(6)操作Ⅰ的名称是___________,操作Ⅱ根据下表KMnO4和K2CO3两物质在溶解性上的差异,采用___________、___________(填操作步骤)得到KMnO4粗晶体。
| 10 | 20 | 30 | 40 | 60 |
K2CO3 | 109.0 | 111.0 | 114.0 | 117.0 | 126.0 |
KMnO4 | 4.3 | 6.3 | 9.0 | 12.6 | 22.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.在共价化合物中不可能含有离子键
B.阴阳离子之间通过静电引力形成的化学键,叫离子键
C.含有共价键的化合物一定是共价化合物
D.含有离子键的化合物不一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】没有水,人体内大部分化学反应就无法进行,这说明 ( )
A.水在生物体内可以流动
B.生物体内的生化反应必须在水中进行
C.水是细胞内含量最多的化合物
D.水具有缓和温度变化的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
I.污染物SO2、NO2经O2预处理后用CaSO3悬浊液吸收,可减少尾气中SO2、NOx的含量。
T℃时,O2氧化烟气中SO2、NOx的主要反应的热化学方程式为:

(1)T℃时,反应3NO(g)+O3(g) ![]() 3NO2(g)的△H=_______________kJ.mol-1。
3NO2(g)的△H=_______________kJ.mol-1。
(2)T℃时,将0.6molNO和0.2molO3气体充入到2L固定容积的恒温密闭容器中,NO的浓度随反应时间的变化如图1所示。
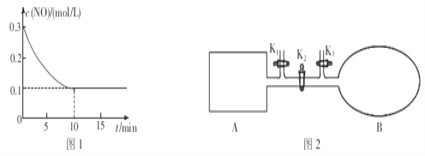
①T℃时,反应3NO(g)+O3(g)![]() 3NO2(g)的平衡常数K=______________。
3NO2(g)的平衡常数K=______________。
②不能说明反应达到平衡状态的是______________。
A.气体颜色不再改变 B.气体的平均摩尔质量不再改变
C.气体的密度不再改变 D.单位时间内生成O3和NO2物质的量之比为1:3
II.NO2的二聚体N2O4是火箭中常用氧化剂。完成下列问题:
(3)如图2所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊。关闭K2,将各1 molNO2通过K1、K3分别充入真空A、B中,反应起始时A、B的体积相同均为aL(忽略导管中的气体体积)。
①若容器A中到达平衡所需时间ts,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)=________________。
②若打开K2,平衡后B容器的体积缩至0.4aL,则打开K2之前,气球B体积为__________L。
③若平衡后在A容器中再充入0.5molN2O4,则重新到达平衡后,平衡混合气中NO2的体积分数______________(填“变大”“变小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com