
����Ŀ�����ǻ������ᶡ�����׳��Ჴ���������������������Խ�ĸ��ù���к�ǿ���������ã���ҵ�ϳ��ö��ǻ��������붡����Ũ������½���������Ӧ���Ƶã�������ij�����鿪���Ĵ����ۡ��õĻ���ԭ�ϳ����Ʊ����ǻ������ᶡ���ĺϳ�·�ߣ�
��ͨ����ͬһ��̼ԭ�������������ǻ����ȶ�������ˮ�γ��ʻ���
��D����������Һ��Ӧ����������
��F�ĺ˴Ź������ױ����������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊl��1��

���������⣺
��1��A�Ļ�ѧ����Ϊ ��
��2����B����C�Ļ�ѧ��Ӧ����ʽΪ ��
�÷�Ӧ������Ϊ ��
��3��D�Ľṹ��ʽΪ ��
��4��F�ķ���ʽΪ ��
��5��G�Ľṹ��ʽΪ ��
��6��E��ͬ���칹���к��б������ܷ���������Ӧ�Ĺ����֣����к˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ2��2��1���� ��д�ṹ��ʽ����
���𰸡���1���ױ���
��2�� ��ȡ����Ӧ��
��ȡ����Ӧ��
��3��![]() ��
��
��4��C7H4O3Na2��
��5��![]() ��
��
��6��13��![]() ��
��
�������������������A�ķ���ʽΪC7H8�����պϳɶ��ǻ������ᶡ����֪��AΪ�ױ�![]() ���ױ����������������£���������λ�ϵ�Hԭ������������ȡ����Ӧ����B��BΪ
���ױ����������������£���������λ�ϵ�Hԭ������������ȡ����Ӧ����B��BΪ![]() �������Ϣ����֪��D�к���ȩ����B�ڹ��������£����ϵ�Hԭ������������ȡ����Ӧ����C��CΪ
�������Ϣ����֪��D�к���ȩ����B�ڹ��������£����ϵ�Hԭ������������ȡ����Ӧ����C��CΪ![]() ��C����������ˮ��Һ�У����ϵ���ԭ�ӷ���ȡ����Ӧ������D�������Ϣ����֪��DΪ
��C����������ˮ��Һ�У����ϵ���ԭ�ӷ���ȡ����Ӧ������D�������Ϣ����֪��DΪ![]() ��D�ڴ���������ȩ������������E��EΪ
��D�ڴ���������ȩ������������E��EΪ![]() ��E�ڼ��Ը��¸�ѹ�����£������Ϣ����֪�������ϵ�Clԭ�ӱ�ȡ������F��ͬʱ����������Ӧ��FΪ
��E�ڼ��Ը��¸�ѹ�����£������Ϣ����֪�������ϵ�Clԭ�ӱ�ȡ������F��ͬʱ����������Ӧ��FΪ![]() ��F�ữ���ɶ��ǻ�������G��
��F�ữ���ɶ��ǻ�������G��![]() �����ݴ˽��
�����ݴ˽��
�⣺��A�ķ���ʽΪC7H8�����պϳɶ��ǻ������ᶡ����֪��AΪ�ױ�![]() ���ױ����������������£���������λ�ϵ�Hԭ������������ȡ����Ӧ����B��BΪ
���ױ����������������£���������λ�ϵ�Hԭ������������ȡ����Ӧ����B��BΪ![]() �������Ϣ����֪��D�к���ȩ����B�ڹ��������£����ϵ�Hԭ������������ȡ����Ӧ����C��CΪ
�������Ϣ����֪��D�к���ȩ����B�ڹ��������£����ϵ�Hԭ������������ȡ����Ӧ����C��CΪ![]() ��C����������ˮ��Һ�У����ϵ���ԭ�ӷ���ȡ����Ӧ������D�������Ϣ����֪��DΪ
��C����������ˮ��Һ�У����ϵ���ԭ�ӷ���ȡ����Ӧ������D�������Ϣ����֪��DΪ![]() ��D�ڴ���������ȩ������������E��EΪ
��D�ڴ���������ȩ������������E��EΪ![]() ��E�ڼ��Ը��¸�ѹ�����£������Ϣ����֪�������ϵ�Clԭ�ӱ�ȡ������F��ͬʱ����������Ӧ��FΪ
��E�ڼ��Ը��¸�ѹ�����£������Ϣ����֪�������ϵ�Clԭ�ӱ�ȡ������F��ͬʱ����������Ӧ��FΪ![]() ��F�ữ���ɶ��ǻ�������G��
��F�ữ���ɶ��ǻ�������G��![]() ����
����
��1��������������֪��AΪ![]() ����ѧ����Ϊ�ױ����ʴ�Ϊ���ױ���
����ѧ����Ϊ�ױ����ʴ�Ϊ���ױ���
��2����B����C��![]() �ڹ��������£����ϵ�Hԭ������������ȡ����Ӧ����
�ڹ��������£����ϵ�Hԭ������������ȡ����Ӧ����![]() ����Ӧ�Ļ�ѧ��Ӧ����ʽΪΪ��
����Ӧ�Ļ�ѧ��Ӧ����ʽΪΪ�� ��
��
�ʴ�Ϊ�� ��ȡ����Ӧ��
��ȡ����Ӧ��
��3��D�Ľṹ��ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
��4��������������֪��FΪ![]() �������ʽΪC7H4O3Na2��
�������ʽΪC7H4O3Na2��
�ʴ�Ϊ��C7H4O3Na2��
��5��������������֪��G�Ľṹ��ʽΪ![]() ��
��
�ʴ�Ϊ��![]() ��
��
��6��EΪ![]() ��ͬ���칹���к��б������ܷ���������Ӧ��˵������ȩ���������������E��ͬ���칹����������ʽ��һ���DZ����Ϻ���һ��������һ����ԭ�ӣ��ڡ��䡢�ԣ���3���칹����һ������һ��ȩ����һ���ǻ���һ����ԭ�ӣ���3�ֲ�ͬ��ȡ��������10��ͬ���칹�壬���Թ�����13�֣��˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ2��2��1��Ϊ
��ͬ���칹���к��б������ܷ���������Ӧ��˵������ȩ���������������E��ͬ���칹����������ʽ��һ���DZ����Ϻ���һ��������һ����ԭ�ӣ��ڡ��䡢�ԣ���3���칹����һ������һ��ȩ����һ���ǻ���һ����ԭ�ӣ���3�ֲ�ͬ��ȡ��������10��ͬ���칹�壬���Թ�����13�֣��˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ2��2��1��Ϊ![]() ���ʴ�Ϊ��13��
���ʴ�Ϊ��13��![]() ��
��


 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ������Ҫ�Ľ������ϡ�ˮ�����ϵ���Ҫ�ɷ�ΪCaO��SiO2��������һ��������������þ�Ƚ����������ʵ���Ҳⶨˮ����Ʒ�иƺ����Ĺ�����ͼ��ʾ��

�ش��������⣺
��1���ڷֽ�ˮ����Ʒ�����У�������Ϊ�ܼ����Ȼ��Ϊ���ܼ���������뼸�����ᡣ���������Ŀ����__________������ʹ��___________�������ᡣ
��2������A����Ҫ�ɷ���_________���䲻����ǿ�ᵫ����һ�����ᷴӦ���÷�Ӧ�Ļ�ѧ����ʽΪ____________________________________��
��3���Ӱ�ˮ�����м��ȵ�Ŀ����___________������B����Ҫ�ɷ�Ϊ_____________��____________���ѧʽ����
��4������Ƴ�����ϡH2SO4��������KMnO4����Һ�ζ���ͨ���ⶨ��������ɼ�ӻ�֪�Ƶĺ������ζ���ӦΪ�� ![]() +H++H2C2O4��Mn2++CO2+H2O��ʵ���г�ȡ0.400 gˮ����Ʒ���ζ�ʱ������0.0500 mol��L-1��KMnO4��Һ36.00 mL�����ˮ����Ʒ�иƵ���������Ϊ______________��
+H++H2C2O4��Mn2++CO2+H2O��ʵ���г�ȡ0.400 gˮ����Ʒ���ζ�ʱ������0.0500 mol��L-1��KMnO4��Һ36.00 mL�����ˮ����Ʒ�иƵ���������Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ��(ҩƷ���и�����������Ҷ��Ƭ)��һ������ȱ����ƶѪ��ҩ������Ҫ�ɷ�������������Ҷ�����ɽ�ĸ�����顢���Ρ������ȣ������Dzⶨ��Դ����������������������ʵ����ȡ10Ƭ������������Ƭ(ÿƬa����)�гɷ�ĩ����ˮ�ܽ⣬����,�ٽ���Һ���100mL��Һ��ȡ��25mL��˫��ˮ��Ӧ(����Ҷ�ᡢ�ɽ�ĸ�����顢���Ρ�����������˫��ˮ��Ӧ)��
��1������һ��Ũ�ȵ�˫��ˮ��Һ����������30%���ܶ�1.1g/cm3��˫��ˮ����1.0mol/L��˫��ˮ100mL,��30%˫��ˮ���ʵ���Ũ��Ϊ_______(����һλС��),����������ȡ30%��˫��ˮ_________mL��
��2������1.0mol/L��˫��ˮ100mLʱ������ʵ������10mL������15mL����С�ձ�������������ͷ�ιܡ���Һ©���в���Ҫ�õ���________��_______����ȱ�ٵ�ʵ��������________��
��3����ʵ�������������½���,��ʵ����Ƶķ�Ӧԭ����___________(�����ӷ���ʽ��ʾ)��
��4��������ʵ������1.0mol/L��˫��ˮbmL����ÿƬ������������Ҷ��Ƭ��������������������Ϊ________(�ú�a��b��ʽ�ӱ�ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������������Һ[KAl(SO4)2]�������Ũ�Ȼ�ϡ��û����Һ��SO42-Ũ��Ϊ0.4mol/L��ȡ100mL���Һ����0.4mol/L��KOH��Һ����Ҫ�����ij�����������Ũ�ȵ�KOH�������( )
A. 100mL B. 150mL C. 200mL D. 250mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��2-��������������Ϳ����������Ӽ�����ʵ�����п�������ͼ��ʾװ���Ʊ�1��2-�������飮����A��F��װ���Ҵ���Ũ����Ļ��Һ��D�е��Թ���װ��Һ�壮���ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ�������l40����ˮ�������ѡ����г�װ������ȥ��
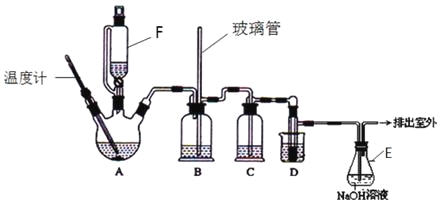
�й������б����£�
�Ҵ� | 1,2-�������� | ���� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶȣ�g�� cm-3 | 0.79 | 2.2 | 0.71 |
�е㣯�� | 78.5 | 132 | 34.6 |
�۵㣯�� | һl30 | 9 | -1l6 |
��д���пհף�
��1��A����Ҫ���������Ҵ�����ˮ��Ӧ������ȥ��Ӧ������д���Ҵ��������ȥ��Ӧ�Ļ�ѧ����ʽ�� ��
D�з�����Ӧ�Ļ�ѧ����ʽΪ�� ��
��2����ȫƿB���Է�ֹ�����������Լ��ʵ�����ʱ�����Ƿ�����������д����������ʱƿB�е����� ��
��3����װ��C��Ӧ���� ����Ŀ�������շ�Ӧ�п������ɵ��������壺������ȷѡ��ǰ����ĸ��
a��ˮ b��Ũ���� c������������Һ d������̼��������Һ
��4������E��NaOH��Һ�������� ��
��5�������������������������ѣ�����________����������ƣ��ķ�����ȥ��
��6����Ӧ������Ӧ����ˮ��ȴװ��D������ҪĿ������ϩ���巴Ӧʱ���ȣ���ȴ�ɱ�����Ĵ����ӷ������ֲ��ܹ�����ȴ�����ñ�ˮ������ԭ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����KMnO4������������Ϊ36.5%�����ᣨ��������Һ�ܶ�Ϊ1.19g/cm3������Ӧ����ʽ���£�2KMnO4+16HCl=2KCl+2MnCl2+5 Cl2��+8H2O
��1��31.6gKMnO4��ʹ���ٿ�HCl�������������������ڱ�״���µ����Ϊ��������
��2������10mL36.5%��������Һϡ�͵�100mL����ϡ�ͺ��������Һ�����ʵ���Ũ��Ϊ����mol/L?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������
A. ��![]() ��Ϊͬ���칹��ķ����廯������6��
��Ϊͬ���칹��ķ����廯������6��
B. ����5��̼ԭ�ӵ�ij������������һ��ȡ����Ľṹ������3��
C. �ױ������ϵ�һ����ԭ�ӱ���3��̼ԭ�ӵ����ȡ�����õ��Ľṹ������6��
D. �ƵĽṹ��ʽΪ ���������ᷴӦ��������5��һ����ȡ����
���������ᷴӦ��������5��һ����ȡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������·����������л���Ӧ����ѧ��Ӧ������ȫ��ͬ����
A. �Ҵ���Ũ����ֱ���170���140��������·�Ӧ
B. ������ֱ���NaOH��ˮ��Һ��NaOH�Ĵ���Һ�з�Ӧ
C. ����ϩ�ƾ�����ϩ�����ᣨ![]() ���ϳɾ�����
���ϳɾ�����
D. �Ҵ�ʹ�����ظ������Һ��ɫ����ȩ������������ͭ����Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���ԭ��������ʾ������Ԫ��֮������γ����ӻ��������( )
A. 1��7 B. 13��17 C. 8��16 D. 9��15
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com