
【题目】下列叙述错误的是
A. 与![]() 互为同分异构体的芳香族化合物有6种
互为同分异构体的芳香族化合物有6种
B. 含有5个碳原子的某饱和链烃,其一氯取代物的结构可能有3种
C. 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,得到的结构可能有6种
D. 菲的结构简式为 ,它与硝酸反应,可生成5种一硝基取代物
,它与硝酸反应,可生成5种一硝基取代物
【答案】A
【解析】A、![]() 分子式为C7H8O,其同分异构体为芳香族化合物,含有苯环,侧链为甲基、羟基,有邻、间、对三种,侧链还可以为-CH2OH、-OCH3,有如下结构:
分子式为C7H8O,其同分异构体为芳香族化合物,含有苯环,侧链为甲基、羟基,有邻、间、对三种,侧链还可以为-CH2OH、-OCH3,有如下结构: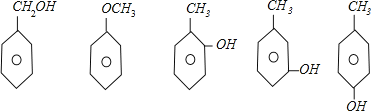 ,A错误;B、含有5个碳原子的饱和链烃为C5H12,有正戊烷、异戊烷、新戊烷,正戊烷中有3种H原子,异戊烷中有4种H原子,新戊烷中有1种H原子,B正确;C、含有3个碳原子的烷基为丙基、异丙基两种,甲苯苯环上有3种氢原子,分别处于甲基的邻、间、对位位置上,所以甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,同分异构体最多有3×2=6种,C正确;D、菲为对称结构,有如图所示的5种H原子
,A错误;B、含有5个碳原子的饱和链烃为C5H12,有正戊烷、异戊烷、新戊烷,正戊烷中有3种H原子,异戊烷中有4种H原子,新戊烷中有1种H原子,B正确;C、含有3个碳原子的烷基为丙基、异丙基两种,甲苯苯环上有3种氢原子,分别处于甲基的邻、间、对位位置上,所以甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,同分异构体最多有3×2=6种,C正确;D、菲为对称结构,有如图所示的5种H原子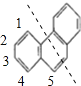 ,所以与硝酸反应,可生成5种一硝基取代物,D正确,答案选A。
,所以与硝酸反应,可生成5种一硝基取代物,D正确,答案选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)N、H两元素按原子数目比l∶3和2∶4构成分子A和B,A的中心原子的杂化方式是________,A的电子式为____________,B的结构式为____________。
(2)NO3-的空间构型为________ ;写出NO3-互为等电子体的一种分子的化学式______。
(3)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心,该化合物化学式为______,每个Ba2+与_____个O2-配位。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时V2O5转化为VO![]() ,反应的离子方程式为______________,同时V2O4转化成VO2+。“废渣1”的主要成分是________。
,反应的离子方程式为______________,同时V2O4转化成VO2+。“废渣1”的主要成分是________。
(2)“氧化”中欲使3 mol的VO2+变为VO![]() ,则需要氧化剂KClO3至少为________mol。
,则需要氧化剂KClO3至少为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对羟基苯甲酸丁酯(俗称尼泊金丁酯)可用作防腐剂,对酵母和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得.出下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基;
②D可与银氨溶液反应生成银镜;
③F的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为l:1.

答下列问题:
(1)A的化学名称为 ;
(2)由B生成C的化学反应方程式为 ;
该反应的类型为 ;
(3)D的结构简式为 ;
(4)F的分子式为 ;
(5)G的结构简式为 ;
(6)E的同分异构体中含有苯环且能发生银镜反应的共有种,其中核磁共振氢谱有三种不同化学环境的氢,且峰面积比为2:2:1的是 (写结构简式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的水溶液呈现黄色,A、B、C、D之间有如图所示转化关系。

(1)A是________________(填写相关物质的化学式);
(2)C溶液与NaOH溶液混合后产生的现象____________________;
(3)①的反应类型:______(选填“化合”、“分解”、“置换”、“复分解”) ;
(4)某待测液中既有B中阳离子,又有C中阳离子。
检验待测液中有C中阳离子的方法:___________________________;
检验待测液中有B中阳离子的方法:__________________________;
(5)写出D![]() E的反应方程式:______________________。
E的反应方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表达下列反应的离子方程式为
A. 用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B. 硫化亚铁与浓硫酸混合加热:2H++FeS=H2S↑+ Fe2+
C. 向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3![]() =Al2(CO3)3↓
=Al2(CO3)3↓
D. 用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH-=![]() +
+![]() + H2O
+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学帮助水质检测站配制490 mL 0.5 mol L-1NaOH溶液以备使用。
(1)该同学应选择_____mL的容量瓶。
(2)应用托盘天平准确称量_______g NaOH固体。
(3)配制过程如图乙所示,则图甲操作应在图乙中的______ (填字母)之间。
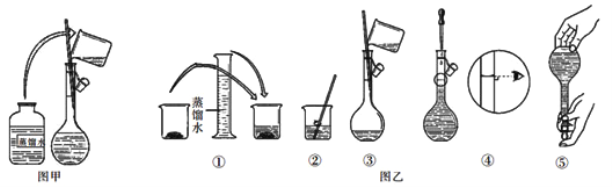
A.①与② B.②与③ C.③与④
(4)若在配制过程中出现下列情况,会使所配制NaOH溶液的浓度偏低的是______(填字母)。
A.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
B.定容时俯视
C.配制溶液所用的容量瓶洗净后没有烘干
D.NaOH固体在烧杯中溶解后,立即将溶液转移到容量瓶内,并接着进行后续操作
E.定容摇匀后,发现液面低于刻度线,再加入蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①热分解法、②热还原法、③电解法是工业上制取金属的三种常用方法。下列金属与冶炼方法相对应的是( )
A. Al、Na—③ B. Ca、Cu—② C. Fe、Mg—③ D. Al、Hg—①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的CaCl2、MgCl2、Na2SO4 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
![]()
(1)判断BaCl2已过量的方法是______________。
(2)第⑥步中,相关的离子方程式是____________________。
(3)为检验精盐纯度,需配制230mL0.2mol/L NaCl(精盐)溶液,则需用托盘天平称取精盐固体的质量为_______,需要的玻璃仪器有量筒、 __________________。
(4)配制NaCl(精盐)溶液时,若出现下列操作,造成结果偏低的是__________。
A.称量时NaCl已潮解 B.天平的砝码已锈蚀
C.定容摇匀时,液面下降又加水 D.定容时仰视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com