
【题目】实验室需要480mL1mol·L-1NaOH溶液,根据溶液配制情况回答下列问题:
(1)实验中除了托盘天平(砝码)、药匙、量筒、烧杯、玻璃棒外还需要的其他仪器有___。
(2)如图是某同学在实验室配制该NaOH溶液的过程示意图,其中有错误的是___(填操作序号)。
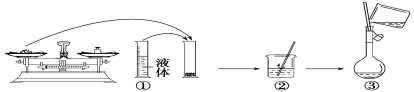
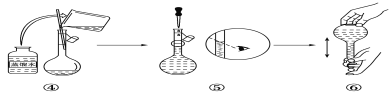
(3)下列操作会导致所配溶液的物质的量浓度偏高的是___。
A.配制NaOH溶液时,NaOH固体中含有Na2O杂质
B.用蒸馏水溶解NaOH固体后,立即转入容量瓶中定容
C.定容后发现液面高于刻线,可用胶头滴管将多余的水吸出
D.定容时仰视刻度线
E.用托盘天平称量 NaOH 固体时,砝码生锈
F.配制前容量瓶中有少量蒸馏水
(4)若某同学用密度为1.2g/cm3,质量分数为36.5%的浓盐酸配制100mL3mol/L的稀盐酸,需要用量筒量取浓盐酸的体积为___mL。
【答案】胶头滴管、500mL容量瓶 ①③⑤ ABE 25.0
【解析】
(1)根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(2)依据配置一定物质的量浓度溶液的正确操作步骤和仪器的正确使用方法解答;
(3)根据实验操作对![]() 的影响进行误差分析;
的影响进行误差分析;
(4)根据![]() 计算浓度,再根据稀释过程中溶质的物质的量不变,就取浓盐酸的体积。
计算浓度,再根据稀释过程中溶质的物质的量不变,就取浓盐酸的体积。
(1)操作步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管,根据提供的仪器可知,还需仪器有500ml容量瓶、胶头滴管;
(2)①量筒为量取仪器,不能用来溶解物质,故①错误;
②用玻璃杯搅拌加速固体的溶解,故②正确;
③玻璃棒引流操作时,玻璃棒下端应靠在容量瓶刻度线下方,故③错误;
④加水至刻度线的下方,操作正确,故④正确;
⑤定容时,眼睛应平视刻度线,故⑤错误;
⑥加盖摇匀,使溶液混合均匀,操作正确,故⑥正确;
答案为:①③⑤;
(3)A.配制NaOH溶液时,NaOH固体中含有Na2O杂质,氧化钠和水反应生成NaOH,生成相同物质的量的NaOH,氧化钠需要的质量小,所以会导致NaOH的物质的量偏大,则配制溶液浓度偏大,A符合题意;
B.用水溶解NaOH固体后,立即转入容量瓶中定容,热的溶液体积偏大,冷却后体积变小,则配制的溶液体积偏小,配制的溶液浓度偏高,B符合题意;
C.定容后发现液面高于刻线,可用胶头滴管将多余的水吸出,配制的溶液中溶质的物质的量偏小,配制的溶液浓度偏低,C不符合题意;
D.定容时仰视刻度线,导致加入的蒸馏水体积偏大,配制的溶液体积偏多,则配制的溶液浓度偏小,D不符合题意;
E.称量NaOH的固体时,砝码生锈,砝码质量变重,称量的NaOH质量偏大,浓度偏大,E符合题意;
F、容量瓶中有少量蒸馏水,不影响溶质的物质的量和溶液的体积,因此不影响浓度,F不符合题意;
答案选ABE;
(4)浓盐酸的浓度![]() ,配制100mL3mol/L的稀盐酸,根据稀释前后溶质的物质的量不变,设要用量筒量取浓盐酸的体积为VmL,100mL×3mol/L=V×12mol/L,V=25.0mL。
,配制100mL3mol/L的稀盐酸,根据稀释前后溶质的物质的量不变,设要用量筒量取浓盐酸的体积为VmL,100mL×3mol/L=V×12mol/L,V=25.0mL。


科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.1mol/L的H2A溶液中滴加0.1mol/LNaOH溶液,含A元素相关微粒物质的量随pH的变化如图所示。下列说法正确的是
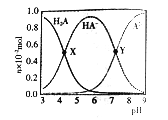
A. H2A在水中的电离方程式是:H2A=H++HA-, HA-![]() H++A2-
H++A2-
B. 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
C. Y点溶液中存在以下关系: c(H+)+c(Na+)=c(OH-)+3c(HA-)
D. X点溶液中含A元素相关微粒:c(H2A)+c(HA-)+c(A2-)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】α-鸢尾酮香料的分子结构如图,下列说法不正确的是

A. α-鸢尾酮可与某种酚互为同分异构体
B. 1 mol α-鸢尾酮最多可与3molH2加成
C. α-鸢尾酮能发生银镜反应
D. α-鸢尾酮经加氢→消去→加氢三步反应可转变为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼是新型无机材料中的明星元素。

(1)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为 ______,图为磷化硼晶体结构中最小的重复单元,磷化硼的晶体类型是 ______,一个晶胞中含 ______个P原子,每个B或P均形成4个共价键,其中有一个配位键,提供空轨道的是 ______原子。
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是 ______(填元素符号),其基态原子的电子排布式为 ______,氮化硼中B元素的化合价为 ______。
(3)环硼氮烷与苯是等电子体,其一氯代物有两种结构、二氯代物有四种结构,写出环硼氮烷分子结构式 ______。
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料。在BF3分子中,F-B-F的键角是 ______ 度,B原子采用 ______ 杂化;BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液100mL,其中可能含Fe3+、Al3+、Na+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子中的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示。
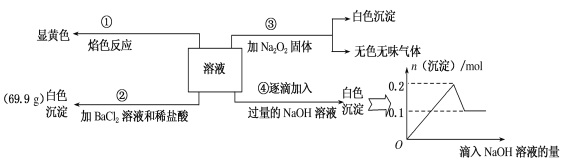
请回答下列问题:
(1)焰色反应是___(填“物理”或“化学”)变化;实验③中产生的无色无味气体是___(填化学式)。
(2)原溶液中一定存在的离子有___,一定不存在的离子有____。
(3)若溶液中K+物质的量为0.04mol,则c(Na+)=___mol/L。
(4)将一定量Fe2O3和Al2O3混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:
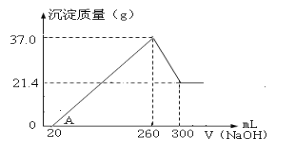
①混合物中含Fe2O3的质量为___g;
②所用硫酸溶液物质的量浓度为___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)3—甲基—1一丁炔的结构简式为_____________
(2)![]() 的分子式为_____________
的分子式为_____________
(3)烃A在同温、同压下蒸气的密度是H2的35倍,其分子式为_____________。
(4)分子式为C8H10属于芳香烃的同分异构体共有_____________种,其中____________(填结构简式)在苯环上的一氯取代产物有两种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为:_____KClO3+________HCl(浓)→_________KCl+_______ClO2↑+______Cl2↑+__________H2O
(1)请配平该化学方程式(未知系数填入横线内)。
(2)浓盐酸在反应中显示出来的性质是________(填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)5 ℃ 下将产物氯气0.1 mol溶于水配成1 L溶液,请写出氯气溶于水的化学反应方程式____________________。
(4)若改变温度至70 ℃,发现KClO3和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是进行气体性质实验的常用装置,液体一定不能充满试管的是

A.若a为水,b是HClB.若a为水,b是NO2
C.若a为水(滴有酚酞),b是NH3D.若a为NaOH溶液,b是Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近我国科学家预测并据此合成了新型碳材料:T-碳。可以看作金刚石结构中的一个 碳原子被四个碳原子构成一个正四面体结构单元替代(如图所示,所有小球都代表碳原子)。下列说法正确的是( )
金刚石 T-碳
T-碳
A.T-碳与石墨、金刚石互为同分异构体
B.T-碳晶体与金刚石晶体类似,属于原子晶体
C.T-碳晶体和金刚石晶体中含有的化学键不同
D.T-碳与金刚石中的碳原子采取的杂化方式不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com