
【题目】钴的化合物在磁性材料生产、电池制造、催化剂制备等方面应片非常广泛。
(1)Co2+基态外围电子排布式为______________。
(2)制备[Co(H2O)6]2+反应为(NH4)2[Co(SCN)4]+6H2O=[Co(H2O)6](SCN)2+2NH4SCN。
①配合物[Co(H2O)6]2+中与Co2+形成配位键的原子是_______(填元素符号);SCN-的空间构型为_____(用文字描述)。
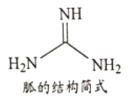
②NH4SCN在180-190℃分解并制得胍(结构简式如下图所示),胍分子中氮原子杂化轨道类型____;lmol胍中含σ键数目为___________。
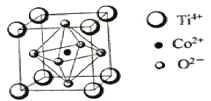
(3)一种钴的化合物可用作石油脱硫的催化剂,其晶胞结构如下图所示,则晶体中与每个O2-紧邻的O2-有________个(填数字)。
【答案】 3d7 O 直线形 sp3和sp2 8mol 8
【解析】 (1)钴是27号元素,所以Co2+基态外围电子排布式为3d7。
(2)①配合物[Co(H2O)6]2+中,水分子是配体,其中O原子有孤电子对,与中心原子Co2+形成配位键的原子是O;SCN-与CO2是等电子体,故其空间构型为直线形。
②由胍的结构简式可知,胍分子中有两种氮原子,每个氮原子都有1个孤电子对,其中两个氨基中的氮原子形成3个σ键,故其杂化轨道类型为sp3,另一个氮原子形成2个σ键和1个π键,其杂化轨道类型为sp2;lmol胍中含σ键数目为8mol。
(3)由晶胞结构示意图可知,晶胞中每个面的面心都有1个O2-,其与晶胞中邻近的4个面的面心上的O2-紧邻,一个面心为2个相邻的晶胞所共用,所以与每个O2-紧邻的O2-有8个。


科目:高中化学 来源: 题型:
【题目】下列关于F、Cl、Br、I的说法不正确的是( )
A.原子核外电子层数逐渐增多
B.被其他卤素单质从其卤化物中置换出来的可能性逐渐增大
C.单质的颜色逐渐加深
D.氢化物稳定性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. Cu(OH)2与稀硝酸反应:H++OH-=H2O
B. 铜片与浓硝酸反应:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
C. 铁与稀硝酸反应:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
D. 浓烧碱溶液中加入铝片:2Al + 4OH-= 2AlO2- + 2 H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2会对环境和人体健康带来极大的危害,工业上采取多种方法来减少这些有害气体的排放。SO2的除去有如下两种方法:
方法1(双碱法): 用NaOH吸收SO2,并用CaO使NaOH再生:NaOH溶液![]() Na2SO3。
Na2SO3。
(1)写出过程①的离子方程式:_____________________。
(2)CaO在水中存在如下转化:CaO(s)+H2O(1)= Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq)。从平衡移动的角度,简述过程②NaOH再生的原理:___________________________。
Ca2+(aq)+2OH-(aq)。从平衡移动的角度,简述过程②NaOH再生的原理:___________________________。
方法2:用氨水除去SO2:
(3)已如25℃,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=13×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0mol/L,溶液中的c(OH-)=______。将SO2通入该氨水中,当c(OH-)降为1.0×10-7mol/L时,溶液的c(SO32-)/c(HSO3-)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4L一氯甲烷中含极性共价键数目为4NA
B. 常温下,46g NO2、N2O4组成的混合气体中所含有的分子数为NA
C. 36g3H2中含有的中子数目为12NA
D. 2.24 L(标准状况)O2与足量钠反应时,转移电子数目不可能为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,三种难溶电解质的溶度积如下表。
物质 | Ag2CrO4 | AgCl | AgBr |
Ksp | 1.0×10-12 | 1.8×10-10 | 7.7×10-13 |
下列说法正确的是
A. 向饱和AgCl溶液中通入少量HCl气体,溶液中c(Ag+)不变
B. 浓度均为1×10-6 molL﹣1的AgNO3、HBr溶液等体积混合后会生成AgBr沉淀
C. 常温下,以0.01 molL﹣1 AgNO3溶液滴定20mL0.01molL﹣1KCl和0.01molL﹣1K2CrO4的混合溶液,CrO42-先沉淀
D. 常温下,Ag2CrO4(s)+2Cl-(aq)![]() 2AgCl(s)+CrO42-(aq)的平衡常数K=3.1×107
2AgCl(s)+CrO42-(aq)的平衡常数K=3.1×107
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修5:有机化学基础]氯吡格雷是一种用于抑制血小板聚集的药物,可通过如图方法合成:

已知:①![]()
![]()
![]() ;②
;②![]() 中氯原子较难水解;③RCHO
中氯原子较难水解;③RCHO![]()
![]() 。
。
根据以上信息回答下列问题:
(1)A的名称是_________,F中无氧官能团的名称是_______。
(2)D的结构简式为_______;C分子中最多有____个原子共平面。
(3)写出下列反应的化学方程式:反应②:_________________。
(4)已知:![]() ,则由乙醇、甲醇为有机原料制备化合物
,则由乙醇、甲醇为有机原料制备化合物![]() ,需要经历的反应类型有________(填写编号)。①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物
,需要经历的反应类型有________(填写编号)。①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物![]() 的最后一步反应_______________________________________________。
的最后一步反应_______________________________________________。
(5)E的同分异构体中,满足下列条件的有___种(不考虑立体异构),其中一种的核磁共振氢谱显示5组峰,且峰面积之比为1∶1∶2∶2∶2,请写出其结构简式____。
①结构中含有苯环且存在与F相同的官能团;
②能发生银镜反应,其碱性条件下水解的两种产物也能发生银镜反应。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com