
(7分)
I.Zn – MnO2干电池应用广泛,其电解质溶液是ZnCl2一NH4Cl混合溶液。
(1)该电池的负极材料是 。电池工作时,电子流向 极(填“正”、“负”)。
(2)若ZnCl2- NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,欲除去Cu2+,最好选用下列试剂中的 (填代号)
A. NaOH B.Zn C.Fe D.NH3.H2O
Ⅱ.下图是甲烷燃料电池原理示意图,请回答下列问题:
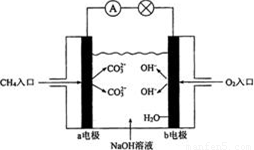
(3)电池的正极是 (填“a”或“b”)电极,负极上的电极反应式是 。
(4)电池工作一段时间后电解质溶液的pH (填“增大”、“减小”、“不变”)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
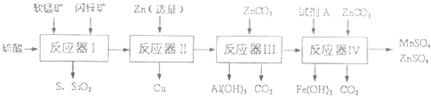
| 物质 | Fe(OH)3 | A1(OH)3 | Zn(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 2.7 | 3.3 | 5.4 | 7.6 | 8.3 |
| 完全沉淀pH | 4.4 | 5.2 | 8.0 | 9.6 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 锌锰干电池中含NH4Cl淀粉糊(电糊)、Mn02、炭粉和锌筒(含锌、铁和铜 等)等物质(如图).
锌锰干电池中含NH4Cl淀粉糊(电糊)、Mn02、炭粉和锌筒(含锌、铁和铜 等)等物质(如图).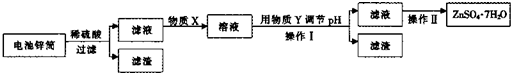
| 氢氧化物 | Fe(OH)3 | Mn(OH)2 | Fe(OH)2 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.7 | 8.1 | 7.6 | 6.5 | 4.7 |
| 完全沉淀的pH | 3.7 | 10.1 | 9.6 | 8.0 | 6.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
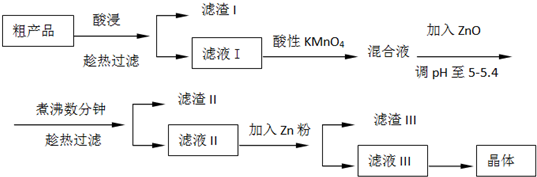
| 沉淀物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Cd(OH)2 | Mn(OH)2 | pH值 | 8.0 | 9.7 | 3.2 | 6.7 | 9.4 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012年黑龙江龙东地区高一下学期期末考试化学试卷(带解析) 题型:填空题
I(4分)冶炼金属常用以下几种方法:①以C、CO或H2做还原剂 ②以活泼金属Na、Mg等还原 ③利用铝热反应原理还原 ④电解法 ⑤热分解法。下列金属各采用哪种方法还原最佳。(用序号填写下列空白)。
(1)Fe、Zn、Cu等中等活泼金属 。
(2)Na、Mg、Al等活泼或较活泼金属 。
(3)Hg、Ag等不活泼金属 。
(4)V、Cr、Mn、W等高熔点金属 。
II(共6分).从A.乙烯 B.乙酸 C.葡萄糖 D.纤维素 E.油脂 F.蛋白质六种有机物中选择合适的物质,将其字母序号填在空格内。
(1)属于烃类的是 。
(2)能与乙醇发生酯化反应的是 。
(3)植物通过光合作用直接生成的有机物是 。
(4)肉、蛋、奶等富含 。
(5)能作为制造肥皂的原料是 。
(6)棉花、甘蔗渣的主要成分是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com