
����Ŀ����֪K��Ka��Kb��Kw��Kh��Ksp�ֱ��ʾ��ѧƽ�ⳣ��������ĵ���ƽ�ⳣ��������ĵ���ƽ�ⳣ����ˮ�����ӻ��������ε�ˮ��ƽ�ⳣ�������ܵ���ʵ��ܶȻ�������
��1���й�����������˵����ȷ����______��
a�����Ƕ��ܷ�ӳһ�������¶�Ӧ�仯���еij̶�
b�����ǵĴ�С�����¶ȵ����߶�����
c�������£�CH3COOH��ˮ�е�Ka�����ڱ���CH3COONa��Һ�е�Ka
d��һ���¶��£���CH3COONa��Һ�У�Kw��Ka��Kh
��2��25��ʱ����a mol��L��1�İ�ˮ��0.01 mol��L��1�������������������Һ��c(NH4+)��c(Cl��)������Һ��_____(����������������������)�ԣ��ú�a�Ĵ���ʽ��ʾNH3��H2O�ĵ���ƽ�ⳣ��Kb��____��
��3����¯�����з����ķ�Ӧ��FeO(s)��CO(g)![]() Fe(s)��CO2(g) ��H<0���÷�Ӧ��ƽ�ⳣ������ʽK��_____����֪1100 ��ʱ��K��0.25����ƽ��ʱCO��ת����Ϊ________���ڸ��¶��£�����ø�¯��c(CO2)��0.020 mol��L��1��c(CO)��0.1 mol��L��1�����ʱ��Ӧ��������(��)_____��(��)(����>����<����������)��
Fe(s)��CO2(g) ��H<0���÷�Ӧ��ƽ�ⳣ������ʽK��_____����֪1100 ��ʱ��K��0.25����ƽ��ʱCO��ת����Ϊ________���ڸ��¶��£�����ø�¯��c(CO2)��0.020 mol��L��1��c(CO)��0.1 mol��L��1�����ʱ��Ӧ��������(��)_____��(��)(����>����<����������)��
��4����֪������Fe(OH)3��Mg(OH)2��Ksp�ֱ�Ϊ8.0��10��38��1.0��10��11����Ũ�Ⱦ�Ϊ0.1 mol��L��1��FeCl3��MgCl2�Ļ����Һ�м����Һ��ҪʹFe3����ȫ������Mg2����������Ӧ�õ�����ҺpH�ķ�Χ��______(��֪lg2��0.3)��
���𰸡�ad �� ![]()
![]() 20% > 3.3��pH<9
20% > 3.3��pH<9
��������
(1)ƽ�ⳣ��ֻ���¶��йأ������¶�ƽ�������ȷ����ƶ���
(2)���û����Һ��c(NH4+)=c(Cl-)�����ݵ���غ��c(OH-)�Tc(H+)�����������غ��c(NH3��H2O)=(0.5a-0.005)mol/L�����ݵ���غ��c(H+)=c(OH-)=10-7mol/L����Һ�����ԣ�NH3H2O�ĵ��볣��Kb=![]() ��
��
(3)���ݻ�ѧ����ʽ��ƽ�ⳣ��������д����ʽ������ʼʱCO��Ũ��Ϊ1mol/L��
FeO(s)��CO(g)![]() Fe(s)��CO2(g)
Fe(s)��CO2(g)
��ʼ���ʵ���Ũ��(mol/L) 1 0
�仯���ʵ���Ũ��(mol/L) c c
ƽ�����ʵ���Ũ��(mol/L) 1-c c
���ƽ�ⳣ���ı���ʽ����ƽ��ʱCO��Ũ�ȣ��ټ�����ת���ʣ�����Ũ���̼�����ƽ�ⳣ���ȽϷ�����Ӧ���еķ���
(4)�ֱ����Fe3+��ȫ����ʱ��pH��Mg2+��ʼ����ʱ��pH��
(1)a��ƽ�ⳣ������������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ��������Ƕ��ܷ�ӳһ�������¶�Ӧ�仯���еij̶ȣ���a��ȷ��
b�������¶�ƽ�������ȷ����ƶ��������ѧƽ������Ӧ�Ƿ��ȷ�Ӧ���������¶Ȼ�ѧƽ�ⳣ��K��С����b����
c������ƽ�ⳣ��ֻ���¶��йأ��¶���ͬ����ƽ�ⳣ����ͬ����c����
d��һ���¶��£���CH3COONa��Һ��Ka=![]() ��Kh=
��Kh=![]() ��Kw=c��H+����c��OH-������Kw=KaKh����d��ȷ��
��Kw=c��H+����c��OH-������Kw=KaKh����d��ȷ��
��ѡad��
(2)���û����Һ��c(NH4+)=c(Cl-)�����ݵ���غ��c(OH-)�Tc(H+)����Һ�����ԣ����������غ��c(NH3��H2O)=(0.5a-0.005)mol/L�����ݵ���غ��c(H+)=c(OH-)=10-7mol/L����Һ�����ԣ�NH3H2O�ĵ��볣��Kb=![]() =
=![]() =
=![]() ��
��
(3)FeO(s)+CO(g)�TFe(s)+CO2(g)��H��0��ƽ�ⳣ����������ƽ��Ũ�ȵ��ݴη��˻����Է�Ӧ���ƽ��Ũ���ݴη��˻���ƽ�ⳣ��K=![]() ������ʼʱCO��Ũ��Ϊ1mol/L��
������ʼʱCO��Ũ��Ϊ1mol/L��
FeO(s)��CO(g)![]() Fe(s)��CO2(g)
Fe(s)��CO2(g)
��ʼ���ʵ���Ũ��(mol/L) 1 0
�仯���ʵ���Ũ��(mol/L) c c
ƽ�����ʵ���Ũ��(mol/L) 1-c c
��ƽ�ⳣ��K=![]() =
=![]() =0.25����ã�c=0.2mol/L��CO��ת����Ϊ
=0.25����ã�c=0.2mol/L��CO��ת����Ϊ![]() =20%����֪1100��ʱ��K=0.25����ø�¯��c(CO2)��0.020 mol��L��1��c(CO)��0.1 mol��L��1��Ũ����Qc=
=20%����֪1100��ʱ��K=0.25����ø�¯��c(CO2)��0.020 mol��L��1��c(CO)��0.1 mol��L��1��Ũ����Qc=![]() =0.2��K������������¸÷�Ӧδ����ƽ��״̬����Ӧ������У������������� ��
=0.2��K������������¸÷�Ӧδ����ƽ��״̬����Ӧ������У������������� ��
(4)Fe3+��ȫ����ʱ��Һ��c��OH-��=![]() =2��10-11mol/L��c��H+��=5��10-4mol/L����ʱ��Һ��pH=-lgc(H+)=4-lg5=3.3��Mg2+��ʼ����ʱ��Һ��c��OH-��=
=2��10-11mol/L��c��H+��=5��10-4mol/L����ʱ��Һ��pH=-lgc(H+)=4-lg5=3.3��Mg2+��ʼ����ʱ��Һ��c��OH-��=![]() =1��10-5mol/L��c��H+��=1��10-9mol/L����ʱ��Һ��pH=9��ҪʹFe3����ȫ������Mg2����������Ӧ�õ�����Һ��pH��ΧΪ3.3��pH��9��
=1��10-5mol/L��c��H+��=1��10-9mol/L����ʱ��Һ��pH=9��ҪʹFe3����ȫ������Mg2����������Ӧ�õ�����Һ��pH��ΧΪ3.3��pH��9��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�ǿ���С����Ƶ��û�ѧ��ԴʹLED�Ʒ����װ�á�����˵����ȷ����
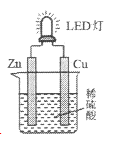
A. ��Һ�е�SO42����ͭ���ƶ�
B. пƬΪԭ��صĸ�����������ԭ��Ӧ
C. �����ϡ���ỻ������֭�������в����е�������
D. ͭƬ�������������ɣ������ķ�ӦΪ��2H++2e����H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�ķ���ʽ��ȷ����
A.����Ȼ�þ��Һ��2Cl�C+2H2O![]() H2��+Cl2��+2OH�C
H2��+Cl2��+2OH�C
B.̼�������Һ�м�������ʯ��ˮ��Ca2++![]() +OH�C=CaCO3��+H2O
+OH�C=CaCO3��+H2O
C.Al2(SO4)3��Һ�м��������ˮ��Al3++3NH3��H2O=Al(OH)3��+3NH4+
D.����������Һ�м���ϡ���H��(aq)��OH��(aq)=H2O(l)����H����57.3 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ļ�����ϳɡ�Ӧ���Լ��Ի�����Ӱ��һֱ�ǿ�ѧ���о����ȵ㡣
(1)������Ҫ��NH3��CO2Ϊԭ�Ͻ��кϳɡ���Ҫͨ������������Ӧ����:
��Ӧ1��2NH3(l)+CO2(g)![]() H2NCOONH4(l)����H1= -117.2 kJ��mol-1
H2NCOONH4(l)����H1= -117.2 kJ��mol-1
��Ӧ2��H2NCOONH4(l)![]() H2O(l)+CO(NH2)2(l)����H2=+21.7 kJ��mol-1
H2O(l)+CO(NH2)2(l)����H2=+21.7 kJ��mol-1
��ش�CO(NH2)2 (l)+H2O(l)![]() 2NH3(l)+CO2(g) ��H3=_____________���÷�Ӧ���Է����е���Ҫԭ����__________________��
2NH3(l)+CO2(g) ��H3=_____________���÷�Ӧ���Է����е���Ҫԭ����__________________��
(2)��̿����ԭSO2����S2����ѧ����ʽΪ��2C(s)+2SO2(g)![]() S2(g)+2CO2(g)���ں��������У�1 mol/LSO2�������Ľ�̿��Ӧ��SO2��ת�������¶ȵı仯��ͼ��ʾ��
S2(g)+2CO2(g)���ں��������У�1 mol/LSO2�������Ľ�̿��Ӧ��SO2��ת�������¶ȵı仯��ͼ��ʾ��
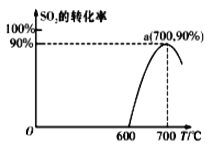
����700�������÷�Ӧ����3���Ӵﵽƽ�⣬����0��3����v(S2)=_______molL-1min-1�����¶��µ�ƽ�ⳣ��Ϊ_________��
�����÷�Ӧ����ʼ�¶�Ϊ700���ĺ��ݾ��������н��У��ﵽƽ��ʱSO2��ת����________90%(��������������������=��)��
������˵��һ����˵���÷�Ӧ�ﵽƽ��״̬����_______��
A����̿���������ٱ仯ʱ
B��CO2��SO2��Ũ�����ʱ
C��SO2������������CO2����������֮��Ϊ1:1
D����������ѹǿ���ٱ仯ʱ
(3) NO2��O2������KNO3������ȼ�ϵ�أ���ԭ����ͼ��ʾ��

ʯīI���������ķ�ӦΪ__________________________________�������·ͨ��1mole-�������Ϲ�����_______mol N2O5 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20mL0.05mol��L��1��ijϡ��H2B��Һ�е���0.1mol��L��1��ˮ����Һ����ˮ�����������Ũ������백ˮ����仯��ͼ�����з�����ȷ���ǣ� ��

A. NaHB��Һ����Ϊ���ԣ�Ҳ����Ϊ����
B. A��B��C������Һ��pH����С��D��E��F������Һ��pH��������
C. E��Һ������Ũ�ȴ�С��ϵ��c(NH4+)>c(B2��)>c(OH��)>c(H+)
D. F����Һc(NH4+)=2c(B2��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں���������ʵ���Һ�У������ж����ѧƽ��档
��1��һ���¶��£���1L0.1molL��1CH3COOH��Һ�м���0.1molCH3COONa���壬ƽ�������Һ��![]() ___�����������С�����䡱����д����ʾ�û����Һ����������Ũ�ȼ��һ����ʽ��______
___�����������С�����䡱����д����ʾ�û����Һ����������Ũ�ȼ��һ����ʽ��______
��2����������20mL 0.1molL��1Na2CO3��Һ����μ���0.1molL��1HCl��Һ40mL����Һ�к�̼Ԫ�صĸ�������CO2���ݳ�δ���������ʵ�����������ҺpH�仯��������£�
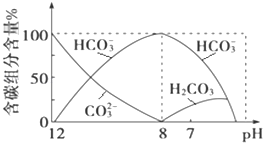
�ش��������⣺
����ͬһ��Һ�У�H2CO3��HCO3����CO32��___����ܡ����ܡ����������棻
�ڵ�pH��7ʱ����Һ�к�̼Ԫ�ص���Ҫ����_____��___����Һ�к������������������ʵ���Ũ�ȵĴ�С��ϵΪ____��
����֪��25��ʱ��CO32��ˮ�ⷴӦ��ƽ�ⳣ����ˮ�ⳣ��Kh�T2��10��4 molL��1������Һ��c��HCO3������c��CO32������2��1ʱ����Һ��pH��_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NiCl2�ǻ����ϳ�������Ҫ����Դ����ҵ�����ú���(Ni)�ϴ�������Ҫ����Ni��������SiO2��Al2O3��Fe�������������ᡢ������ʣ������Ȼ������壨NiCl2��nH2O��������ͼ��
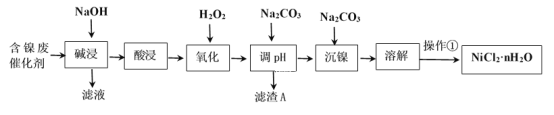
���ֽ�����������Ksp����ֵ���±���ʾ��
��ѧʽ | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp����ֵ | 10-17 | 10-38 | 10-34 | 10-15 |
�ش��������⣺
��1��Al��ԭ�ӽṹʾ��ͼΪ___��
��2��������������ܽ�����ʹ�õ���Ϊ___���������ʱ������Ӧ�����ӷ���ʽΪSiO2+2OH-=SiO32-+H2O��____��
��3��������������H2O2��Һ����������___(�����ӷ���ʽ��ʾ)��Ȼ�����pHʹ��Һ����Ԫ��ǡ����ȫ����������Ũ����10-5mol��L-1ʱ�����ӳ�����ȫ������ʱ�����µ�pHԼΪ____��
��4��������������ʵ���������Ϊ�������ȣ�Ũ����___Ϊֹ����ȴ�ᾧ�����ˡ�ϴ�ӡ�������ò�Ʒ��
��5���������ѳ�Ϊ��϶�����������Ҫ������ͣ����ڼ��Ե������Һ�Ĺ���ԭ�����£�M+Ni(OH)2![]() MH+NiOOH(ʽ��MΪ����Ͻ�)��д����س������������ĵ缫��Ӧʽ___��
MH+NiOOH(ʽ��MΪ����Ͻ�)��д����س������������ĵ缫��Ӧʽ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������һ�����Ƹ�Ѫѹ��ҩ����м��壬����ͨ�����·����ϳɣ�
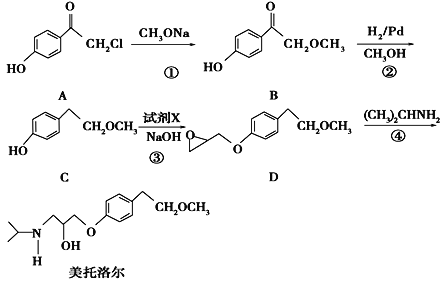
��ش��������⣺
��1��д��C�еĹ����ŵ�����Ϊ_________________.
��2����������ķ���ʽ________________.
��3��д����Ӧ�ٵĻ�ѧ����ʽ__________________________________________����Ӧ�ڵķ�Ӧ������_____________
��4����Ӧ���м�����Լ�X�ķ���ʽΪC3H5OCl��X�Ľṹ��ʽΪ____________________.
��5����������������B��ͬ���칹������_______�֣����к˴Ź������������ֲ�ͬ��ѧ�������⣬�ҷ������Ϊ3��2��2��1��1��1����________________________(д�ṹ��ʽ)
���ܷ���������Ӧ�����ܷ���ˮ��
������FeCl3��Һ������ɫ��Ӧ
��ֻ��һ����
��6����������֪ʶ�������Ŀ���������Ϣ��д����![]() ��
��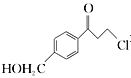 Ϊԭ���Ʊ�
Ϊԭ���Ʊ�![]() �ĺϳ�·������ͼ(���Լ���ѡ)���ϳ�·������ͼʾ�����£�
�ĺϳ�·������ͼ(���Լ���ѡ)���ϳ�·������ͼʾ�����£�![]() _______________________
_______________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ѫ֬����Ӱ������ɿ���������H��һ���ٴ����Ƹ�Ѫ֢֬��ҩ�H�Ľṹ��ʽ��ͼ��ʾ��
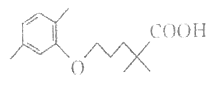
����˵������ȷ���ǣ� ��
A. �л���H���еĹ�����ֻ���Ȼ�
B. 1mol H��ȫȼ������19molO2
C. �л���H�Ƿ��㻯����
D. �л���H�ܺ��ơ�̼�����Ʒ�Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com