
|
100 ml 1 mol/L的AlCl3溶液与100 ml 3.5 mol/L的NaOH溶液混合,得到沉淀为 | |
| [ ] | |
A. |
7.8 g |
B. |
0 g |
C. |
9.1 g |
D. |
3.9 g |
科目:高中化学 来源:四川省南山中学2011-2012学年高一上学期12月月考化学试题(1) 题型:038
将0.1 mol的镁、铝混合物溶于100 mL 4 mol/LHCl溶液中,然后再滴加1 mol/L NaOH溶液.请回答:
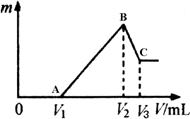
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如上图所示已知当V1=160 mL时,求金属粉末中Mg的物质的量以及V3为多少mL.
(该小问写出计算过程)
(2)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 4 mol/LHCl溶液溶解此混合物后,再加入450 mL 1 mol/L的NaOH溶液,所得沉淀中无Al(OH)3.满足此条件的a的取值范围是:________
查看答案和解析>>
科目:高中化学 来源:非常讲解·教材全解全析 高中化学 必修1 (山东版) 山东版 题型:022
往100 mL 1 mol/L的NaOH溶液中通入CO2,其溶质的物质的量(m)与通入CO2气体的物质的量(n)的关系如图.

(1)AB段(不包括A、B两点)溶质的成分是________,n的取值范围是________,溶质的物质的量(m)为________,溶质的质量为________g(均用n表示).
(2)BC段(不包括B、C两点)溶质的成分是________,n的取值范围是________,溶质的物质的量(m)为________,溶质的质量为________g(均用n表示).
查看答案和解析>>
科目:高中化学 来源:江苏省苏北四市2012届高三第一次调研测试化学试题 题型:058
“实验化学”
为测定抗贫血药物复方硫酸亚铁中铁的含量,某化学学习小组进行了以下实验研究.
[实验原理]有些溶液本身无色,但加入其他试剂后会有明显的颜色,溶液颜色的深浅和浓度有关,通过比较颜色的深浅可测定物质的含量.
[实验用品]2.00×10-2 mol/L Fe3+的标准溶液、蒸馏水、5% KSCN溶液、pH=4的HAc-NaAc缓冲溶液、1∶1 HNO3溶液、复方硫酸亚铁药片.
铁架台(铁夹)、100 mL容量瓶、胶头滴管、量筒、烧杯、三脚架、石棉网、酒精灯、玻璃棒、25 mL比色管、pH试纸.
[实验过程]
(1)配制系列标准溶液:分别量取2.00×10-2 mol/L Fe3+的标准溶液6.00 mL、6.50 mL、7.00 mL、7.50 mL置于4支25 mL比色管中,再加入1.0 mL 5%KSCN溶液和2.5 mL pH=4的HAc-NaAc缓冲溶液,加蒸馏水稀释至刻度.
(2)制取待测液:取1片复方硫酸亚铁药片,准确称量其质量,置于50 mL烧杯中,加入2 mL蒸馏水溶解,再加入2 mL 1∶1 HNO3溶液,小心加热2~3 min.冷却后,全部移入100 mL容量瓶中,再加入4.0 mL 5%KSCN溶液和10.0 mL pH=4的HAc-NaAc缓冲溶液等,振动、定容、摇匀制得待测液100 mL.取25.00 mL待测液加入与(1)相同规格的比色管中.
(3)比色:将(2)所得比色管中的溶液与(1)各比色管中的溶液进行比较,确定待测液中Fe3+的浓度范围.
请回答下列问题:
(1)在含有Fe3+的溶液中加入KSCN溶液,溶液显________色.
(2)完成该实验,还缺少的仪器有________、________.
(3)加入pH=4的HAc-NaAc缓冲溶液的目的是________.
(4)实验中量取 HNO3溶液、HAc-NaAc缓冲溶液量筒即可,原因是________.
(5)标准溶液的浓度过大或过小均对实验结果有影响,则浓度过小对实验结果造成的影响是________.
(6)若测得待测液中Fe3+的物质的量浓度为cmol/L,药片的质量为m,则药片中铁元素的质量分数为________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁盘锦第二高中高二第二次阶段考试化学试卷(带解析) 题型:填空题
(14分)物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种。请根据所学化学知识回答下列问题:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中离子浓度由大到小的顺序为_______。
(2)B为0.1 mol·L-1的NaHCO3溶液,NaHCO3在该溶液中存在的平衡有(用离子方程式表示)______________ , ______________ , _______________。
(3)以下各小题均为常温下的溶液
j某溶液中由水电离的c(H+)=10-10mol·L-1,则该溶液的pH为__________。
k盐类水解的逆反应是中和反应 (填“对”或“错”)
lHCO3—溶液呈碱性说明HCO3—的电离能力弱于水解能力 (填“对”或“错”)
m盐溶液显酸碱性,一定是由水解引起的 (填“对”或“错”)
(4)D为含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:
AgCl(s)  Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 ml蒸馏水 ②100 mL 0.3 mol·lL-1 AgNO3溶液 ③100 mL 0.1 mol·L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为_______________(填序号),此时溶液②中Cl-物质的量浓度为__________________。
查看答案和解析>>
科目:高中化学 来源:2014届辽宁盘锦第二高中高二第二次阶段考试化学试卷(解析版) 题型:填空题
(14分)物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种。请根据所学化学知识回答下列问题:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中离子浓度由大到小的顺序为_______。
(2)B为0.1 mol·L-1的NaHCO3溶液,NaHCO3在该溶液中存在的平衡有(用离子方程式表示)______________ , ______________ , _______________。
(3)以下各小题均为常温下的溶液
j某溶液中由水电离的c(H+)=10-10mol·L-1,则该溶液的pH为__________。
k盐类水解的逆反应是中和反应 (填“对”或“错”)
lHCO3—溶液呈碱性说明HCO3—的电离能力弱于水解能力 (填“对”或“错”)
m盐溶液显酸碱性,一定是由水解引起的 (填“对”或“错”)
(4)D为含有足量AgCl固体的饱和溶液,AgCl在溶液中存在如下平衡:
AgCl(s)  Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在25℃时,AgCl的Ksp=1.8×10-10。现将足量AgCl分别放入下列液体中:①100 ml蒸馏水 ②100 mL 0.3 mol·lL-1 AgNO3溶液 ③100 mL 0.1 mol·L-1MgCl2溶液充分搅拌后冷却到相同温度,Ag+浓度由大到小的顺序为_______________(填序号),此时溶液②中Cl-物质的量浓度为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com