
| A. | 46 g的NO2和N2O4混合气体含有的原子数为3NA | |
| B. | 1 mol Na2O2与足量H2O反应,转移的电子数为NA | |
| C. | 物质的量浓度为0.5 mol/L MgCl2溶液,含有Cl-离子数为NA | |
| D. | 2.7g铝与足量的盐酸或氢氧化钠溶液反应,生成H2的分子数均为0.15NA |
分析 A、NO2和N2O4的最简式为NO2;
B、过氧化钠与水的反应为歧化反应;
C、溶液体积不明确;
D、求出铝的物质的量,然后根据1mol铝生成1.5mol氢气来分析.
解答 解:A、NO2和N2O4的最简式为NO2,故46g混合物中含有的NO2的物质的量为1mol,故含有3mol原子即3NA个,故A正确;
B、过氧化钠与水的反应为歧化反应:2Na2O2+2H2O=4NaOH+O2↑,此反应中,2mol过氧化钠转移2mol电子,故1mol过氧化钠转移1mol电子即NA个,故B正确;
C、溶液体积不明确,故溶液中的氯离子的个数无法计算,故C错误;
D、2.7g铝的物质的量为0.1mol,根据方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知:1mol铝生成1.5mol氢气,故0.1mol铝转移0.15mol氢气即0.15NA个,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:解答题
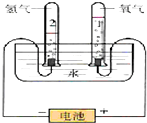 水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图.
水是人类宝贵的自然资源,也是一种重要的化工原料.如图是电解水原理的实验装置图. .
.| 质 量 | 物质的量 | O2与H2的体积比(同温同压下) | |
| O2 | 3.2g | 0.1mol | 1:2 |
| H2 | 0.4g | 0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干水是纯净物 | B. | 干水和干冰是同一种物质 | ||
| C. | 干水中的水分子不再运动 | D. | 用干水能更好地吸收CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是组成中含有氢元素的化合物都属于酸 | |
| B. | 凡是组成中含有OH-的化合物都属于碱 | |
| C. | 酸和碱中至少含有一种相同的元素 | |
| D. | 酸和碱中都含有金属阳离子和阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H2 | B. | C2H4 | C. | C3H4 | D. | C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23g Na完全转化生成Na2O和Na2O2,失去电子数为NA 到2NA之间 | |
| B. | 常温常压下,46g由NO2和N2O4组成的混合气体中含有原子的总数为3NA | |
| C. | 含2mol H2SO4的浓硫酸与足量铜微热反应,生成SO2分子数为NA | |
| D. | 粗铜精炼时转移1mol电子,阳极上溶解的Cu原子数一定为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应方程式 | 平衡常数 |
| Si+4HF(aq)?SiF4+2H2 | K1 |
| Si+4HCl(aq)?SiCl4+2H2 | K2 |
| Si+4HBr(aq)?SiBr4+2H2 | K3 |
| A. | K1>K2>K3 | B. | K1>K3>K2 | C. | K2>K3>K1 | D. | K3>K2>K1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com