
【题目】A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知烃B在标准状况下的密度为1.16g·L-1,C能发生银镜反应,F为有浓郁香味,不易溶于水的油状液体。
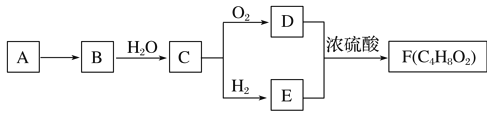
请回答:
(1)有机物D中含有的官能团名称是___。
(2)D+E→F的反应类型是___。
(3)有机物A在高温下转化为B的化学方程式是___。
(4)下列说法正确的是___。
(A)有机物E与金属钠反应比水与金属钠反应要剧烈
(B)有机物D、E、F可用饱和Na2CO3溶液鉴别
(C)实验室制备F时,浓硫酸主要起氧化作用
(D)有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
【答案】羧基 取代反应(或酯化反应) 2CH4![]() CH≡CH+3H2 BD
CH≡CH+3H2 BD
【解析】
A是天然气的主要成分,则A为CH4;已知烃B在标准状况下的密度为1.16gL-1,则B的摩尔质量为:M(B)=22.4L/mol×1.16gL-1≈26g/mol;C能发生银镜反应,则C分子中含有醛基;F为有浓郁香味,不易溶于水的油状液体,则F为酯,根据转化关系可知F为CH3COOC2H5;C催化氧化得D,C与氢气发生还原反应生成E,则D为CH3COOH、E为CH3CH2OH、C为CH3CHO;B与水反应生成乙醛,且B的摩尔质量为26g/mol,则B为CH≡CH,以此来解答。
(1)A为CH4,B为CH≡CH,D的结构简式为D为CH3COOH,其含有的官能团为羧基;
(2)有机物D+E→F的化学方程式为CH3COOH+CH3CH2OH→CH3COOC2H5+H2O此反应是酯化反应,属于取代反应;
(3)A为CH4,B为CH≡CH,C为CH3CHO,D为CH3COOH,CH4在高温下转化为CH≡CH的化学方程式是2CH4![]() CH≡CH+3H2;
CH≡CH+3H2;
(3)A. E为CH3CH2OH,乙醇与金属钠反应不如水与金属钠反应剧烈,故A错误;
B. D为CH3COOH、E为CH3CH2OH、F为CH3COOC2H5,乙酸与碳酸钠生成气体,乙酸乙酯不溶于饱和碳酸钠溶液,乙醇易溶于碳酸钠溶液,所以可用饱和Na2CO3溶液鉴别三者,故B正确;
C. 实验室制备F时,浓硫酸主要起催化作用和脱水剂作用,故C错误;
D. 有机物C为CH3CHO,CH3CHO中含有醛基,醛基能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化,故D正确;
故答案为:BD。


科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为![]() ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)A为____(写出元素符号,下同);
(2)B为____,简化电子排布式是____;
(3)C为____,外围电子排布式是____;
(4)D为____,轨道表示式是____;
(5)E原子结构示意图是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某纯碱样品中含有少量NaCl杂质,现用如图所示装置来测定纯碱样品中Na2CO3的质量分数(铁架台、铁夹等在图中均已略去;碱石灰是生石灰与氢氧化钠的混合物,可以吸收水和二氧化碳)。
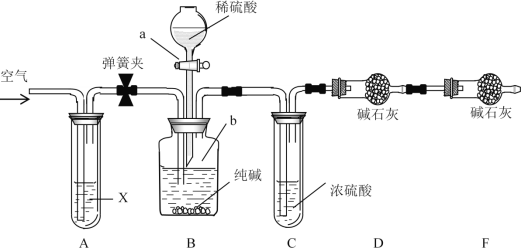
实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为80.20g;
③准确称得20.00g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入一定量空气;
⑥然后称得干燥管D的总质量为86.36g ;
⑦重复步骤⑤和⑥的操作,直到干燥管D的质量不变,为86.80 g。
试回答:
(1)装置B中发生反应的离子方程式_________________________________;
(2)装置A中试剂X应选用足量的(______)
A.饱和NaCl溶液 B.浓H2SO4
C.NaHCO3溶液 D.NaOH溶液
(3)①请用文字叙述装置C的作用:__________________________________。
②请用文字叙述装置E的作用:__________________________________。
(4)如果将分液漏斗中的硫酸换成浓度相同的盐酸,则会导致测定结果_____(填“偏大”、 “偏小”或“不变”,下同);若没有操作⑤⑦,则会导致测定结果__________。
(5)根据实验中测得的有关数据,计算出纯碱样品Na2CO3的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关NaHCO3溶液的说法正确的是
A. 该溶液中,H+、Al3+、Cl-能大量共存 B. 该溶液中c(H2CO3)<c(CO32-)
C. 该溶液中阳离子总数大于阴离子总数 D. 常温下,加水稀释,  变小
变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符合的是
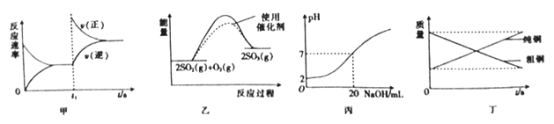
A.图甲表示t1时刻增加反应物浓度后v(正)和v(逆)随时间的变化
B.图乙表示反应2SO2(g)+O2(g)=2SO3(g) △H<0 在两种条件下物质能量随反应过程的变化
C.图丙表示25℃时用0.01mol/LNaOH溶液滴定20.00 mL 0.01mol/LHCl溶液时pH随NaOH 溶液体积的变化
D.图丁表示电解精炼铜时纯铜和粗铜的质量随时间的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
A | B | ||||||
D | E | F | |||||
C | G | H |
(1)上述元素的单质中熔点最高的可能是________________(填名称)。
(2)D的氢化物比G的氢化物稳定,其原因是__________________________________________________________。
(3)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为___________;该物质溶于水后的溶液呈________性(填“酸”、“碱”或“中”)。
(4)现有另一种元素X,其原子获得一个电子所释放出的能量是上表中所列元素中最大的,则X是周期表中第__________族元素。
(5)“神舟”六号载人飞船内需要有一种化合物来吸收航天员呼出的CO2,你认为该物质应该是由上表中的___________(填字母代号)元素组成的,用化学方程式表示吸收原理_________________________________________________________________。
飞船中需要制造一种适合航天员生存的人工态环境,还应该在氧气中充入一种稀释气体,该气体化学式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在容积恒定的密闭容器中发生反应A(s)+2B(g)![]() C(g)+D(g)。下列不能说明反应一定达到化学平衡状态的是
C(g)+D(g)。下列不能说明反应一定达到化学平衡状态的是
A. v正(B)=2v逆(C) B. 每消耗1molC,同时生成1molD
C. 气体的密度保持不变 D. 容器内压强保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示A、B、C、D、E五种含氮物质相互转化的关系。其中A、B、C、D常温下都是气体,B为红棕色。
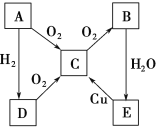
(1)写出下列物质的名称:
B________; E________。
(2)写出各步反应的化学方程式:
①A→C________________________________________;
②D→C________________________________________;
③C→B_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学的知识填空。
(1)已知铜在常温下能被稀HNO3溶解:3Cu + 8HNO3=3Cu(NO3)2 + 2NO↑+ 4H2O
①用双线桥法表示上述电子转移的方向和数目(在化学方程式上标出)______。
②请将上述反应改写成离子方程式:_________________________________________;
③19.2g铜与稀硝酸完全反应,生成的气体在标准状况下的体积为_________________L;若4 mol HNO3参加反应,则该过程转移电子的数目为__________________________。
(2)标准状况下,44.8 L由O2和CO2组成的混合气体的质量为82g,则O2的质量为_________g,该混合气体的平均摩尔质量为_______________________。
(3)3.4g NH3中所含氢原子数目与标准状况下__________ L CH4所含氢原子数相同。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com