
(14分)为了减少CO对大气的污染,某研究性学习小组拟研究利用CO和H2O反应转化为绿色能源H2。已知:
2CO(g)+O2(g)=2CO2(g) △H=—566kJmoL-1
2H2(g)+O2(g)=2H2O(g) △H=—483.6kJmoL-1
H2O(g)=H2O(l) △H=—44.0kJmoL-1
(1)写出CO和H2O(g)作用生成CO2和H2的热化学方程式:___________________________。
(2)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g) 2NH3(g) △H=—92.4kJ/mol
2NH3(g) △H=—92.4kJ/mol
当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示。

①图中t3时引起平衡移动的条件可能是__________________________________________,其中表示平衡混合物中NH3的含量最高的一段时间是_____________。
②温度为T℃时,将1 mol N2和2 mol H2放入容积为0.5 L的密闭容器中,充分反应后测得N2的平衡转化率为50%。则反应在T℃时的平衡常数为____________mol-2·L2。
③目前工业合成氨的原理是:
下图表示随条件改变,平衡体系中氨气体积分数的变化趋势。

当横坐标为压强时,变化趋势正确的是(填序号,下同)__________,当横坐标为温度时,变化趋势正确的是___________。
(3)常温下氨气和HCl均极易溶于水,现将相同体积、相同物质的量浓度的氨水和盐酸混合,所得溶液中各离子的物质的量浓度按照由大到小的顺序排列依次为_______>_______>_______>________。
(每空2分,共14分)(1)CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
(2)①升温 t2-t3 ②4 ③c a
(3)c(Cl-)>c(NH4+)>c(H+)>c(OH-) (顺序正确得2分,顺序有误不得分)
【解析】
试题分析:(1)已知:①2CO(g)+O2(g)=2CO2(g) △H=—566kJmoL-1,②2H2(g)+O2(g)=2H2O(g)△H=—483.6kJmoL-1,则根据盖斯定律可知(①—②)÷2即可得到CO和H2O(g)作用生成CO2和H2的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.2kJ·mol-1。
(2)氢气是合成氨的重要原料,合成氨反应的热化学方程式如下:
N2(g)+3H2(g) 2NH3(g) △H=—92.4kJ/mol
2NH3(g) △H=—92.4kJ/mol
①t3时正逆反应速率均增大,其中逆反应速率大于正反应速率,平衡向逆反应方向进行。由于正方应是体积减小的放热的可逆反应,则引起平衡移动的条件是升高温度。平衡向正反应方向进行,氨气的含量高,因此根据图像可知表示平衡混合物中NH3的含量最高的一段时间是t2-t3。
②温度为T℃时,将1 mol N2和2 mol H2放入容积为0.5 L的密闭容器中,充分反应后测得N2的平衡转化率为50%。则根据方程式可知生成氨气是0.5mol×2=1.0mol,剩余氨气0.5mol,氢气2mol—1.5mol=0.5mol,则反应在T℃时的平衡常数为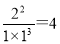 mol-2·L2。
mol-2·L2。
③目前工业合成氨的原理是: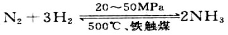
图表示随条件改变,平衡体系中氨气体积分数的变化趋势。当横坐标为压强时,增大压强平衡向正反应方向进行,氨气的含量升高,所以变化趋势正确的是c;当横坐标为温度时,升高温度平衡向逆反应方向进行,氨气的含量降低,则变化趋势正确的是a。
(3)常温下氨气和HCl均极易溶于水,现将相同体积、相同物质的量浓度的氨水和盐酸混合,二者恰好反应生成氯化铵,铵根水解溶液显酸性,则所得溶液中各离子的物质的量浓度按照由大到小的顺序排列依次为c(Cl-)>c(NH4+)>c(H+)>c(OH-) 。
考点:考查盖斯定律、外界条件对平衡状态的影响、平衡常数计算以及浓度大小比较


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列各组在溶液中的反应,不管反应物量的多少,都只能用同一个离子方程式来表示的是
A.NaHCO3与Ca (OH)2 B.Ba(OH)2与H2SO4
C.HCl与NaAlO2 D.AlCl3与NaOH
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三下学期初考理综化学试卷(解析版) 题型:简答题
草酸(H2C2O4)溶液与酸性KMnO4溶液反应时,溶液褪色总是先慢后快,某学习小组探究反应过程中使褪色加快的主要原因,过程如下:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为:
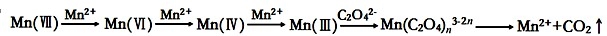
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是 。
【设计、完成实验】
(1)称取 g草酸晶体(H2C2O4·2H2O),配置500mL 0.10mol/L H2C2O4溶液。
①在上述过程中必须用到的2种定量仪器是托盘天平和 。
②下列操作会使所配溶液浓度偏低的是 (填下列选项的字母序号)。
A.称取草酸晶体时,将草酸晶体放在托盘天平右盘
B.定容时俯视刻度线
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
(2)完成探究,记录数据
实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间 (s) | |||
0.10mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50mol/L 稀硫酸 | |||
1 | 30 | 20 | 30 | 20 | 18 | |
2 | 30 | 20 | 30 | 20 | 水浴控制温度65℃ | 15 |
3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
4 | 30 | 20 | x | 20 | 加入5mL 0.10mol/L K2SO4溶液 | 18 |
则x = ,假设2成立。
(3)由于KMnO4能氧化水中有机物等因素,为配制好稳定的KMnO4溶液,其浓度需标定。取10.00 mL 0.10mol/L H2C2O4溶液于锥形瓶中,加入10mL 0.50mol/L 稀硫酸,用(2)中KMnO4溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液4
稀硫酸,用(2)中KMnO4溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液4 0.00 mL,则草酸溶液与酸性KMnO4溶液反应的离子方程
0.00 mL,则草酸溶液与酸性KMnO4溶液反应的离子方程 式为: 。上述实验中KMnO4溶液的物质的量浓度为 。
式为: 。上述实验中KMnO4溶液的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期中化学试卷(解析版) 题型:选择题
下列关干氧化物的各项叙述正确的是
①酸性氧化物不一定是非金属氧化物
②非金属氧化物肯定是酸性氧化物
③碱性氧化物肯定是金属氧化物
④金属氧化物肯定是喊性氧化物
⑤酸性氧化物均可与水反应生成相应的酸
⑥与水反应生成酸的氧化物不一定是酸性氧化物,与水反应生成碱的氧化物不一定是碱住氧化物
⑦不能跟酸反应的氧化物一定能跟碱反应
A.①③⑥ B.①②⑤⑦ C.③④⑤ D.①②⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期期中化学试卷(解析版) 题型:选择题
下列实验过程中,始终无明显现象的是
A.CO2通人到CaCl2溶液中
B.NH3通人AlCl3溶液中
C.用脱脂棉包裹Na2O2粉末露置在潮湿空气中
D.稀盐酸滴加到Fe(OH)3胶体溶液中
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列说法中,正确的是
A.常温下,某NaHSO3溶液的pH<7,则该溶液中c(SO32-)<c(H2SO3)
B.25℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,所消耗溶液体积为:V(醋酸溶液)>V(NaOH溶液)
C.将l mL pH=2的醋酸溶液加水稀释到10 mL,pH变为3
D.常温下,将Na2CO3溶液加水稀释, 的值增大
的值增大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列有关反应的离子方程式的书写中,正确的是
A.C12通入水中:C12+H2O=2H++Cl-+ClO-
B.硫酸铝溶液与过量氨水反应:Al3++3NH3·H2O=3NH4++Al(OH)3↓
C.实验室用石灰石和盐酸反应制取CO2:CO32-+2H+=H2O+CO2↑
D.向Na2SO3溶液中加入稀硝酸:SO32-+2H+=H2O+SO2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北大冶一中等六校高三元月调考理综化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍,稀释后溶液的pH=4
B.25℃时Ksp(AgCl)=1.8×10—10,向AgCl沉淀的溶解平衡体系中加入NaCl固体,AgCl的溶解度可能增大
C.浓度均为0.1 mol·L-1的下列溶液,pH由大到小的排列顺序为:NaOH>Na2CO3>(NH4)2SO4>NaHSO4
D.为确定H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH >7,则H2A是弱酸;若pH<7,则H2A是强酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省淮南市高三一模理综化学试卷(解析版) 题型:填空题
(14分)邻羟基桂皮酸(D)是合成香精的重要原料,下列为合成邻羟基桂皮酸的路线之一

试回答:
(1)A中含氧官能团的名称是 和 。
(2)B→C的反应类型 。
(3)D与过量NaOH溶液反应的化学方程式 。
(4)有机物E与D互为同分异构体,且E有如下特点:
① 是苯的对位取代物, ② 能与NaHCO3反应放出气体 ,③能发生银镜反应。
请写出E的一种结构简式 。
(5)下列说法正确的是 。
a.A的化学式为C7H8O2 b.B能与NaHCO3溶液反应
c.C可能发生聚合反应 d.1mol有机物D最多能与4mol H2加成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com