
�״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ��һ����CO��H2Ϊԭ�Ϻϳɼ״����÷�Ӧ���Ȼ�ѧ����ʽΪ��CO(g)+2H2(g) CH3OH(g) ��H1=��116 kJ��mol��1
CH3OH(g) ��H1=��116 kJ��mol��1
��1�������й�������Ӧ��˵����ȷ����________��
a�����¡����������£������ڵ�ѹǿ�������仯����淴Ӧ�ﵽƽ��
b��һ�������£�H2������������CO���������ʵ�2��ʱ���淴Ӧ�ﵽƽ��
c����������������䣬�����¶ȿ����CO��ת����
d��ʹ�ú��ʵĴ��������̴ﵽƽ���ʱ�䲢���CH3OH�IJ���
��2�����ݻ�Ϊ1L�ĺ��������У��ֱ��о���230�桢250�桢270�������¶��ºϳɼ״��Ĺ��ɡ���ͼ�����������¶��²�ͬ��H2��CO����ʼ��ɱȣ���ʼʱCO�����ʵ�����Ϊ1mol����COƽ��ת���ʵĹ�ϵ��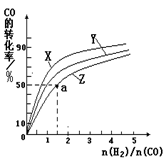
�������������¶��У�����Z��Ӧ���¶��� ��
������ͼ��a���Ӧ�����ݣ�����÷�Ӧ�ڶ�Ӧ�¶��µ�ƽ�ⳣ��K ��д��������̣���
���ڴ����Ӧλ���ϻ�����������Ӧ�ﵽƽ���С��ϵѹǿ���ﵽ�µ�ƽ������У����淴Ӧ������ʱ��ı仯��ϵͼ����ע��
��3����֪��CO(g)+ O2(g)=CO2(g) ��H2=��283 kJ��mol��1
O2(g)=CO2(g) ��H2=��283 kJ��mol��1
H2(g)+ O2(g)=H2O(g) ��H3=��242 kJ��mol��1
O2(g)=H2O(g) ��H3=��242 kJ��mol��1
���ʾ1mol��̬�״���ȫȼ������CO 2��ˮ����ʱ���Ȼ�ѧ����ʽΪ ��
��16�֣�
��1����a��2�֣�
�ڣ�5�֣��⣺����ͼ���֪CO��ת����Ϊ50%��H2�����ʵ���Ϊ1.5mol����
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
����ֵ���ʼŨ��/ mol��L��1 1 1.5 0
����ֵı仯Ũ��/ mol��L��1 0.5 1 0.5
����ֵ�ƽ��Ũ��/ mol��L��1 0.5 0.5 0.5��2�֣�
K=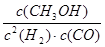 =
=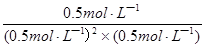 =4L2?mol��2
=4L2?mol��2
��3�֣�K�ı���ʽ���������ݡ������1�֣�������λ���۷֣�
��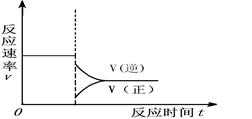
��4�֣����������ֵ㣺���淴Ӧ���ʱ仯������ȷ�����ұ�ע��ȷ����2�֣�������������ƽ̨���ע3Ҫ�أ�3����ȷ��2�֣�2����ȷ��1�֣�1����ȷ��0�֡�����������Ӧ���ʱ仯������ȷ�����ұ�ע��ȷ����2�֣�������������ƽ̨���ע3Ҫ�أ�3����ȷ��2�֣�2����ȷ��1�֣�1����ȷ��0�֡���
��3��CH3OH(g)+3/2O2(g)  CO2(g)+2H2O(g) ��H=��651kJ?mol��1
CO2(g)+2H2O(g) ��H=��651kJ?mol��1
��3�֣�����ʽ��״̬��ȷ1�֡���Ӧ��2�֣���λ��©��1�֣�
���������������1������CO(g)+2H2(g) CH3OH(g)������Ӧ���������ʵ�����С�ķ������ŷ�Ӧ��������У������������ܵ����ʵ�����С����˺��¡����������£������ڵ�ѹǿ��С����ѹǿ���ٱ仯��˵�������������ܵ����ʵ������ֲ��䣬��Ӧ�ﵽƽ�⣬��a��ȷ���������������ʺ�CO���������ʶ�������Ӧ���ʣ�����֮��ʼ�յ���ϵ��֮�ȣ�ȱ���淴Ӧ���ʣ���b����CO(g)+2H2(g)
CH3OH(g)������Ӧ���������ʵ�����С�ķ������ŷ�Ӧ��������У������������ܵ����ʵ�����С����˺��¡����������£������ڵ�ѹǿ��С����ѹǿ���ٱ仯��˵�������������ܵ����ʵ������ֲ��䣬��Ӧ�ﵽƽ�⣬��a��ȷ���������������ʺ�CO���������ʶ�������Ӧ���ʣ�����֮��ʼ�յ���ϵ��֮�ȣ�ȱ���淴Ӧ���ʣ���b����CO(g)+2H2(g) CH3OH(g)����H1=��116 kJ��mol��1��˵������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�������Ȼ��淴Ӧ�����ƶ�����CO��ת���ʼ�С����c������������ʹƽ���ƶ������Լӿ췴Ӧ���ʣ����ʹ�ô��������̴ﵽƽ���ʱ�䣬���Dz������CH3OH�IJ�������d������2���ٺϳɼ״������Ƿ��ȷ�Ӧ�������¶�ƽ�������Ȼ��淴Ӧ�����ƶ���CO��ƽ��ת���ʼ�С����CO��ת����ԽС����Ӧ�¶�Խ�ߣ�ͼ��n(H2)/n(CO)���ֲ���ʱ��CO��ƽ��ת���ʣ�X>Y>Z��������Z��Ӧ���¶���270�棻�ڶ�ͼ�ɵã�a��ĺ�����n(H2)/n(CO)=1.5��������CO��ƽ��ת����Ϊ50%������ʼʱn(CO)=1mol����n(H2)=1.5mol����
CH3OH(g)����H1=��116 kJ��mol��1��˵������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�������Ȼ��淴Ӧ�����ƶ�����CO��ת���ʼ�С����c������������ʹƽ���ƶ������Լӿ췴Ӧ���ʣ����ʹ�ô��������̴ﵽƽ���ʱ�䣬���Dz������CH3OH�IJ�������d������2���ٺϳɼ״������Ƿ��ȷ�Ӧ�������¶�ƽ�������Ȼ��淴Ӧ�����ƶ���CO��ƽ��ת���ʼ�С����CO��ת����ԽС����Ӧ�¶�Խ�ߣ�ͼ��n(H2)/n(CO)���ֲ���ʱ��CO��ƽ��ת���ʣ�X>Y>Z��������Z��Ӧ���¶���270�棻�ڶ�ͼ�ɵã�a��ĺ�����n(H2)/n(CO)=1.5��������CO��ƽ��ת����Ϊ50%������ʼʱn(CO)=1mol����n(H2)=1.5mol����
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
����ֵ���ʼŨ��/ mol��L��1 1 1.5 0
����ֵı仯Ũ��/ mol��L��1 0.5 1 0.5
����ֵ�ƽ��Ũ��/ mol��L��1 0.5 0.5 0.5
K=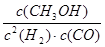 =
=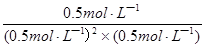 =4L2?mol��2
=4L2?mol��2
�ۻ�ͼҪ�㣺a������CO(g)+2H2(g) CH3OH(g)������Ӧ�����������С�ķ����������������С��ϵѹǿʱ��ƽ�����������������淴Ӧ�����ƶ������淴Ӧ���ʴ�������Ӧ���ʣ�b�����ڷ�Ӧ��������������������������С��������Ӧ���ʺ��淴Ӧ���ʾ����Լ�С��c���ﵽ��ƽ��֮ǰ���淴Ӧ������С������Ӧ������������Ϊƽ�����淴Ӧ�����ƶ���������Ũ����С����Ӧ��Ũ������������ԭƽ���С��d���ﵽ��ƽ��ʱ������Ӧ���ʺ��淴Ӧ������ȣ�������ԭƽ���С����3���Ƚ���֪�����Ȼ�ѧ����ʽ���Ϊ�٢ڢۣ��ٸ��ݸ�˹���ɣ��ɢ�+�ۡ�2���ٿɵã�CH3OH(g)+3/2O2(g)
CH3OH(g)������Ӧ�����������С�ķ����������������С��ϵѹǿʱ��ƽ�����������������淴Ӧ�����ƶ������淴Ӧ���ʴ�������Ӧ���ʣ�b�����ڷ�Ӧ��������������������������С��������Ӧ���ʺ��淴Ӧ���ʾ����Լ�С��c���ﵽ��ƽ��֮ǰ���淴Ӧ������С������Ӧ������������Ϊƽ�����淴Ӧ�����ƶ���������Ũ����С����Ӧ��Ũ������������ԭƽ���С��d���ﵽ��ƽ��ʱ������Ӧ���ʺ��淴Ӧ������ȣ�������ԭƽ���С����3���Ƚ���֪�����Ȼ�ѧ����ʽ���Ϊ�٢ڢۣ��ٸ��ݸ�˹���ɣ��ɢ�+�ۡ�2���ٿɵã�CH3OH(g)+3/2O2(g)  CO2(g)+2H2O(g) ��H=��651kJ?mol��1��
CO2(g)+2H2O(g) ��H=��651kJ?mol��1��
���㣺���黯ѧ��Ӧԭ�����漰��ѧƽ��ı�־�����������ƽ���ƶ���Ӱ�졢����ѧƽ�ⳣ���ļ��㡢���ȷ�Ӧ�����ȷ�Ӧ���¶ȶ�ƽ���ƶ���Ӱ�졢����ѹǿ�Է�Ӧ���ʺ�ƽ���ƶ���ͼ��˹���ɡ��Ȼ�ѧ����ʽ�ȡ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������һ����ࡢ��Ч��������Դ��
I.�ü�����ȡ�����ķ�Ӧ��Ϊ�������������仯����ͼ��ʾ��
��1�������ˮ������Ӧ���ɶ�����̼���������Ȼ�ѧ����ʽ�� ��
II.���ݻ�Ϊ1L���ܱ������ڣ�����0.1molCO��0.1molH2O���ڴ������ڵ������¸��¼���ʹ�䷴Ӧ�����CO2��Ũ����ʱ��仯��ͼ����ͼ��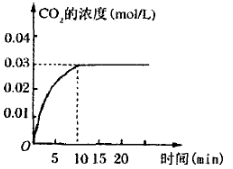
��2���ڸ��¶��£��ӷ�Ӧ��ʼ���ﵽƽ��ʱ��CO��ƽ����Ӧ����Ϊ ��
��3�����¶��£��˷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ�������÷�����ʾ�� ��
��4�����иı��У���ʹƽ��������Ӧ�����ƶ����� ��
| A�������¶� | B������ѹǿ |
| C������H2O��g����Ũ�� | D������CO2��g����Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�о�CO2��CH4����Ӧʹ֮ת��ΪCO��H2���Լ���ȼ��Σ������С����ЧӦ������Ҫ�����塣
��1����֪��2CO��g��+O2��g����2CO2��g�� ��H����566kJ/mol
2H2��g��+O2��g����2H2O��g�� ��H����484kJ/mol
CH4��g��+2O2��g����CO2��g��+2H2O��g�� ��H����890kJ/mol
��CH4��g��+CO2��g����2CO��g��+2H2��g����H��____________��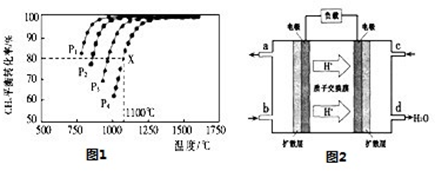
(2)���ܱ�������ͨ�����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L��CH4��CO2����һ�������·�����ӦCH4��g��+CO2��g����2CO��g��+2H2��g�������CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ1��
��������ʵ��˵���÷�Ӧһ���ﵽƽ����� ��
a��CO2��Ũ�Ȳ��ٷ����仯
b��������CH4����2������CO��
c����������ƽ����Է��������������仯
d��CO��H2�����ʵ�����Ϊ1:1
�ھ�ͼ��֪��P1��P2��P3��P4�ɴ�С��˳��Ϊ ��
����ѹǿΪP4��1100��������£��÷�Ӧ5minʱ�ﵽƽ��x�㣬����CO��ʾ�÷�Ӧ������Ϊ �����¶��£���Ӧ��ƽ�ⳣ��Ϊ ��
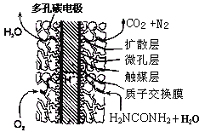
(3)��CO��H2�ɺϳɼ״�(CH3OH)���Լ״���������Ӧ�Ƴɵ�ȼ�ϵ����ͼ2��ʾ���õ�ع�������O2Ӧ�� (�c��һb��)��ͨ�ˣ���ظ�����ӦʽΪ �����øõ�ص�⾫��ͭ��ÿ�õ�6. 4gͭ��ת�Ƶ�����ĿΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�ϳɰ�Ȼ������������������Ҫ�Ļ���������
I����3��2 L���ܱ������У�����ͬ���¶��¡�ʹ����ͬ�Ĵ����ֱ���з�Ӧ��
3H2(g) + N2(g) 2NH3(g)������ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ�й��������£�
2NH3(g)������ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ�й��������£�
| �� | �� | �� | ||
| ��Ӧ��Ͷ���� | 3 mol H2��2 mol N2 | 6 mol H2��4mol N2 | 2 mol NH3 | ||
| �ﵽƽ���ʱ��/min | | 5 | 8 | ||
| ƽ��ʱN2��Ũ��/mol��L��1 | c1 | 1.5 | | ||
| NH3��������� | ��1 | | ��3 | ||
| ��������ܶ�/g��L��1 | ��1 | ��2 | |
 H2NCOONH4 (l) (���������) ��H1
H2NCOONH4 (l) (���������) ��H1 H2O(l)��H2NCONH2(l) ��H2
H2O(l)��H2NCONH2(l) ��H2 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��������Ҫ�Ļ�����Ʒ֮һ��
��1���ϳɰ��õ��������Լ���Ϊԭ���Ƶá��йػ�ѧ��Ӧ�������仯����ͼ��ʾ��
��Ӧ�٢ڢ�Ϊ_________��Ӧ������ȡ����ȡ�����CH4(g)��H2O(g)��Ӧ����CO(g)��H2(g)���Ȼ�ѧ����ʽΪ__________________��
�� �� ��
��2���ð�����ȡ����[CO(NH2)2]�ķ�ӦΪ��2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)��
CO(NH2)2(l)+H2O(g)��
��ij�¶��£����ݻ�Ϊ10L���ܱ�������ͨ��2mol NH3��1molCO2����Ӧ�ﵽƽ��ʱCO2��ת����Ϊ50%���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=___________�����¶���ƽ�ⳣ��K�ļ�����Ϊ____________��
��Ϊ��һ�����CO2��ƽ��ת���ʣ����д�ʩ���ܴﵽĿ�ĵ���_____________
| A�����NH3��Ũ�� | B������ѹǿ |
| C����ʱת�����ɵ����� | D��ʹ�ø���Ч�Ĵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
50mL0.50mol�� L��1������50mL0.55mol��L��1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺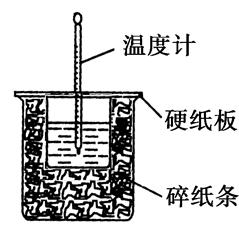
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ���������________��
��2���ձ���������ֽ����������____________________��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ________���ƫ��ƫС������Ӱ�족��
��4��ʵ���и���60mL 0.50mol��L��1�����50mL0.55mol��L��1NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������________�����ȡ�������ȡ����������к���________�����ȡ�������ȡ�������������_____________________________________��
��5������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��____________����50mL 0.50mol��L��1NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��________�������ƫ��ƫС������Ӱ�족��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��50 mL 0.50 mol/L��������50 mL 0.55 mol/L������������Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺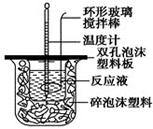
��1���ձ�����������ĭ���ϵ�������___________________________
��2�����β���������ܷ��û������ʽ�������棿_____(��ܡ����ܡ�)��
��ԭ����_______________________________________________________��
��3��ʵ��ʱ����������Һ��Ũ��Ҫ��0.55 mol/L��ԭ����______________________��
ʵ����������60 mL 0.50 mol/L��������50 mL 0.55 mol/L������������Һ���з�Ӧ�� ������ʵ����ȣ����ų�������_______ _____(���ȡ�������ȡ�)����ʵ���������ȷ���������к���________________(���ȡ�������ȡ�)��
��4����֪��ϡ��Һ�У�ǿ���ǿ����кͷ�Ӧ����1 mol H2Oʱ���ų�57.3 kJ����������������Ӧ���Ȼ�ѧ����ʽΪ��__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
80��ʱ,2L�ܱ������г���0��40molN2O4,������Ӧ
N2O4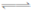 2NO2
2NO2 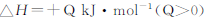 ,�����������:
,�����������: 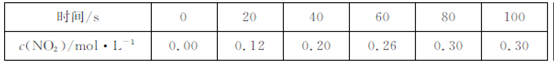 �����ж���ȷ����
�����ж���ȷ����
| A�������¶ȸ÷�Ӧ��ƽ�ⳣ��K��С |
B��20~40s��,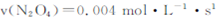 |
| C����Ӧ��ƽ��ʱ,���յ�����Ϊ0��30QkJ |
| D��100sʱ��ͨ��0��40molN2O4,����ƽ��ʱN2O4��ת�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ���¶��£�ij�ܱ�����������·�Ӧ��CO(g)+H2O(g)  CO2(g)+H2(g) ������ӦΪ���ȷ�Ӧ��������Ӧ�ﵽƽ��ʱ����������и����ʵ����ʵ�����Ϊ n mol����ʹH2�����ʵ���Ũ������1������������������ʱ�����д�ʩ�ɲ��õ��ǣ� ��
CO2(g)+H2(g) ������ӦΪ���ȷ�Ӧ��������Ӧ�ﵽƽ��ʱ����������и����ʵ����ʵ�����Ϊ n mol����ʹH2�����ʵ���Ũ������1������������������ʱ�����д�ʩ�ɲ��õ��ǣ� ��
�������¶� ������ѹǿ
����ͨ��n mol CO2��n mol H2 ���ټ���2n mol CO��2n mol H2O(g)
| A���٢� | B���ڢ� | C���ۢ� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com