
【题目】可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。医院抢救钡离子中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:Ksp(BaCO3)=5.1×10-9 mol2·L-2;Ksp(BaSO4)=1.1×10-10 mol2·L-2。下列推断正确的是( )
A. 不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4)
B. 抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替
C. 若误饮[Ba2+]=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
D. 可以用0.36 mol·L-1的Na2SO4溶液给钡离子中毒患者洗胃
【答案】D
【解析】
A.胃液中为盐酸环境,难溶碳酸盐在胃液中溶解,故不能用碳酸钡作为内服造影剂,故A错误;B.在酸性环境下,用碳酸钠溶液不能沉淀出钡离子,故B错误;C.硫酸钡作内服造影剂说明硫酸钡电离出的钡离子浓度是安全的,此时c(Ba2+)= ![]() =1.05×10-5mol/L>1.0×10-5mol/L,故误饮c(Ba2+)=1.0×10-5mol/L的溶液时,不会引起钡离子中毒,故C错误;D. 当用0.36 mol/L的Na2SO4溶液洗胃时,胃液中c(Ba2+)=Ksp(BaSO4)÷c(SO42-)=(1.1×10-10÷0.36) mol/L=3.1×10-10mol/L<1.05×10-5mol/L,故D正确;答案选D。
=1.05×10-5mol/L>1.0×10-5mol/L,故误饮c(Ba2+)=1.0×10-5mol/L的溶液时,不会引起钡离子中毒,故C错误;D. 当用0.36 mol/L的Na2SO4溶液洗胃时,胃液中c(Ba2+)=Ksp(BaSO4)÷c(SO42-)=(1.1×10-10÷0.36) mol/L=3.1×10-10mol/L<1.05×10-5mol/L,故D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)![]() 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是

A. 图中a点的值为0.15 B. 该反应的平衡常数K=0.03
C. 温度升高,平衡常数K值减小 D. 平衡时A2的转化率为62.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查得N≡N键能为945.6 kJ·mol-1、H—N键能为391 kJ·mol-1。已知氮气与氢气化合生成2 mol氨气时放出的能量为92.4 kJ。则H—H键的键能是( )
A. 45 kJ·mol-1B. 436 kJ·mol-1
C. 1 308 kJ·mol-1D. 135 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如下图所示。下列说法正确的是( )
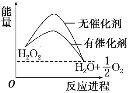
A. 加入催化剂,减小了反应的热效应
B. 加入催化剂,可提高H2O2的平衡转化率
C. H2O2分解的热化学方程式:H2O2===H2O+1/2 O2 ΔH>0
D. 反应物的总能量高于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二钴(Co2O3)常用于制滤光眼镜的添加剂、催化剂和氧化剂。以含钴废料(主要成分CoO、Co2O3,含有少量MnO2、NiO、Fe3O4)为原料制备Co2O3的流程如下:
(1)研磨的目的是____________。滤渣1的主要成分为______________(填化学式)。
(2)酸浸时双氧水的作用有___________。不能用盐酸代替硫酸,因为Co2O3与盐酸反应生成Cl2,污染境,该反应的离子方程式为__________。

(3)在实验室里,萃取操作要用到的玻璃仪器主要有___________。有机相再生时提取出的Ni2+可用于制备氢镍电池,该电池充电时的总反应为Ni(OH)2+M![]() NiOOH+MH。则放电时正极的电极反应式为__________。
NiOOH+MH。则放电时正极的电极反应式为__________。
(4)沉钴时发生反应的离子方程式为_______。煅烧时发生反应的化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如图所示。反应原理为:CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法正确的是

A. b为正极,电极反应式为:O2+4H++4e-=2H2O
B. 电解质溶液中的H+移向a电极
C. 若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
D. 呼出气体中酒精含量越高,微处理器中通过的电流越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求作答:
(1)FeCl3水溶液呈酸性,原因是(用离子方程式表示):___________________,实验室配制FeCl3溶液的方法是__________________________。
(2)泡沫灭火剂中装有Al2(SO4)3溶液、NaHCO3溶液及起泡剂,写出使用时发生反应的离子方程式____________________________
(3)写出难溶电解质的溶度积表达式,Mg(OH)2:____________;在Mg(OH)2悬浊液中加入MgCl2固体,平衡________移动(填“正向”“逆向”或“不”),Ksp________(填“增大”“减小”或“不变”)。
(4)1 g炭与水蒸气反应生成CO和H2,需吸收a kJ热量,此反应的热化学方程式为______________________________________________。
(5)火箭发射时可用肼(N2H4)为燃料,以二氧化氮做氧化剂,它们相互反应生成氮气和水蒸气。已知:N2(g)+2O2(g)===2NO2(g),ΔH=+67.7 kJ·mol-1;N2H4(g)+O2(g)===N2(g)+2H2O(g),ΔH=-534 kJ·mol-1,则N2H4和NO2反应的热化学方程式___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com