
(12分)如图为100mL 2mol /L 的AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线。试回答:
(1) A点时已参加反应的AlCl3和 NaOH的物质的量之比为1比 。
(2) AB段曲线所表示的反应的离子方程式是___________________。
(3) B处溶液中存在的物质的量浓度最大的离子是 (填离子符号)。向B处生成的溶液中通入二氧化碳,可见到的现象是 。
(4)如在该AlCl3溶液中生成7.8克沉淀,则消耗的氢氧化钠的物质的量为 mol或 mol。
(12分,每空2分) (1)3;
(2) Al(OH)3+OH-=AlO2-+2H2O;
(3) Na+ ;生成白色沉淀。
(4)0.3mol或0.7mol
解析:A点沉淀达最大量,此时下列反应刚好完成:
AlCl3+3NaOH=Al(OH)3↓+3NaCl, AB段曲线所表
示的反应是沉淀刚好溶解:Al(OH)3+NaOH=NaAlO2+2H2O,离子反应为
Al(OH)3+OH-=AlO2-+2H2O;因此B处溶液中存在的物质是NaCl、NaAlO2浓度最大的离子是Na+,向B处生成的溶液中通入二氧化碳发生如下反应:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3,有白色沉淀产生;
⑷当氢氧化钠量少:AlCl3+3NaOH=Al(OH)3↓+3NaCl
3mol 78g
n 7.8g n=0.3mol
当氢氧化钠量多,AlCl3全部反应产生沉淀,后沉淀溶解一部分
AlCl3+3NaOH=Al(OH)3↓+3NaCl
1mol 3mol 78g
0.2mol n m n=0.6mol m=15.6g
Al(OH)3+NaOH=NaAlO2+2H2O
78g 1mol
15.6g-7.8g n1 n1=0.1mol,则消耗的氢氧化钠的物质的量为0.6mol+0.1mol=0.7mol。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
| 氢氧化钠溶液 分子式:NaOH 相对分子质量:40 密度:1.2g?cm-3 质量分数:20%(1)该NaOH溶液的物质的量浓度为 6 6 mol/L.(2)现在要配制该浓度的NaOH溶液100ml,需称量 24.0 24.0 g固体氢氧化钠.溶液配制的所需的基本步骤如下: (3)将上述实验步骤A到F按实验过程先后次序排列 CBDFAE CBDFAE .(4)上述实验步骤A、B、E、F都用到的仪器名称为 100ml容量瓶 100ml容量瓶 .(5)下列操作对NaOH溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“无影响”). ①摇匀后发现液面低于刻度线再加水 偏低 偏低 ;②容量瓶中原有少量蒸馏水 无影响 无影响 ;③定容时俯视观察液面 偏高 偏高 .
查看答案和解析>> 科目:高中化学 来源: 题型:阅读理解 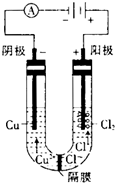 如图为细菌冶铜和火法冶铜的主要流程. 如图为细菌冶铜和火法冶铜的主要流程.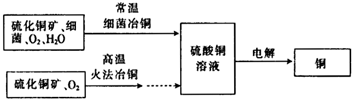 (1)①写出用惰性电极电解硫酸铜溶液的化学方程式: ②若电解一定时间后,外加0.1mol的氢氧化铜可使电解液恢复到电解前的浓度,电路中转移电子物质的量 (2)细菌冶金又称微生物浸矿,是近代湿法冶金工业上的一种新工艺.细菌冶铜与火法冶铜相比,优点为 (3)用惰性电极分别电解浓的氯化铜溶液和硫酸铜溶液.电解浓的氯化铜溶液时发现阴极有金属铜生成,同时阴极附近会出现棕褐色溶液.而电解硫酸铜溶液时,没有棕褐色溶液生成.下面是关于棕褐色溶液成分的探究: ①有同学认为,阴极附近出现的棕褐色溶液是氯气反应的结果,你认为他的猜测是否正确? 资料1: 一般具有混合价态(指化合物中同一元素存在两种不同的化合价,如Fe3O4中的Fe元索)的物质的颜色比单一价态的物质的颜色要深. 资料2: CuCl微溶于水,能溶于浓盐酸. ②猜想:棕褐色溶液中可能含有的离子是 ③验证猜想:完成实验方案(配制棕褐色溶液).取少量 ④已知电解前,U形管中加入了100mL 0.5mol?L-1 CuCl2溶液,电解结朿时电路中一共转移了0.03mol电子,且阴极生成0.64g铜,则形成的低价阳离子的物质的量为 查看答案和解析>> 科目:高中化学 来源:2011—2012学年江苏省淮安中学高一上学期期末考试化学试卷(带解析) 题型:计算题 (12分)如图为100mL 2 mol /L 的AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线。试回答: 查看答案和解析>> 科目:高中化学 来源:2014届江苏省高一上学期期末考试化学试卷(解析版) 题型:计算题 (12分)如图为100mL 2 mol /L 的AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与NaOH的物质的量之间的关系曲线。试回答:
(1) A点时已参加反应的AlCl3和 NaOH的物质的量之比为1比 。 (2) AB段曲线所表示的反应的离子方程式是___________________。 (3) B处溶液中存在的物质的量浓度最大的离子是 (填离子符号)。向B处生成的溶液中通入二氧化碳,可见到的现象是 。 (4)如在该AlCl3溶液中生成7.8克沉淀,则消耗的氢氧化钠的物质的量为 mol或 mol。
查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |