
【题目】铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物。
(1)铁炭混合物在水溶液中可形成许多微电池。将含有Cr2O72-的酸性废水通过铁炭混合物,在微电池正极上Cr2O72-转化为Cr3+,其电极反应式为_____________。
(2)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示0。
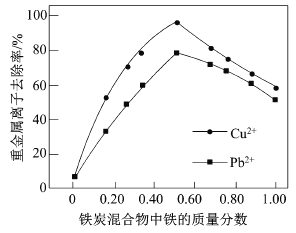
①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是__________。
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是_____________。
(3)纳米铁粉可用于处理地下水中的污染物。
①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为 。
②纳米铁粉与水中NO3-反应的离子方程式为4Fe+NO3-+10H+=4Fe2++NH4++3H2O
研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是 。
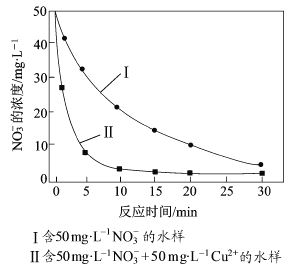
③相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异(见右图),产生该差异的可能原因是 。
【答案】(1)Cr2O72-+6e-+14H+=2Cr3++7H2O;(2)①活性炭对Cu2+和Pb2+有吸附作用
②铁的质量分数增加,铁炭混合物中微电池数目减少;
(3)①2Fe2++BH4-+4OH-=2Fe+ B(OH)4-+2H2↑;②纳米铁粉与H+反应生成H2;
③Cu或Cu2+催化纳米铁粉去除NO3-的反应(或形成的Fe-Cu原电池增大纳米铁粉去除NO3-的反应速率)。
【解析】
试题分析:(1)混合物在水溶液中可形成许多微电池。将含有Cr2O72-的酸性废水通过铁炭混合物,在微电池正极上Cr2O72-获得电子,被还原产生Cr3+,则正极上发生的电极反应式为Cr2O72-+6e-+14H+=2Cr3++7H2O;
(2)①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,原因是活性炭是酥松多孔的物质,表面积大,吸附力强,可以吸附水中少量的Cu2+和Pb2+,从而可以降低水中Cu2+和Pb2+的浓度;
②铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,铁炭混合物中微电池数目减少,因此Cu2+和Pb2+的去除率不升反降;
(3)①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,根据电子守恒、电荷守恒及原子守恒,可得反应的离子方程式为2Fe2++BH4-+4OH-=2Fe+ B(OH)4-+2H2↑;
②纳米铁粉与水中NO3-反应的离子方程式为4Fe+ NO3-+10H+=4Fe2++NH4++3H2O,若pH偏低,则溶液的酸性增强,会发生反应:Fe+2H+=Fe2++ H2↑;导致NO3-的去除率下降;
③根据图像可知,相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异,可能是由于Cu或Cu2+催化纳米铁粉去除NO3-的反应(或形成的Fe-Cu原电池增大纳米铁粉去除NO3-的反应速率)。


科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
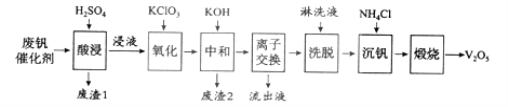
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”“碱”“中”)。
R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”“碱”“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机推断题。有机物G是一种医药中间体,可通过如图所示路线合成。A的产量是衡量一个国家石油化工发展水平的重要标志,H的分子式是C7H8。
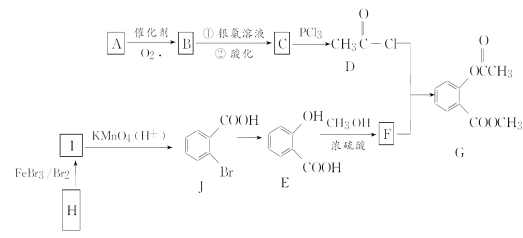
已知:![]()
请回答以下问题:
(1)A的结构简式是________。
(2)H→I的化学反应方程式为___ _____,
E→F的化学方程式为_________________ ______________。
(3)C→D的反应类型是________,I→J的反应类型是________。
(4)两个E分子在一定条件下发生分子间脱水生成一种环状酯的结构简式是_________。
(5)满足以下条件的F的同分异构体还有________种(不包含F)。
①能与氯化铁溶液发生显色反应
②红外光谱等方法检测分子中有“COO”结构
③苯环上有两个取代基
其中能与碳酸氢钠溶液反应且核磁共振氢谱测定有5个吸收峰的同分异构体的结构简式为
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】19世纪中叶,俄国化学家门捷列夫( )
A. 提出了原子分子学说 B. 提出了元素周期律
C. 制出了第一张元素周期表 D. 发现了质量守恒定律
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[实验化学]
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中、受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。
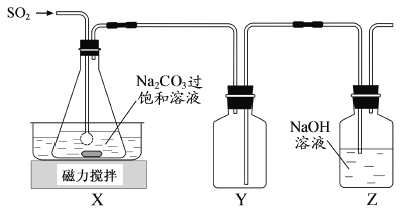
当溶液pH约为4时,停止反应,在20℃左右静置结晶。生成Na2S2O5的化学方程式为
2NaHSO3=Na2S2O5+H2O
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为____________________。
(2)装置Y的作用是______________________________。
(3)析出固体的反应液经减压抽滤、洗涤、25℃~30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、________________和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体。用饱和SO2水溶液洗涤的目的是______。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是 ( )
A. 利用质谱法
B. 利用红外光谱法
C. 利用核磁共振氢谱
D. 利用金属钠或者金属钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平衡反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3 H2(g)![]() CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2(g)+ H2(g)![]() CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,经过相同反应时间测得如下实验数据:

【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醛的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)![]() H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K= ;反应II的ΔH2= kJ·mol-1。
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有 。
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是 。
(4)在右图中分别画出I在无催化剂、有Cat.1和由Cat.2三种情况下“反应过程-能量”示意图。

(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在___ 极,该电极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质中杂质(括号内为杂质)的检验、除杂的试剂或方法都正确的是( )
选项 | 物质及其杂质 | 检验方法 | 除杂 |
A | Cl2(HCl) | 通入AgNO3溶液中 | 饱和食盐水 |
B | FeCl2溶液(FeCl3) | 滴入KSCN溶液 | 通入过量氯气 |
C | 苯(苯酚) | 滴入FeCl3溶液 | 碱洗分液 |
D | KNO3晶体(NaCl) | 焰色反应 | 重结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A为缓释阿司匹林的主要成分。用于内燃机润滑油的有机物Y 和用于制备水凝胶的聚合物P 的合成路线如下。

已知:
(1)D 的分子式为C7H6O3,D 中所含的官能团是 。
(2)D→Y的化学方程式是 。
(3)反应Ⅰ的另一种产物是M,其相对分子质量是60,B 、M 均能与NaHCO3反应产生CO2。
①M 是 。
②B→D的化学方程式是 。
(4)下列说法正确的是 。
a.B、C、D中均含有酯基
b.乙二醇可通过![]() 的路线合成
的路线合成
c.C能与饱和溴水反应产生白色沉淀
(5)红外光谱测定结果显示,E 中不含羟基。
①X→E的反应类型是 。
② E的结构简式是 。
(6)若X的聚合度n=1,有机物A 只存在一种官能团,A 的结构简式是 。
(7)聚合物P的结构简式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com