
在第3周期中,置换酸中氢的能力最强的元素的元素符号为 ,化学性质最稳定的元素符号是 ,最高价氧化物的水化物的酸性最强的化合物的化学式是 ,最高价氧化物的水化物的碱性最强的化合物的化学式是 ,显两性的氢氧化物的化学式是 ,该两性氢氧化物与盐酸、氢氧钠溶液分别反应的离子方程式为 、 ,原子半径最大的金属元素的名称是 ,离子半径最小的离子结构示意图是 。
【考点】本题考查同周期元素性质的递变规律,题目难度不大,注意加强对基础知识的积累。
【解析】同周期元素从左到右元素的金属性逐渐减弱,非金属性逐渐增强,则置换酸中氢的能力最强的元素为金属性最强的元素为Na;碱性最强的化合物为NaOH;化学性质最稳定的元素为0族元素,第三周期元素为Ar;最高价氧化物的水化物的酸性最强的化合物对应的元素为Cl元素,对应的酸为HClO4;第三周期中的两性氢氧化物为Al(OH)3;与盐酸、氢氧化钠溶液分别反应的离子方程式为:Al(OH)3+3H+=Al3++3H2O、Al(OH)3+3OH-=[Al(OH)4]-;同周期元素从左到右元素原子半径逐渐减小,则原子半径最大的是Na;离子半径最小的离子为Al3+,离子结构示意图是 。
。
【答案】Na Ar HClO4 NaOH Al(OH)3 Al(OH)3 +3H+ =Al3+ +3H2O Al(OH)3 +OH― = AlO2― +2H2O 钠 


科目:高中化学 来源: 题型:
关于乙醇结构方面的说法中正确的是( )
A.乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH-而显碱性
B.乙醇与乙酸反应生成乙酸乙酯,所以乙醇显碱性
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
查看答案和解析>>
科目:高中化学 来源: 题型:
根据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池如图所示,其中盐桥为琼脂-饱和KNO3盐桥。
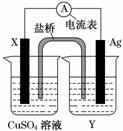
请回答下列问题:
(1)电极X的材料是________;电解质溶液Y是________;
(2)银电极为电池的____极,写出两电极的电极反应式:
银电极:____________;X电极:____________。
(3)外电路中的电子是从______电极流向______电极。
(4)盐桥中向CuSO4溶液中迁移的离子是________(填序号)。
A.K+ B.NO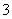
C.Ag+ D.SO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列性质的递变中,正确的是
A.O、Na、S的原子半径依次增大 B.LiOH、KOH、CsOH的碱性依次增强
C.HF、NH3、SiH4的稳定性依次增强 D.HCl、HBr、HI的还原性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
将纯锌片和纯铜片按下图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的酸性均减弱
D.产生气泡的速率甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)甲烷通常用来作燃料,其燃烧反应的化学方程式是 。
(2) 若用甲烷—氧气构成燃料电池,电解质溶液为KOH溶液,试写出该电池的
正极的电极反应式 ;
负极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
I:CH4 ( g ) + H2O ( g )=CO ( g ) + 3H2 ( g )
II:CO ( g ) + 2H2 ( g )=CH3OH ( g )
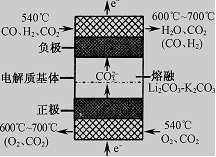
(1)反应(I)制得的混合气体和水煤气成分相同,也能形成燃料电池。下图是利用其作原料,采用熔融碳酸盐为电解质的燃料电池工作原理示意图,则该电池的负极反应式可表示为:
。
(2)在使用甲醇时,若有残留,对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。实验室用下图装置模拟上述过程:
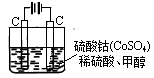
①写出阳极电极反应式 。
②写出除去甲醇的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,10mL浓度为amol·L-1的醋酸溶液pH=4。下列能使溶液的pH=7的措施是
A.将溶液稀释到 10L
B.将溶液与10mL浓度为amol·L-1的NaOH溶液混合
C.将溶液与10mL、pH=10的NaOH溶液混合
D.往溶液中加入适量的氢氧化钠,使溶液中c(Na+)=c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
向物质的量相等的硫酸铝和硫酸铵溶于水形成的混合溶液中逐滴加入氢氧化钠溶液直至过量。下列表示氢氧化钠溶液加入的体积(X)与溶液中沉淀的量(Y)的关系示意图中正确的是
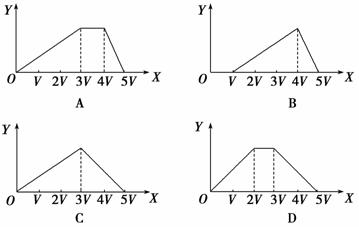
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com