
【题目】在一个绝热的固定容积的密闭容器中发生可逆反应:mA(g)+nB(g)![]() pC(g)+qD(g),当m、n、p、q为任意整数时,达到平衡的标志是
pC(g)+qD(g),当m、n、p、q为任意整数时,达到平衡的标志是
①体系的压强不再改变 ②体系的温度不再改变 ③各组分的浓度不再改变 ④各组分的质量分数不再改变 ⑤反应速率v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q ⑥单位时间内m mol A断键反应,同时p mol C也断键反应 ⑦混合气体的密度不再改变
A.③④⑤⑥⑦ B.②③④⑥ C.①③④⑤ D.①③④⑥⑦
【答案】B
【解析】①当m+n=p+q时,任何时刻体系的压强都保持不变,故体系的压强不再改变不能作为判断反应是否达平衡的标志;②由于是绝热容器,体系的温度不再改变时,反应物的转化率恒定,体系内各物质的浓度不变,反应达平衡;③由于容器的容积恒定,各组分的浓度不再改变时,各组分的物质的量保持不变,反应达平衡;④各组分的质量分数不再改变,各组分的浓度也不再改变,反应达平衡;⑤任何时刻关系式v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q均成立,不能作为判断反应是否达平衡的标志;⑥单位时间内m mol A断键反应,同时p mol C也断键反应,说明A的消耗量与A的生成量相等,浓度维持不变,反应达平衡;⑦由于容器容积和气体总质量不变,所以混合气体的密度任何时刻都不会变,不能据此判断反应是否建立平衡。故选项B符合。


科目:高中化学 来源: 题型:
【题目】用如图所示装置进行如下实验:
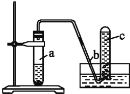
(1)在检查装置的气密性后,向试管a中加入10 mL 6 mol·L-1的稀硝酸和1 g铜片,立即用带有导管的橡皮塞塞紧试管口。请写出在试管a中有可能发生的反应的化学方程式_____________________、_____________________。
(2)在实验过程中常常反应开始时速率缓慢,随后逐渐加快,这是由于______________________,当反应进行一段时间后速率又逐渐减慢,原因是_____________________________。
(3)欲较快地制得NO,可采取的措施是____________ (填写字母序号)。
A.加热 B.使用铜粉 C.稀释HNO3 D.增大硝酸的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应与能量的说法正确的是
A. Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) △H=-216kJ/mol,E反应物< E生成物
B. CaCO3(s)=CaO(s)+CO2(g) ΔH=+178.2kJ·mol-1,E反应物< E生成物
C. HCl(g)=1/2H2(g)+1/2Cl2(s) ΔH=+92.3 kJ·mol-1,1 mol HCl在密闭容器中分解达平衡后放出92.3 kJ的能量
D. 将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g) ![]() 2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式中,书写正确的是
A.实验室用大理石跟稀盐酸制取二氧化碳:2H+ + CO32- = CO2↑+ H2O
B.将铝粉投入氢氧化钠溶液中: 2Al + 2OH- = 2AlO2- + H2↑
C.铁粉与氯化铁溶液反应:Fe + Fe3+ = 2Fe2+
D.金属钠与水反应:2Na + 2H2O = 2Na+ + 2OH-+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 碳酸钠可用于去除餐具的油污B. 氢氧化铝可用于中和胃酸过多
C. 二氧化硅可用作计算机芯片D. 铝合金大量用于高铁建设
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com