
【题目】下列反应的离子方程式不正确的是( )
A.NaOH加入NaHCO3溶液中:OH- + HCO![]() = H2O + CO
= H2O + CO![]()
B.少量CO2通入NaOH溶液中:2OH- + CO2= CO![]() + H2O
+ H2O
C.盐酸加入NaHCO3溶液中:H+ + HCO![]() = H2O + CO2↑
= H2O + CO2↑
D.金属钠与水反应:Na + H2O = Na+ + OH- + H2 ↑
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3DZn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3DZn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)。
ZnO(s)+2Ni(OH)2(s)。

A. 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B. 充电时阳极反应为Ni(OH)2(s)+OH(aq)e![]() NiOOH(s)+H2O(l)
NiOOH(s)+H2O(l)
C. 放电时负极反应为Zn(s)+2OH(aq)2e![]() ZnO(s)+H2O(l)
ZnO(s)+H2O(l)
D. 放电过程中OH通过隔膜从负极区移向正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,下列溶液的碱性最强的是
A. pH=11的溶液
B. 0.1 mol/L Ba(OH)2溶液
C. 1 L含有4 g NaOH的溶液
D. Kw/c(H+)=1.0×10-2的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应COCl2(g) ![]() Cl2(g) + CO(g) △H>0达到平衡时各物质的浓度在不同条件下的变化状况如图所示(第10 min到14 min的COCl2浓度变化曲线未示出)。
Cl2(g) + CO(g) △H>0达到平衡时各物质的浓度在不同条件下的变化状况如图所示(第10 min到14 min的COCl2浓度变化曲线未示出)。
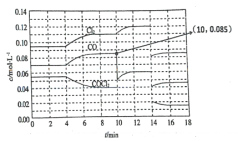
下列说法正确的是
A. 第4 min时改变的条件可能是扩大容器体积
B. 第2 min时的平衡常数K(2)大于第8 min时的平衡常数K(8)
C. 12 min时反应在温度T(8)下重新达到平衡,则此时c(COCl2) = 0.031 mol/L(结果保留两位有效数字)
D. 产物CO在2~3 min、5~6 min、12~13 min时的平均反应速率大小为:υ(5~6) > υ(2~3) > υ(12~13)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题小组探究乙酸乙酯(CH3COOC2H5)在不同温度、不同浓度NaOH溶液中的水解速率,取四支大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积来确定水解反应的速率。
实验试剂 | 试管Ⅰ(55 ℃) | 试管Ⅱ(55 ℃) | 试管Ⅲ(55 ℃) | 试管Ⅳ(75 ℃) |
乙酸乙酯/mL | 1 | V1 | V2 | V3 |
1 mol/L NaOH mL | V4 | 3 | 0 | V5 |
蒸馏水/mL | 0 | V6 | 5 | 2 |
已知:①水解反应CH3COOC2H5 + H2O ![]() CH3COOH + C2H5OH;
CH3COOH + C2H5OH;
②CH3COOC2H5难溶于水,密度比水小。
(1)V4 = ____________。
(2)①下列说法正确的是____________________________;
A、加入水,平衡正向移动
B、加入稀盐酸可使平衡逆向移动
C、酯层体积不再改变时,反应停止
D、c(CH3COOH) = c(C2H5OH)时,反应达平衡状态
②用各物质的浓度表示水解平衡常数Kh,则表达式为____________。
(3)实验中常用饱和食盐水代替蒸馏水,目的是减小乙酸乙酯在水中的溶解度,会使实验结果更准确,______________填“能”或“不能”)用饱和Na2CO3溶液代替蒸馏水。
(4)实验中,试管Ⅳ比试管Ⅱ中的酯层减少更快,可能的原因有_______。(乙酸乙酯的沸点为77.1 ℃)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是

A. 放电时,a电极反应为
B. 放电时,溶液中离子的数目增大
C. 充电时,b电极每增重![]() ,溶液中有
,溶液中有![]() 被氧化
被氧化
D. 充电时,a电极接外电源负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
|
|
|
|
A.4.03米大口径碳化硅反射镜 | B.2022年冬奥会聚氨酯速滑服 | C.能屏蔽电磁波的碳包覆银纳米线 | D.“玉兔二号”钛合金筛网轮 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
(1)甲烷水蒸气催化重整是制高纯氢的方法之一。
①反应器中初始反应的生成物为H2和CO2,其物质的量之比为4∶1,甲烷和水蒸气反应的方程式是______________。
②已知反应器中还存在如下反应:
i.CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1
ii.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2
iii.CH4(g)=C(s)+2H2(g) ΔH3
……
iii为积炭反应,利用ΔH1和ΔH2计算ΔH3时,还需要利用__________反应的ΔH。
③反应物投料比采用n(H2O)∶n(CH4)=4∶1,大于初始反应的化学计量数之比,目的是________________(选填字母序号)。
a.促进CH4转化 b.促进CO转化为CO2 c.减少积炭生成
④用CaO可以去除CO2。H2体积分数和CaO消耗率随时间变化关系如下图所示。从t1时开始,H2体积分数显著降低,单位时间CaO消耗率_______(填“升高”“降低”或“不变”)。此时CaO消耗率约为35%,但已失效,结合化学方程式解释原因:____________________________。

(2)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接_______________。
产生H2的电极反应式是_______________。
②改变开关连接方式,可得O2。
③结合①和②中电极3的电极反应式,说明电极3的作用:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示。下列关于该有机物的说法正确的是

A. 1mol 该有机物最多与4molH2反应生成C9H16O2
B. 该有机物中所有碳原子不可能处于同一平面上
C. 该有机物能发生酯化、加成、氧化、水解等反应
D. 与该有机物具有相同官能团的同分异构体有3种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com