
| A. | $\frac{{20M×{{10}^{-3}}}}{127}$g | B. | 20M g | C. | $\frac{{20×{{10}^{-3}}}}{M}$g | D. | $\frac{20}{M}$g |
分析 1kg食盐中至少含碘元素20mg,根据n=$\frac{m}{M}$计算I元素物质的量,再根据I元素守恒确定每千克食盐加入碘酸钾(KIO3)的物质的量,最后根据m=nM计算出加入碘酸钾的质量.
解答 解:1kg食盐中至少含碘元素20mg,即含Ⅰ物质的量为:$\frac{20×1{0}^{-3}g}{127g/mol}$mol=$\frac{20×1{0}^{-3}}{127}$mol,则每千克食盐中碘酸钾的物质的量为:n(KIO3)=n(I)=$\frac{20×1{0}^{-3}}{127}$mol,其质量为:$\frac{20×1{0}^{-3}}{127}$mol×Mg/mol=$\frac{20M×1{0}^{-3}}{127}$g,
故选A.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量之间的关系为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
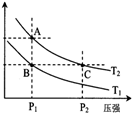 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池放电时,电池负极周围溶液的pH 不断增大 | |
| B. | 电池充电时,阳极反应为:Ni(OH)2+OH--e-═NiO(OH)+H2O | |
| C. | 电池充电时,氢元素被氧化 | |
| D. | 电池放电时,负极反应为:H2-2e-═2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该AgI胶粒带正电荷 | |
| B. | 该AgI胶体带负电荷 | |
| C. | 该AgI胶体进行电泳时,胶粒向阳极移动 | |
| D. | 该AgI胶体是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu | |
| B. | 氧化镁与稀盐酸混合:MgO+H+═Mg2++H2O | |
| C. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 相同温度下,同浓度的溶液的pH:CH3COONa>Na2CO3>NaHCO3>NaClO | |
| B. | 同温同浓度的三种溶液:①(NH4)2SO4②(NH4)2CO3③(NH4)2FeSO4 c (NH4+)大小:②>①>③ | |
| C. | 室温时pH=8的NaOH溶液与pH=8的氨水等体积混合pH等于8 | |
| D. | 向1mL0.1mol/L AgNO3溶液中滴加3~5滴0.1mol/L NaCl溶液,产生白色沉淀,再滴入KI溶液,沉淀变成黄色,由此推出:Ksp(AgI)<Ksp(AgCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合物中含氧原子的质量为1.6g | |
| B. | 原硝酸的物质的量浓度为2.0mol/L | |
| C. | 反应中产生标况下NO的体积为4.48L | |
| D. | 固体物质溶解后剩余HNO3为0.2mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com