
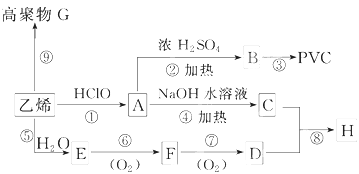
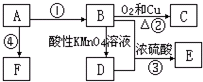
 ,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为
,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为 ,据此解答.
,据此解答. ,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为
,乙烯与水发生加成反应生成E为CH3CH2OH,乙醇在催化剂条件下发生氧化反应生成F为CH3CHO,CH3CHO可进一步氧化得到D为CH3COOH,反应①为乙烯与次氯酸发生加成反应生成A为HOCH2CH2Cl,A发生水解反应生成C为HOCH2CH2OH,(5)中C与D按物质的量之比为1:2反应生成H,则H为CH3COOCH2CH2OOCCH3,A发生消去反应生成B为CH2=CHCl,B在发生加聚反应得到PVC为 ,
, ,故答案为:碳碳双键、氯原子;
,故答案为:碳碳双键、氯原子; ;
;| Cu |
| △ |
| Cu |
| △ |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |


科目:高中化学 来源: 题型:
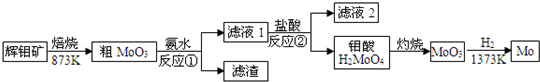
查看答案和解析>>
科目:高中化学 来源: 题型:
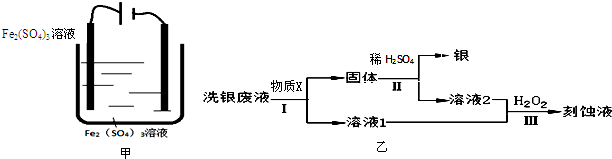
| 沉淀物 | 开始沉淀pH | 完全沉淀pH |
| Fe(OH)3 | 2.0 | 3.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
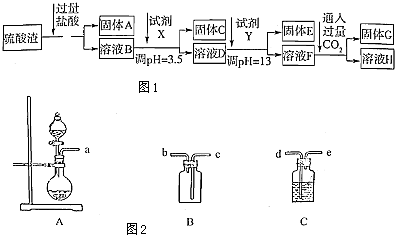 硫酸工业中废渣的成分为SiO2、Fe2O3、Al2O3、MgO.某探究性学习小组的同学设计以下实验方案,将硫酸渣中金属元素转化为氢氧化物沉淀分离开来.
硫酸工业中废渣的成分为SiO2、Fe2O3、Al2O3、MgO.某探究性学习小组的同学设计以下实验方案,将硫酸渣中金属元素转化为氢氧化物沉淀分离开来.| 阳离子 | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时的pH | 1.9 | 3.7 | 9.6 |
| 沉淀完全时的pH | 3.2 | 5.2 | 11.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚氯乙烯塑料制品可用于包装食品 |
| B、乙二醇可用于配制汽车防冻液 |
| C、部分卤代烃可用作灭火剂 |
| D、三硝基甲苯是一种黄色烈性炸药,常用于国防和民用爆破 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com