


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将NaAlO2溶液在蒸发皿中蒸干,最终得到的固体物质是Al(OH)3 |
| B、溶液中c(H+)>c(OH-),该溶液一定显酸性 |
| C、用原电池作电源进行电解时,电子从原电池负极流向电解池阴极 |
| D、外加电流的阴极保护法,构成了电解池;牺牲阳极的阴极保护法构成了原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
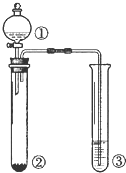
| A、①浓盐酸,②MnO2③NaOH,实验结论:制氯气并吸收尾气 |
| B、①浓硫酸,②蔗糖,③溴水,实验结论:浓硫酸具有脱水性、氧化 |
| C、①稀盐酸,②Na2SO3,③Ba(NO3)2溶液,实验结论:SO2与可溶性钡盐均可生成白色沉淀 |
| D、①浓硝酸,②Na2CO3,③Na2SiO3溶液,实验结论:酸性:硝酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3CHBrCH(OH)CH2CH3 |
| B、HCOOCH2CH(CH3)CH2OOCH |
| C、CH3CH(OH)CHO |
| D、CH2(OH)(CHOH)4CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用酒精萃取碘水中的碘 |
| B、用分液的方法除去NaCl溶液中含有的少量氢氧化铁胶体 |
| C、用溶解、过滤、蒸发的方法提纯含有少量CaCO3的KCl |
| D、用加硫酸钠溶液再过滤的方法提纯含少量硝酸钡的硝酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、△H<0 |
| B、Q2>Q1 |
| C、△H=2(Q1-Q2) |
| D、△H=Q1-Q2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com