
 ,故答案为:
,故答案为: ;
;
| ||
| ||


科目:高中化学 来源: 题型:
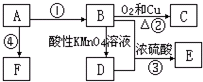
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、白醋中滴入石蕊试液呈红色 |
| B、pH试纸显示醋酸的pH为2~3 |
| C、蛋壳浸泡在白醋中有气体放出 |
| D、白醋加入豆浆中有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使甲基橙呈红色的溶液中K+、Na+、NO3-、S2O32- |
| B、无色透明溶液中:NH4+、Na+、SO42-、CH3COO- |
| C、使酚酞变红色的溶液中:Ba2+、Cl-、K+、NO3- |
| D、无色透明溶液中:SO42-、Cl-、K+、Cr2O72- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属气态氧化物都不是电解质 |
| B、SO2、NO2、C02都会导致酸雨的形成 |
| C、氮的氧化物都属于大气污染物 |
| D、Si、S的氧化物均属于酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、玻璃容器可长期盛放各种酸 |
| B、纯碱可用于清洗油污 |
| C、浓氨水可检验氯气管道漏气 |
| D、通过浓硫酸除去NH3中的H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:

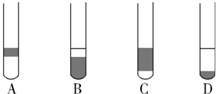
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、431kJ?mol-1 |
| B、946kJ?mol-1? |
| C、649kJ?mol-1 |
| D、869kJ?mol-1? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com