
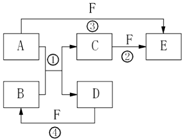
 A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出).
A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出). CO2↑+4NO2↑+2H2O,
CO2↑+4NO2↑+2H2O, CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O; ,E溶液中滴加KSCN溶液呈血红色,说明E溶液中含有Fe3+,A应为FeS2,F应为氧化性酸,可为HNO3,则B为H2SO4,FeS2与O2的反应为工业制备硫酸的重要反应,在沸腾炉中进行,反应的方程式为4FeS2+11O2
,E溶液中滴加KSCN溶液呈血红色,说明E溶液中含有Fe3+,A应为FeS2,F应为氧化性酸,可为HNO3,则B为H2SO4,FeS2与O2的反应为工业制备硫酸的重要反应,在沸腾炉中进行,反应的方程式为4FeS2+11O2 2Fe2O3+8SO2,
2Fe2O3+8SO2,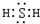 ; 4FeS2+11O2
; 4FeS2+11O2 2Fe2O3+8SO2;沸腾炉;
2Fe2O3+8SO2;沸腾炉; Si+2CO↑,SiO2可与烧碱反应,方程式为SiO2+2NaOH=Na2SiO3+H2O,
Si+2CO↑,SiO2可与烧碱反应,方程式为SiO2+2NaOH=Na2SiO3+H2O, Si+2CO↑; SiO2+2NaOH=Na2SiO3+H2O.
Si+2CO↑; SiO2+2NaOH=Na2SiO3+H2O.

科目:高中化学 来源: 题型:阅读理解
| 氟化物 | X | Y | Z |
| 熔点/K | 1266 | 1534 | 183 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 [化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.
[化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com