
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4 (g)![]() 2NO2 (g)△H,随温度升高,混合气体的颜色变深。回答下列问题:
2NO2 (g)△H,随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的△H ___0(填“﹥”或“﹤”);100℃时,体系中各物质浓度随时间变化如图所示。在0~60s时段,反应速率v(N2O4)为___________molL-1s-1,反应的平衡常数K为_______molL-1。
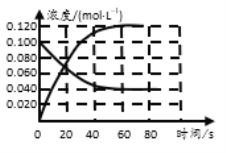
(2)100℃时,在容积为1.00L的容器中,通入1mol NO2(g)和1mol N2O4(g),此时v正_______ v逆(填“>”或“<”或“=”)。
【答案】> 1×10-3 0.36 <
【解析】
(1)随温度升高,混合气体的颜色变深,则表明平衡正向移动,由此得出反应的△H 与0的关系;在0~60s时段,反应速率v(N2O4)为![]() ,反应的平衡常数K为
,反应的平衡常数K为![]() 。
。
(2)100℃时,在容积为1.00L的容器中,通入1mol NO2(g)和1mol N2O4(g),利用浓度商与K进行比较,确定平衡移动的方向,从而确定v正与 v逆的相对大小。
(1)随温度升高,混合气体的颜色变深,则表明平衡正向移动,由此得出反应的△H>0;在0~60s时段,反应速率v(N2O4)为![]() =1×10-3molL-1s-1,反应的平衡常数K为
=1×10-3molL-1s-1,反应的平衡常数K为![]() =0.36molL-1。答案为:>;1×10-3;0.36;
=0.36molL-1。答案为:>;1×10-3;0.36;
(2)100℃时,在容积为1.00L的容器中,通入1mol NO2(g)和1mol N2O4(g),Q=![]() =1>0.36,所以平衡逆向移动,v正<v逆。答案为:<。
=1>0.36,所以平衡逆向移动,v正<v逆。答案为:<。


科目:高中化学 来源: 题型:
【题目】在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得各物质的浓度如下表。据此判断下列结论正确的是

A.在t3时刻反应已经停止
B.A的转化率比B的转化率低
C.在容器中发生的反应为: 2A+B![]() 2C
2C
D.在t2~t3内A的平均反应速率为:[1/(t3-t2)]mol·L-1·s-1[
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用如图所示装置进行有关实验:

(1)B是用来收集实验中产生的气体的装置,但未将导管画全,请在图上把导管补充完整_________。
(2)实验中他们取6.4 g铜片和12 mL 18 mol·L1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①写出铜跟浓硫酸反应的化学方程式:__________________;
②为什么有一定量的余酸但未能使铜片完全溶解,你认为原因是__________________;
③下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是________(填编号)。
A.铁粉 B.BaCl2溶液 C.银粉 D.Na2CO3溶液
(3)装置C中试管D内盛装的是品红溶液,当B中气体收集满后,有可能观察到的现象是_____________,待反应结束后,向C中烧杯内加入沸水,D中观察到的现象是_____________。
(4)实验装置C有可能造成环境污染,试用最简单的方法加以解决,__________________(实验用品自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丙叉环丙烷(n)由于其特殊的结构,一直受到结构和理论化学家的关注,它有如下转化关系。下列说法正确的是
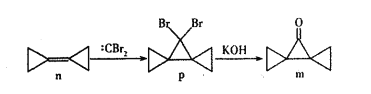
A. n分子中所有原子都在同一个平面上
B. n和:CBr2生成p的反应属于加成反应
C. p分子中极性键和非极性键数目之比为2:9
D. m分子同分异构体中属于芳香族化合物的共有四种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用相关化学知识进行判断,下列结论错误的是( )
A.蛋白质水解的最终产物是氨基酸
B.向饱和硼酸溶液中滴加![]() 溶液,有
溶液,有![]() 气体生成
气体生成
C.某吸热反应能自发进行,因此该反应是熵增反应
D.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种以软锰矿(主要成分为MnO2、SiO2、Al2O3)和黄铁矿(FeS2、SiO2)为原料冶炼金属锰的工艺流程如图所示:
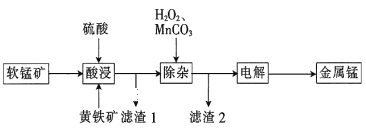
已知相关金属离子[c(Mn+)=0.1molL-1]形成氢氧化物沉淀的pH如下:
金属离子 | Fe3+ | Mn2+ | Al3+ |
开始沉淀的pH | 2.7 | 8.3 | 3.2 |
沉淀完全的pH | 3.7 | 9.8 | 5.0 |
回答下列问题:
(1)MnO2本身不能溶于硫酸,但是在Fe2+的作用下却能溶解,写出该反应的离子方程式:___。
(2)滤渣1的成分除了SiO2外,还有一种淡黄色的物质是___(填化学式)。
(3)除杂步骤中加入的MnCO3的作用是___,该过程需调节溶液pH的范围是___,若把pH调得过高,除了会使锰的产率会降低,其后果还有___。
(4)用惰性电极进行电解,电解刚开始时阴极的电极反应式为___,电解后阳极的电解质溶液可返回___(填“酸浸”“除杂”或“电解”)工序继续使用。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞作指示剂)的滴定曲线,下列说法正确的是
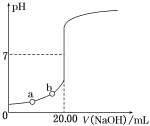
A. 水电离出的氢离子浓度:a<b
B. 盐酸的物质的量浓度为0.010 0 mol·L-1
C. 指示剂变色时,说明盐酸与NaOH恰好完全反应
D. 当滴加NaOH溶液为10.00 mL时,该混合液的pH=1+lg 3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】树脂交联程度决定了树脂的成膜性。下面是一种成膜性良好的醇酸型树脂的合成路线,如图所示。
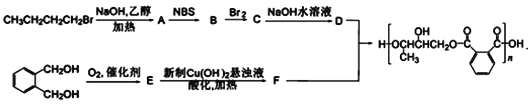
(1)B的分子式为C4H7Br,且B不存在顺反异构,B的结构简式为___,A到B步骤的反应类型是___。
(2)E中含氧官能团的名称是___,D的系统命名为___。
(3)下列说法正确的是___。
A.1mol化合物C最多消耗3molNaOH B.1mol化合物E与足量银氨溶液反应产生2molAg
C.F不会与Cu(OH)2悬浊液反应 D.丁烷、1-丁醇、化合物D中沸点最高的是丁烷
(4)写出D、F在一定条件下生成醇酸型树脂的化学方程式____。
(5)![]() 的符合下列条件的同分异构体有__种。
的符合下列条件的同分异构体有__种。
①苯的二取代衍生物 ②遇FeCl3溶液显紫色 ③可发生消去反应
(6)己知丙二酸二乙酯能发生以下反应:
![]()
以丙二酸二乙酯、1,3-丙二醇、乙醇钠为原料合成![]() ,请设计出合理的反应流程___。
,请设计出合理的反应流程___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于焓变(ΔH)的叙述或判断中错误的是

A. 2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,则该反应的 ΔH<0
B. 500 ℃、30 MPa下,0.5 mol N2和1.5 mol H2充分反应放出 19.3 kJ 热量,则反应“N2(g)+3H2(g) ![]() 2NH3(g)”的 ΔH=-38.6 kJ·mol-1
2NH3(g)”的 ΔH=-38.6 kJ·mol-1
C. 据下图1 知:ΔH1 = ΔH2+ΔH3
D. 据下图2 知:E的大小对该反应的ΔH 无影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com