
【题目】下列关于胶体的叙述不正确的是( )
A.胶体区别于其他分散系的本质特征是分散质微粒直径在10-9~10-7m之间
B.用平行光照射FeCl3溶液和Fe(OH)3胶体时,均能产生丁达尔现象
C.向豆浆中加入盐卤做豆腐是胶体聚沉在生活中的具体应用
D.溶液、胶体、浊液均属于混合物
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物的判断正确的是( )
A.有机化合物都是从有机体中提取分离出来的
B.有机化合物都能燃烧
C.有机化合物不一定都不溶于水
D.有机化合物不具备无机化合物的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室常用以下几种方法制取氯气。
(1)二氧化锰与浓盐酸反应制氯气,写出其反应的离子方程式:________________________________________________________________________。
(2)高锰酸钾与浓盐酸反应制氯气,写出其反应的化学方程式:________________________________________________________________________。
(3)氯酸钾与浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比为________。
Ⅱ.某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数的测定。
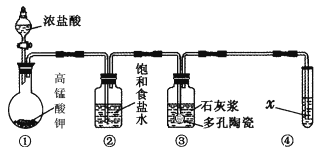
(1) 装置③中发生反应的化学方程式为____________________________,该反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法是________________________________________________________________________。
(2)测定漂白粉有效成分的质量分数:称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.100 0 mol·L-1KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为
3ClO-+I-===3Cl-+IO
IO+5I-+3H2O===6OH-+3I2
实验测得数据如下表所示。
滴定次数 | 1 | 2 | 3 |
KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
该漂白粉中有效成分的质量分数为________;若滴定过程中未充分振荡溶液,局部变浅蓝色时就停止滴定,则测定结果将________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+对于该平衡,下列叙述正确的是( )
CH3COO-+H+对于该平衡,下列叙述正确的是( )
A. 加入水时,平衡向逆反应方向移动
B. 加入少量NaOH固体,平衡向正反应方向移动
C. 加入少量0.1mol·L-1 HCl溶液,溶液中c(H+)减小
D. 加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )

A. a点时溶液中存在c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. 0~a段溶液中水电离出的OH-浓度先增大后减小
C. a=0.2
D. ab段发生反应的离子方程式为CO32-+2H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是重要的溶剂和替代燃料,工业上常以CO和H2的混合气体为原料在一定条件下制备甲醇。
(1)工业上可以通过下列途径获得H2,其中节能效果最好的是___________。
A.高温分解水制取H2:2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
B.电解水制取H2:2 H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
C.甲烷与水反应制取H2:CH4+ H2O![]() 3H2+CO
3H2+CO
D.在光催化剂作用下,利用太阳能分解水制取H2:2H2O![]() 2H2↑+ O2↑
2H2↑+ O2↑
(2)在2L的密闭容器中充入1mo1 CO和2mol H2,一定条件下发生反应;CO(g)+2H2(g) ![]() CH3OH(g),测得CO和CH3OH(g)的物质的量随时间的变化如下图所示。
CH3OH(g),测得CO和CH3OH(g)的物质的量随时间的变化如下图所示。
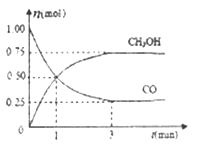
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____,平衡时氢气的体积分数为____。
②能够判断该反应达到平衡的是______。
A. CO、H2和CH3OH三种物质的浓度相等
B. 密闭容器中混合气体的密度不再改变
C. 密闭容器中混合气体的平均相对分子质量不再改变
D. 相同时间内消耗1mo1CO,同时消耗1mol CH3OH
(3)为使合成甲醇原料的原子利用率达到100%,实际生产中制备水煤气时还需使用CH4,则生产投料时,n(C):n(H2O):n(CH4)=__________。
(4)据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量是现用镍氢电池和锂电池的10倍,可连续使用一个月才充电一次。假定放电过程中,甲醇完全氧化产生的二氧化碳被充分吸收生成CO32-。则该电池负极的电极反应式为__________________,电池放电过程中溶液的pH将_____(填“下降”、“上升”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知白磷和P4O6的分子结构如图所示,又知化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查知P—P键能为198 kJ·mol-1、P—O键能为360 kJ·mol-1、O===O键能为498 kJ·mol-1。若生成1 mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
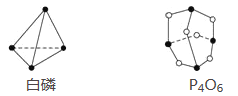
A. 吸收1 638 kJ能量 B. 放出1 638 kJ能量
C. 吸收126 kJ能量 D. 放出126 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图中所示的实验方法、装置或操作正确的是( )
|
|
A.测量锌与稀硫酸反应的速率 | B.证明非金属性:Cl>C>Si |
|
|
C.进行酸碱中和滴定实验 | D.测定中和热 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2009年,M IT的唐纳德·撒多维教授领导的小组研制出一种镁锑液态金属储能电池。电池突破了传统电池设计理念,以NaCl、KCl和MgCl2的熔融盐作为电解质。以Mg和Sb两极金属,整个电池在700℃工作,处在液体状态。由于密度的不同,在重力下分层,分别形成上层金属Mg,下层金属Sb和中间的NaCl、KCl及MgCl2电解质层。电池的工作原理如图所示,关于该电池的说法不正确的是 ( )
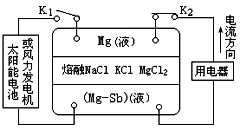
A. 电池充电时Cl—从上向下移动
B. 电池放电时正极的电极反应式为Mg2++2e—=Mg
C. 电池充电时阳极的电极反应式为:2Cl—-2e—=Cl2↑
D. 电池充电时中层熔融盐的组成不发生改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com